+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Local refinement of dimeric HMPV N-RNA bound to the C-terminal region of P | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Nucleoprotein / Virus / Nucleocapsid / RNA-binding / HMPV / Pneumoviridae / Mononegavirales / VIRAL PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報helical viral capsid / virion component / viral nucleocapsid / host cell cytoplasm / ribonucleoprotein complex / RNA-dependent RNA polymerase activity / RNA binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Human metapneumovirus (strain CAN97-83) (ウイルス) / Human metapneumovirus (strain CAN97-83) (ウイルス) /  | |||||||||
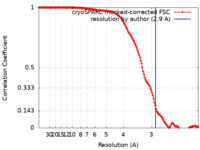
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Whitehead JD / Decool H / Leyrat C / Carrique L / Fix J / Eleouet JF / Galloux M / Renner M | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: Structure of the N-RNA/P interface indicates mode of L/P recruitment to the nucleocapsid of human metapneumovirus. 著者: Jack D Whitehead / Hortense Decool / Cédric Leyrat / Loic Carrique / Jenna Fix / Jean-François Eléouët / Marie Galloux / Max Renner /    要旨: Human metapneumovirus (HMPV) is a major cause of respiratory illness in young children. The HMPV polymerase (L) binds an obligate cofactor, the phosphoprotein (P). During replication and ...Human metapneumovirus (HMPV) is a major cause of respiratory illness in young children. The HMPV polymerase (L) binds an obligate cofactor, the phosphoprotein (P). During replication and transcription, the L/P complex traverses the viral RNA genome, which is encapsidated within nucleoproteins (N). An essential interaction between N and a C-terminal region of P tethers the L/P polymerase to the template. This N-P interaction is also involved in the formation of cytoplasmic viral factories in infected cells, called inclusion bodies. To define how the polymerase component P recognizes N-encapsidated RNA (N-RNA) we employed cryogenic electron microscopy (cryo-EM) and molecular dynamics simulations, coupled to activity assays and imaging of inclusion bodies in cells. We report a 2.9 Å resolution structure of a triple-complex between multimeric N, bound to both RNA and the C-terminal region of P. Furthermore, we also present cryo-EM structures of assembled N in different oligomeric states, highlighting the plasticity of N. Combined with our functional assays, these structural data delineate in molecular detail how P attaches to N-RNA whilst retaining substantial conformational dynamics. Moreover, the N-RNA-P triple complex structure provides a molecular blueprint for the design of therapeutics to potentially disrupt the attachment of L/P to its template. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_17620.map.gz emd_17620.map.gz | 1.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-17620-v30.xml emd-17620-v30.xml emd-17620.xml emd-17620.xml | 18.2 KB 18.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_17620_fsc.xml emd_17620_fsc.xml | 14.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_17620.png emd_17620.png | 77.1 KB | ||
| Filedesc metadata |  emd-17620.cif.gz emd-17620.cif.gz | 6 KB | ||
| その他 |  emd_17620_half_map_1.map.gz emd_17620_half_map_1.map.gz emd_17620_half_map_2.map.gz emd_17620_half_map_2.map.gz | 226.8 MB 226.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-17620 http://ftp.pdbj.org/pub/emdb/structures/EMD-17620 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17620 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17620 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_17620_validation.pdf.gz emd_17620_validation.pdf.gz | 718 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_17620_full_validation.pdf.gz emd_17620_full_validation.pdf.gz | 717.5 KB | 表示 | |
| XML形式データ |  emd_17620_validation.xml.gz emd_17620_validation.xml.gz | 21 KB | 表示 | |
| CIF形式データ |  emd_17620_validation.cif.gz emd_17620_validation.cif.gz | 27.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17620 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17620 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17620 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17620 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8pdsMC  8pdlC  8pdmC  8pdnC  8pdoC  8pdpC  8pdqC  8pdrC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_17620.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_17620.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.05 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_17620_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
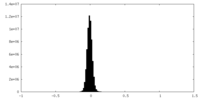
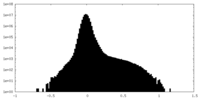
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_17620_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
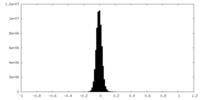
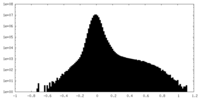
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Local refinement of dimeric HMPV N-RNA bound to the C-terminal re...
| 全体 | 名称: Local refinement of dimeric HMPV N-RNA bound to the C-terminal region of P |
|---|---|
| 要素 |
|
-超分子 #1: Local refinement of dimeric HMPV N-RNA bound to the C-terminal re...
| 超分子 | 名称: Local refinement of dimeric HMPV N-RNA bound to the C-terminal region of P タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#3 |
|---|
-超分子 #2: Nucleoprotein
| 超分子 | 名称: Nucleoprotein / タイプ: complex / ID: 2 / 親要素: 1 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Human metapneumovirus (strain CAN97-83) (ウイルス) Human metapneumovirus (strain CAN97-83) (ウイルス)株: CAN97-83 |
-超分子 #3: RNA
| 超分子 | 名称: RNA / タイプ: complex / ID: 3 / 親要素: 1 / 含まれる分子: #2 |
|---|---|
| 由来(天然) | 生物種:  |
-超分子 #4: Human metapneumovirus P C-terminal region
| 超分子 | 名称: Human metapneumovirus P C-terminal region / タイプ: complex / ID: 4 / 親要素: 1 / 含まれる分子: #3 |
|---|---|
| 由来(天然) | 生物種:  Human metapneumovirus (strain CAN97-83) (ウイルス) Human metapneumovirus (strain CAN97-83) (ウイルス)株: CAN97-83 |
-分子 #1: Nucleoprotein
| 分子 | 名称: Nucleoprotein / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Human metapneumovirus (strain CAN97-83) (ウイルス) Human metapneumovirus (strain CAN97-83) (ウイルス)株: CAN97-83 |
| 分子量 | 理論値: 43.57652 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSLQGIHLSD LSYKHAILKE SQYTIKRDVG TTTAVTPSSL QQEITLLCGE ILYAKHADYK YAAEIGIQYI STALGSERVQ QILRNSGSE VQVVLTRTYS LGKIKNNKGE DLQMLDIHGV EKSWVEEIDK EARKTMATLL KESSGNIPQN QRPSAPDTPI I LLCVGALI ...文字列: MSLQGIHLSD LSYKHAILKE SQYTIKRDVG TTTAVTPSSL QQEITLLCGE ILYAKHADYK YAAEIGIQYI STALGSERVQ QILRNSGSE VQVVLTRTYS LGKIKNNKGE DLQMLDIHGV EKSWVEEIDK EARKTMATLL KESSGNIPQN QRPSAPDTPI I LLCVGALI FTKLASTIEV GLETTVRRAN RVLSDALKRY PRMDIPKIAR SFYDLFEQKV YHRSLFIEYG KALGSSSTGS KA ESLFVNI FMQAYGAGQT MLRWGVIARS SNNIMLGHVS VQAELKQVTE VYDLVREMGP ESGLLHLRQS PKAGLLSLAN CPN FASVVL GNASGLGIIG MYRGRVPNTE LFSAAESYAK SLKESNKINF SSLGLTDEEK EAAEHFLNVS DDSQNDYE UniProtKB: Nucleoprotein |
-分子 #3: Phosphoprotein
| 分子 | 名称: Phosphoprotein / タイプ: protein_or_peptide / ID: 3 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Human metapneumovirus (strain CAN97-83) (ウイルス) Human metapneumovirus (strain CAN97-83) (ウイルス) |
| 分子量 | 理論値: 895.075 Da |
| 配列 | 文字列: DIYQLIM UniProtKB: Phosphoprotein |
-分子 #2: RNA
| 分子 | 名称: RNA / タイプ: rna / ID: 2 詳細: E.coli RNA, co-purified with N. Due to mixed sequence, modelled as poly-C コピー数: 1 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 4.227587 KDa |
| 配列 | 文字列: CCCCCCCCCC CCCC |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 8 / 詳細: 12.5 mM Tris-HCl, pH 8.0, 125 mM NaCl |
| 凍結 | 凍結剤: ETHANE-PROPANE / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 44.2 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.6 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー











 Z
Z Y
Y X
X