+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Human RAD51B-RAD51C-RAD51D-XRCC2 (BCDX2) complex, 2.2 A resolution | ||||||||||||||||||
 マップデータ マップデータ | |||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||
 キーワード キーワード | Complex / ssDNA-binding / ATPase / RAD51 / DNA BINDING PROTEIN | ||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報meiotic DNA recombinase assembly / Rad51B-Rad51C-Rad51D-XRCC2 complex / Rad51C-XRCC3 complex / female meiosis sister chromatid cohesion / crossover junction DNA endonuclease activity / telomere maintenance via recombination / Impaired BRCA2 binding to PALB2 / reciprocal meiotic recombination / Homologous DNA Pairing and Strand Exchange / Defective homologous recombination repair (HRR) due to BRCA1 loss of function ...meiotic DNA recombinase assembly / Rad51B-Rad51C-Rad51D-XRCC2 complex / Rad51C-XRCC3 complex / female meiosis sister chromatid cohesion / crossover junction DNA endonuclease activity / telomere maintenance via recombination / Impaired BRCA2 binding to PALB2 / reciprocal meiotic recombination / Homologous DNA Pairing and Strand Exchange / Defective homologous recombination repair (HRR) due to BRCA1 loss of function / Defective HDR through Homologous Recombination Repair (HRR) due to PALB2 loss of BRCA1 binding function / Defective HDR through Homologous Recombination Repair (HRR) due to PALB2 loss of BRCA2/RAD51/RAD51C binding function / Resolution of D-loop Structures through Synthesis-Dependent Strand Annealing (SDSA) / Resolution of D-loop Structures through Holliday Junction Intermediates / sister chromatid cohesion / ATP-dependent DNA damage sensor activity / male meiosis I / Presynaptic phase of homologous DNA pairing and strand exchange / positive regulation of G2/M transition of mitotic cell cycle / replication fork / double-strand break repair via homologous recombination / HDR through Homologous Recombination (HRR) / Meiotic recombination / cell junction / Factors involved in megakaryocyte development and platelet production / spermatogenesis / DNA recombination / intracellular membrane-bounded organelle / DNA repair / perinuclear region of cytoplasm / mitochondrion / DNA binding / nucleoplasm / ATP binding / nucleus / cytosol / cytoplasm 類似検索 - 分子機能 | ||||||||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||||||||
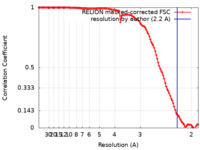
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.2 Å | ||||||||||||||||||
 データ登録者 データ登録者 | Greenhough LA / Liang CC / West SC | ||||||||||||||||||
| 資金援助 |  英国, European Union, 5件 英国, European Union, 5件
| ||||||||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2023 ジャーナル: Nature / 年: 2023タイトル: Structure and function of the RAD51B-RAD51C-RAD51D-XRCC2 tumour suppressor. 著者: Luke A Greenhough / Chih-Chao Liang / Ondrej Belan / Simone Kunzelmann / Sarah Maslen / Monica C Rodrigo-Brenni / Roopesh Anand / Mark Skehel / Simon J Boulton / Stephen C West /   要旨: Homologous recombination is a fundamental process of life. It is required for the protection and restart of broken replication forks, the repair of chromosome breaks and the exchange of genetic ...Homologous recombination is a fundamental process of life. It is required for the protection and restart of broken replication forks, the repair of chromosome breaks and the exchange of genetic material during meiosis. Individuals with mutations in key recombination genes, such as BRCA2 (also known as FANCD1), or the RAD51 paralogues RAD51B, RAD51C (also known as FANCO), RAD51D, XRCC2 (also known as FANCU) and XRCC3, are predisposed to breast, ovarian and prostate cancers and the cancer-prone syndrome Fanconi anaemia. The BRCA2 tumour suppressor protein-the product of BRCA2-is well characterized, but the cellular functions of the RAD51 paralogues remain unclear. Genetic knockouts display growth defects, reduced RAD51 focus formation, spontaneous chromosome abnormalities, sensitivity to PARP inhibitors and replication fork defects, but the precise molecular roles of RAD51 paralogues in fork stability, DNA repair and cancer avoidance remain unknown. Here we used cryo-electron microscopy, AlphaFold2 modelling and structural proteomics to determine the structure of the RAD51B-RAD51C-RAD51D-XRCC2 complex (BCDX2), revealing that RAD51C-RAD51D-XRCC2 mimics three RAD51 protomers aligned within a nucleoprotein filament, whereas RAD51B is highly dynamic. Biochemical and single-molecule analyses showed that BCDX2 stimulates the nucleation and extension of RAD51 filaments-which are essential for recombinational DNA repair-in reactions that depend on the coupled ATPase activities of RAD51B and RAD51C. Our studies demonstrate that BCDX2 orchestrates RAD51 assembly on single stranded DNA for replication fork protection and double strand break repair, in reactions that are critical for tumour avoidance. | ||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_17206.map.gz emd_17206.map.gz | 6.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-17206-v30.xml emd-17206-v30.xml emd-17206.xml emd-17206.xml | 28.5 KB 28.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_17206_fsc.xml emd_17206_fsc.xml | 11.3 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_17206.png emd_17206.png | 60 KB | ||
| マスクデータ |  emd_17206_msk_1.map emd_17206_msk_1.map | 125 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-17206.cif.gz emd-17206.cif.gz | 7.8 KB | ||
| その他 |  emd_17206_additional_1.map.gz emd_17206_additional_1.map.gz emd_17206_half_map_1.map.gz emd_17206_half_map_1.map.gz emd_17206_half_map_2.map.gz emd_17206_half_map_2.map.gz | 98.7 MB 98.7 MB 98.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-17206 http://ftp.pdbj.org/pub/emdb/structures/EMD-17206 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17206 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17206 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_17206_validation.pdf.gz emd_17206_validation.pdf.gz | 657 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_17206_full_validation.pdf.gz emd_17206_full_validation.pdf.gz | 656.6 KB | 表示 | |
| XML形式データ |  emd_17206_validation.xml.gz emd_17206_validation.xml.gz | 18.3 KB | 表示 | |
| CIF形式データ |  emd_17206_validation.cif.gz emd_17206_validation.cif.gz | 24.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17206 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17206 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17206 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17206 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_17206.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_17206.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.95625 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_17206_msk_1.map emd_17206_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: #1
| ファイル | emd_17206_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_17206_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_17206_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : RAD51B-RAD51C-RAD51D-XRCC2 (BCDX2)
| 全体 | 名称: RAD51B-RAD51C-RAD51D-XRCC2 (BCDX2) |
|---|---|
| 要素 |
|
-超分子 #1: RAD51B-RAD51C-RAD51D-XRCC2 (BCDX2)
| 超分子 | 名称: RAD51B-RAD51C-RAD51D-XRCC2 (BCDX2) / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#4 詳細: Recombinant BCDX2 complexes purified from Sf9 insect cells, crosslinked with 0.005% glutaraldehyde (RT, 10 minutes) in the presence of 30 nt ssDNA, and vitrified in the presence of ADP.AlFx. ...詳細: Recombinant BCDX2 complexes purified from Sf9 insect cells, crosslinked with 0.005% glutaraldehyde (RT, 10 minutes) in the presence of 30 nt ssDNA, and vitrified in the presence of ADP.AlFx. THERE IS NO ssDNA BOUND TO BCDX2 IN THIS STRUCTURE |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: DNA repair protein RAD51 homolog 2
| 分子 | 名称: DNA repair protein RAD51 homolog 2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 38.296984 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGSKKLKRVG LSQELCDRLS RHQILTCQDF LCLSPLELMK VTGLSYRGVH ELLCMVSRAC APKMQTAYGI KAQRSADFSP AFLSTTLSA LDEALHGGVA CGSLTEITGP PGCGKTQFCI MMSILATLPT NMGGLEGAVV YIDTESAFSA ERLVEIAESR F PRYFNTEE ...文字列: MGSKKLKRVG LSQELCDRLS RHQILTCQDF LCLSPLELMK VTGLSYRGVH ELLCMVSRAC APKMQTAYGI KAQRSADFSP AFLSTTLSA LDEALHGGVA CGSLTEITGP PGCGKTQFCI MMSILATLPT NMGGLEGAVV YIDTESAFSA ERLVEIAESR F PRYFNTEE KLLLTSSKVH LYRELTCDEV LQRIESLEEE IISKGIKLVI LDSVASVVRK EFDAQLQGNL KERNKFLARE AS SLKYLAE EFSIPVILTN QITTHLSGAL ASQADLVSPA DDLSLSEGTS GSSCVIAALG NTWSHSVNTR LILQYLDSER RQI LIAKSP LAPFTSFVYT IKEEGLVLQA YGNS UniProtKB: UNIPROTKB: O15315 |
-分子 #2: DNA repair protein RAD51 homolog 3
| 分子 | 名称: DNA repair protein RAD51 homolog 3 / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 42.244609 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MRGKTFRFEM QRDLVSFPLS PAVRVKLVSA GFQTAEELLE VKPSELSKEV GISKAEALET LQIIRRECLT NKPRYAGTSE SHKKCTALE LLEQEHTQGF IITFCSALDD ILGGGVPLMK TTEICGAPGV GKTQLCMQLA VDVQIPECFG GVAGEAVFID T EGSFMVDR ...文字列: MRGKTFRFEM QRDLVSFPLS PAVRVKLVSA GFQTAEELLE VKPSELSKEV GISKAEALET LQIIRRECLT NKPRYAGTSE SHKKCTALE LLEQEHTQGF IITFCSALDD ILGGGVPLMK TTEICGAPGV GKTQLCMQLA VDVQIPECFG GVAGEAVFID T EGSFMVDR VVDLATACIQ HLQLIAEKHK GEEHRKALED FTLDNILSHI YYFRCRDYTE LLAQVYLLPD FLSEHSKVRL VI VDGIAFP FRHDLDDLSL RTRLLNGLAQ QMISLANNHR LAVILTNQMT TKIDRNQALL VPALGESWGH AATIRLIFHW DRK QRLATL YKSPSQKECT VLFQIKPQGF RDTVVTSACS LQTEGSLSTR KRSRDPEEEL UniProtKB: DNA repair protein RAD51 homolog 3 |
-分子 #3: DNA repair protein RAD51 homolog 4
| 分子 | 名称: DNA repair protein RAD51 homolog 4 / タイプ: protein_or_peptide / ID: 3 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 35.084254 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGVLRVGLCP GLTEEMIQLL RSHRIKTVVD LVSADLEEVA QKCGLSYKAL VALRRVLLAQ FSAFPVNGAD LYEELKTSTA ILSTGIGSL DKLLDAGLYT GEVTEIVGGP GSGKTQVCLC MAANVAHGLQ QNVLYVDSNG GLTASRLLQL LQAKTQDEEE Q AEALRRIQ ...文字列: MGVLRVGLCP GLTEEMIQLL RSHRIKTVVD LVSADLEEVA QKCGLSYKAL VALRRVLLAQ FSAFPVNGAD LYEELKTSTA ILSTGIGSL DKLLDAGLYT GEVTEIVGGP GSGKTQVCLC MAANVAHGLQ QNVLYVDSNG GLTASRLLQL LQAKTQDEEE Q AEALRRIQ VVHAFDIFQM LDVLQELRGT VAQQVTGSSG TVKVVVVDSV TAVVSPLLGG QQREGLALMM QLARELKTLA RD LGMAVVV TNHITRDRDS GRLKPALGRS WSFVPSTRIL LDTIEGAGAS GGRRMACLAK SSRQPTGFQE MVDIGTWGTS EQS ATLQGD QT UniProtKB: UNIPROTKB: O75771 |
-分子 #4: DNA repair protein XRCC2
| 分子 | 名称: DNA repair protein XRCC2 / タイプ: protein_or_peptide / ID: 4 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 31.921381 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: GCSAFHRAES GTELLARLEG RSSLKEIEPN LFADEDSPVH GDILEFHGPE GTGKTEMLYH LTARCILPKS EGGLEVEVLF IDTDYHFDM LRLVTILEHR LSQSSEEIIK YCLGRFFLVY CSSSTHLLLT LYSLESMFCS HPSLCLLILD SLSAFYWIDR V NGGESVNL ...文字列: GCSAFHRAES GTELLARLEG RSSLKEIEPN LFADEDSPVH GDILEFHGPE GTGKTEMLYH LTARCILPKS EGGLEVEVLF IDTDYHFDM LRLVTILEHR LSQSSEEIIK YCLGRFFLVY CSSSTHLLLT LYSLESMFCS HPSLCLLILD SLSAFYWIDR V NGGESVNL QESTLRKCSQ CLEKLVNDYR LVLFATTQTI MQKASSSSEE PSHASRRLCD VDIDYRPYLC KAWQQLVKHR MF FSKQDDS QSSNQFSLVS RCLKSNSLKK HFFIIGESGV EFC UniProtKB: UNIPROTKB: O43543 |
-分子 #5: ADENOSINE-5'-DIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 5 / コピー数: 1 / 式: ADP |
|---|---|
| 分子量 | 理論値: 427.201 Da |
| Chemical component information |  ChemComp-ADP: |
-分子 #6: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 6 / コピー数: 3 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-分子 #7: ADENOSINE-5'-TRIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-TRIPHOSPHATE / タイプ: ligand / ID: 7 / コピー数: 2 / 式: ATP |
|---|---|
| 分子量 | 理論値: 507.181 Da |
| Chemical component information |  ChemComp-ATP: |
-分子 #8: water
| 分子 | 名称: water / タイプ: ligand / ID: 8 / コピー数: 142 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.25 mg/mL | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
詳細: 25 mM HEPES pH 7.5, 100 mM NaCl, 2.5 mM MgCl2, 0.5 mM ADP.AlFx (0.5 mM ADP, 0.5 mM AlCl3, 10 mM NaF), 0.25 mM TCEP, 0.00075% Tween20, 0.075 mM CHAPSO | ||||||||||||||||||||||||||||||
| グリッド | モデル: UltrAuFoil R2/2 / 材質: GOLD / メッシュ: 200 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: AIR / 詳細: 45 mA | ||||||||||||||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 撮影したグリッド数: 1 / 実像数: 35305 / 平均露光時間: 2.78 sec. / 平均電子線量: 53.2 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.25 µm / 最小 デフォーカス(公称値): 0.75 µm / 倍率(公称値): 105000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Source name: PDB / Chain - Initial model type: experimental model |
|---|---|
| 詳細 | PDB-8OUY was initially docked into the postprocessed map using ChimeraX 1.4, and iteratively real space refined with Phenix and manually modified using COOT |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 温度因子: 50.38 |
| 得られたモデル |  PDB-8ouz: |
 ムービー
ムービー コントローラー
コントローラー









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)