+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-12027 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM map of calcium-bound mTMEM16A(ac)-I551A chloride channel at 4.1 A resolution | |||||||||||||||
 マップデータ マップデータ | Cryo-EM map of calcium-bound mTMEM16A(ac)-I551A chloride channel at 4.1 A resolution | |||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | ligand-gated ion channel / anoctamin-1 / MEMBRANE PROTEIN | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報glial cell projection elongation / trachea development / iodide transmembrane transporter activity / mucus secretion / iodide transport / intracellularly calcium-gated chloride channel activity / cellular response to peptide / Stimuli-sensing channels / voltage-gated chloride channel activity / calcium-activated cation channel activity ...glial cell projection elongation / trachea development / iodide transmembrane transporter activity / mucus secretion / iodide transport / intracellularly calcium-gated chloride channel activity / cellular response to peptide / Stimuli-sensing channels / voltage-gated chloride channel activity / calcium-activated cation channel activity / protein localization to membrane / chloride transport / detection of temperature stimulus involved in sensory perception of pain / chloride channel activity / chloride channel complex / chloride transmembrane transport / regulation of membrane potential / cellular response to heat / presynaptic membrane / phospholipase C-activating G protein-coupled receptor signaling pathway / apical plasma membrane / signaling receptor binding / external side of plasma membrane / glutamatergic synapse / protein homodimerization activity / nucleoplasm / metal ion binding / identical protein binding / plasma membrane 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  | |||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.1 Å | |||||||||||||||
 データ登録者 データ登録者 | Lam AKM / Rheinberger J | |||||||||||||||
| 資金援助 |  スイス, スイス,  オランダ, 4件 オランダ, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2021 ジャーナル: Nat Commun / 年: 2021タイトル: Gating the pore of the calcium-activated chloride channel TMEM16A. 著者: Andy K M Lam / Jan Rheinberger / Cristina Paulino / Raimund Dutzler /   要旨: The binding of cytoplasmic Ca to the anion-selective channel TMEM16A triggers a conformational change around its binding site that is coupled to the release of a gate at the constricted neck of an ...The binding of cytoplasmic Ca to the anion-selective channel TMEM16A triggers a conformational change around its binding site that is coupled to the release of a gate at the constricted neck of an hourglass-shaped pore. By combining mutagenesis, electrophysiology, and cryo-electron microscopy, we identified three hydrophobic residues at the intracellular entrance of the neck as constituents of this gate. Mutation of each of these residues increases the potency of Ca and results in pronounced basal activity. The structure of an activating mutant shows a conformational change of an α-helix that contributes to Ca binding as a likely cause for the basal activity. Although not in physical contact, the three residues are functionally coupled to collectively contribute to the stabilization of the gate in the closed conformation of the pore, thus explaining the low open probability of the channel in the absence of Ca. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_12027.map.gz emd_12027.map.gz | 58.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-12027-v30.xml emd-12027-v30.xml emd-12027.xml emd-12027.xml | 18.6 KB 18.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_12027.png emd_12027.png | 173.7 KB | ||
| マスクデータ |  emd_12027_msk_1.map emd_12027_msk_1.map | 64 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-12027.cif.gz emd-12027.cif.gz | 6.5 KB | ||
| その他 |  emd_12027_half_map_1.map.gz emd_12027_half_map_1.map.gz emd_12027_half_map_2.map.gz emd_12027_half_map_2.map.gz | 48.4 MB 48.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-12027 http://ftp.pdbj.org/pub/emdb/structures/EMD-12027 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12027 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12027 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_12027.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_12027.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Cryo-EM map of calcium-bound mTMEM16A(ac)-I551A chloride channel at 4.1 A resolution | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
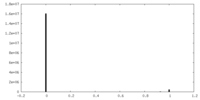
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.012 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_12027_msk_1.map emd_12027_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
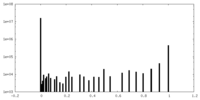
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_12027_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
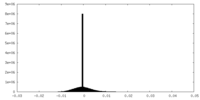
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_12027_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
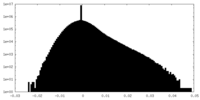
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : mTMEM16A(ac)-I551A in calcium-bound form
| 全体 | 名称: mTMEM16A(ac)-I551A in calcium-bound form |
|---|---|
| 要素 |
|
-超分子 #1: mTMEM16A(ac)-I551A in calcium-bound form
| 超分子 | 名称: mTMEM16A(ac)-I551A in calcium-bound form / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 221.908 KDa |
-分子 #1: Anoctamin-1
| 分子 | 名称: Anoctamin-1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 111.016914 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MRVPEKYSTL PAEDRSVHIV NICAIEDLGY LPSEGTLLNS LSVDPDAECK YGLYFRDGKR KVDYILVYHH KRASGSRTLA RRGLQNDMV LGTRSVRQDQ PLPGKGSPVD AGSPEVPMDY HEDDKRFRRE EYEGNLLEAG LELENDEDTK IHGVGFVKIH A PWHVLCRE ...文字列: MRVPEKYSTL PAEDRSVHIV NICAIEDLGY LPSEGTLLNS LSVDPDAECK YGLYFRDGKR KVDYILVYHH KRASGSRTLA RRGLQNDMV LGTRSVRQDQ PLPGKGSPVD AGSPEVPMDY HEDDKRFRRE EYEGNLLEAG LELENDEDTK IHGVGFVKIH A PWHVLCRE AEFLKLKMPT KKVYHISETR GLLKTINSVL QKITDPIQPK VAEHRPQTTK RLSYPFSREK QHLFDLTDRD SF FDSKTRS TIVYEILKRT TCTKAKYSMG ITSLLANGVY SAAYPLHDGD YEGDNVEFND RKLLYEEWAS YGVFYKYQPI DLV RKYFGE KVGLYFAWLG AYTQMLIPAS IVGVIVFLYG CATVDENIPS MEMCDQRYNI TMCPLCDKTC SYWKMSSACA TARA SHLFD NPATVFFSVF MALWAATFME HWKRKQMRLN YRWDLTGFEE EEEAVKDHPR AEYEARVLEK SLRKESRNKE TDKVK LTWR DRFPAYFTNL VSIIFMIAVT FAIVLGVIIY RISTAAALAM NSSPSVRSNI RVTVTATAVI INLVVIALLD EVYGCI ARW LTKIEVPKTE KSFEERLTFK AFLLKFVNSY TPIFYVAFFK GRFVGRPGDY VYIFRSFRME ECAPGGCLME LCIQLSI IM LGKQLIQNNL FEIGIPKMKK FIRYLKLRRQ SPSDREEYVK RKQRYEVDFN LEPFAGLTPE YMEMIIQFGF VTLFVASF P LAPLFALLNN IIEIRLDAKK FVTELRRPVA IRAKDIGIWY NILRGVGKLA VIINAFVISF TSDFIPRLVY LYMYSQNGT MHGFVNHTLS SFNVSDFQNG TAPNDPLDLG YEVQICRYKD YREPPWSEHK YDISKDFWAV LAARLAFVIV FQNLVMFMSD FVDWVIPDI PKDISQQIHK EKVLMVELFM REEQGKQQLL DTWMEKEKPR DVPCNNHSPT THPEAGDGSP VPSYEYHGDA L UniProtKB: Anoctamin-1 |
-分子 #2: CALCIUM ION
| 分子 | 名称: CALCIUM ION / タイプ: ligand / ID: 2 / コピー数: 4 / 式: CA |
|---|---|
| 分子量 | 理論値: 40.078 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.4 構成要素:
詳細: CaCl2 was added immediately before freezing Free calcium concentration is 1mM. | ||||||||||||||
| 凍結 | 凍結剤: ETHANE-PROPANE / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / 平均電子線量: 53.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 49407 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー


















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)