+検索条件
-Structure paper
| タイトル | Gβγ engages PLCβ3 at multiple sites to reorient and facilitate its activation. |
|---|---|
| ジャーナル・号・ページ | bioRxiv, Year 2026 |
| 掲載日 | 2026年1月14日 |
 著者 著者 | Isaac J Fisher / Kanishka Senarath / Kennedy Outlaw / Kaushik Muralidharan / Elisabeth E Garland-Kuntz / Michelle Van Camp / Tommy Komay / Asuka Inoue / Eva Kostenis / Nevin A Lambert / Angeline M Lyon /    |
| PubMed 要旨 | Phospholipase C β (PLCβ) enzymes are activated by heterotrimeric G protein subunits, increasing hydrolysis of phosphatidylinositol-4,5-bisphosphate (PIP2) at the plasma membrane. All four human ...Phospholipase C β (PLCβ) enzymes are activated by heterotrimeric G protein subunits, increasing hydrolysis of phosphatidylinositol-4,5-bisphosphate (PIP2) at the plasma membrane. All four human PLCβ isoforms (PLCβ1-4) are activated by Gα, while PLCβ1-3 are activated to varying extents by Gβγ. The binding sites for Gα on PLCβ are well-established and much has been learned about its mechanism of activation, but comparatively little is known about Gβγ-dependent activation. In this work, we used cryo-electron microscopy (cryo-EM) single particle analysis (SPA), functional assays, and bioluminescence resonance energy transfer (BRET) to investigate how Gβγ interacts with PLCβ3 in concert with activated Gα to regulate phospholipase activity. Gβγ heterodimers bind multiple surfaces of PLCβ3 to promote activation but alone do not recruit the enzyme to the plasma membrane. Instead, Gβγ facilitates activation by Gα, most likely by reorienting the phospholipase catalytic site at the membrane to maximize PIP2 hydrolysis and downstream Ca release. Cell-based functional assays demonstrate that Gβγ is required for maximal PLCβ3 activation even when G heterotrimers are the sole source of Gβγ. Together, these findings demonstrate that Gβγ acts as a critical positive allosteric modulator that regularly acts in concert with Gα to activate PLCβ3 at the plasma membrane. |
 リンク リンク |  bioRxiv / bioRxiv /  PubMed:41648476 / PubMed:41648476 /  PubMed Central PubMed Central |
| 手法 | EM (単粒子) |
| 解像度 | 4.4 - 7.0 Å |
| 構造データ | EMDB-72655, PDB-9y7h: EMDB-72732, PDB-9yao: EMDB-72733, PDB-9yap: |
| 化合物 | 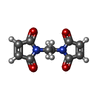 ChemComp-ME7:  ChemComp-CA: |
| 由来 |
|
 キーワード キーワード | SIGNALING PROTEIN / heterotrimeric G protein / phospholipase / lipase / calcium signaling / G protein |
 ムービー
ムービー コントローラー
コントローラー 構造ビューア
構造ビューア 万見文献について
万見文献について









 homo sapiens (ヒト)
homo sapiens (ヒト)
