+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Tube assembly of Atg18-WT | |||||||||
 マップデータ マップデータ | sharp map from CryoSPARC software | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  autophagy (オートファジー) / membrane remodeling / PIP binding / autophagy (オートファジー) / membrane remodeling / PIP binding /  PI3P / PI(3 / 5)P2 / lipid binding protein / PI3P / PI(3 / 5)P2 / lipid binding protein /  MEMBRANE PROTEIN (膜タンパク質) MEMBRANE PROTEIN (膜タンパク質) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報regulation of phosphatidylinositol biosynthetic process / PAS complex / 1-phosphatidyl-1D-myo-inositol 3,5-bisphosphate metabolic process / phagophore /  vacuolar protein processing / positive regulation of vacuole organization / vacuolar protein processing / positive regulation of vacuole organization /  オートファジー / cytoplasm to vacuole targeting by the Cvt pathway / pexophagy / nucleophagy ...regulation of phosphatidylinositol biosynthetic process / PAS complex / 1-phosphatidyl-1D-myo-inositol 3,5-bisphosphate metabolic process / phagophore / オートファジー / cytoplasm to vacuole targeting by the Cvt pathway / pexophagy / nucleophagy ...regulation of phosphatidylinositol biosynthetic process / PAS complex / 1-phosphatidyl-1D-myo-inositol 3,5-bisphosphate metabolic process / phagophore /  vacuolar protein processing / positive regulation of vacuole organization / vacuolar protein processing / positive regulation of vacuole organization /  オートファジー / cytoplasm to vacuole targeting by the Cvt pathway / pexophagy / nucleophagy / protein localization to phagophore assembly site / piecemeal microautophagy of the nucleus / phagophore assembly site membrane / late endosome to vacuole transport / オートファジー / cytoplasm to vacuole targeting by the Cvt pathway / pexophagy / nucleophagy / protein localization to phagophore assembly site / piecemeal microautophagy of the nucleus / phagophore assembly site membrane / late endosome to vacuole transport /  phosphatidylinositol-3-phosphate binding / phagophore assembly site / fungal-type vacuole membrane / phosphatidylinositol-4-phosphate binding / phosphatidylinositol-3,5-bisphosphate binding / vacuolar membrane / phosphatidylinositol-3-phosphate binding / phagophore assembly site / fungal-type vacuole membrane / phosphatidylinositol-4-phosphate binding / phosphatidylinositol-3,5-bisphosphate binding / vacuolar membrane /  extrinsic component of membrane / extrinsic component of membrane /  autophagosome assembly / autophagosome assembly /  ubiquitin binding / cell periphery / ubiquitin binding / cell periphery /  オートファジー / オートファジー /  protein transport / endosome membrane / protein transport / endosome membrane /  エンドソーム / protein-containing complex / エンドソーム / protein-containing complex /  細胞質基質 細胞質基質類似検索 - 分子機能 | |||||||||
| 生物種 |   Saccharomyces cerevisiae (パン酵母) Saccharomyces cerevisiae (パン酵母) | |||||||||
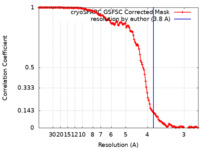
| 手法 | らせん対称体再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.8 Å クライオ電子顕微鏡法 / 解像度: 3.8 Å | |||||||||
 データ登録者 データ登録者 | Mann D / Fromm S / Martinez-Sanchez A / Gopaldass N / Mayer A / Sachse C | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: Atg18 oligomer organization in assembled tubes and on lipid membrane scaffolds. 著者: Daniel Mann / Simon A Fromm / Antonio Martinez-Sanchez / Navin Gopaldass / Ramona Choy / Andreas Mayer / Carsten Sachse /    要旨: Autophagy-related protein 18 (Atg18) participates in the elongation of early autophagosomal structures in concert with Atg2 and Atg9 complexes. How Atg18 contributes to the structural coordination of ...Autophagy-related protein 18 (Atg18) participates in the elongation of early autophagosomal structures in concert with Atg2 and Atg9 complexes. How Atg18 contributes to the structural coordination of Atg2 and Atg9 at the isolation membrane remains to be understood. Here, we determined the cryo-EM structures of Atg18 organized in helical tubes, Atg18 oligomers in solution as well as on lipid membrane scaffolds. The helical assembly is composed of Atg18 tetramers forming a lozenge cylindrical lattice with remarkable structural similarity to the COPII outer coat. When reconstituted with lipid membranes, using subtomogram averaging we determined tilted Atg18 dimer structures bridging two juxtaposed lipid membranes spaced apart by 80 Å. Moreover, lipid reconstitution experiments further delineate the contributions of Atg18's FRRG motif and the amphipathic helical extension in membrane interaction. The observed structural plasticity of Atg18's oligomeric organization and membrane binding properties provide a molecular framework for the positioning of downstream components of the autophagy machinery. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_15410.map.gz emd_15410.map.gz | 229.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-15410-v30.xml emd-15410-v30.xml emd-15410.xml emd-15410.xml | 15.5 KB 15.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_15410_fsc.xml emd_15410_fsc.xml | 13.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_15410.png emd_15410.png | 171 KB | ||
| マスクデータ |  emd_15410_msk_1.map emd_15410_msk_1.map | 244.1 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-15410.cif.gz emd-15410.cif.gz | 5.7 KB | ||
| その他 |  emd_15410_half_map_1.map.gz emd_15410_half_map_1.map.gz emd_15410_half_map_2.map.gz emd_15410_half_map_2.map.gz | 225.9 MB 225.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-15410 http://ftp.pdbj.org/pub/emdb/structures/EMD-15410 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15410 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15410 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_15410.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_15410.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | sharp map from CryoSPARC software | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.35 Å | ||||||||||||||||||||||||||||||||||||
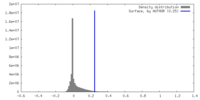
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_15410_msk_1.map emd_15410_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
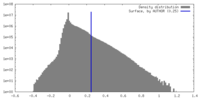
| 密度ヒストグラム |
-ハーフマップ: half map A
| ファイル | emd_15410_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map A | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
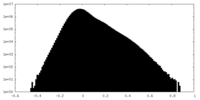
| 密度ヒストグラム |
-ハーフマップ: half map B
| ファイル | emd_15410_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map B | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Filament assembly of Atg18-WT
| 全体 | 名称: Filament assembly of Atg18-WT |
|---|---|
| 要素 |
|
-超分子 #1: Filament assembly of Atg18-WT
| 超分子 | 名称: Filament assembly of Atg18-WT / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:   Saccharomyces cerevisiae (パン酵母) Saccharomyces cerevisiae (パン酵母) |
-分子 #1: Autophagy-related protein 18
| 分子 | 名称: Autophagy-related protein 18 / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Saccharomyces cerevisiae (パン酵母) / 株: ATCC 204508 / S288c Saccharomyces cerevisiae (パン酵母) / 株: ATCC 204508 / S288c |
| 分子量 | 理論値: 55.15793 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 配列 | 文字列: MSDSSPTINF INFNQTGTCI SLGTSKGFKI FNCEPFGKFY SEDSGGYAIV EMLFSTSLLA LVGIGDQPAL SPRRLRIINT KKHSIICEV TFPTSILSVK MNKSRLVVLL QEQIYIYDIN TMRLLHTIET NPNPRGLMAM SPSVANSYLV YPSPPKVINS E IKAHATTN ...文字列: MSDSSPTINF INFNQTGTCI SLGTSKGFKI FNCEPFGKFY SEDSGGYAIV EMLFSTSLLA LVGIGDQPAL SPRRLRIINT KKHSIICEV TFPTSILSVK MNKSRLVVLL QEQIYIYDIN TMRLLHTIET NPNPRGLMAM SPSVANSYLV YPSPPKVINS E IKAHATTN NITLSVGGNT ETSFKRDQQD AGHSDISDLD QYSSFTKRDD ADPTSSNGGN SSIIKNGDVI VFNLETLQPT MV IEAHKGE IAAMAISFDG TLMATASDKG TIIRVFDIET GDKIYQFRRG TYATRIYSIS FSEDSQYLAV TGSSKTVHIF KLG HSMSNN KLDSDDSNME EAAADDSSLD TTSIDALSDE ENPTRLAREP YVDASRKTMG RMIRYSSQKL SRRAARTLGQ IFPI KVTSL LESSRHFASL KLPVETNSHV MTISSIGSPI DIDTSEYPEL FETGNSASTE SYHEPVMKMV PIRVVSSDGY LYNFV MDPE RGGDCLILSQ YSILMD UniProtKB: Autophagy-related protein 18 |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 7.2 |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 99 % / チャンバー内温度: 291 K / 装置: LEICA EM GP |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.0 µm Bright-field microscopy / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / 実像数: 1812 / 平均電子線量: 90.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
-原子モデル構築 1
| 詳細 | Initial PDB was derived from the Atg18-PR72AA filament structure, subunits were individually docked inside the density and the PR72AA loop was manually modified in Coot |
|---|---|
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: Correlation coefficient |
| 得られたモデル |  PDB-8afw: |
 ムービー
ムービー コントローラー
コントローラー








 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)