+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8j0o | ||||||
|---|---|---|---|---|---|---|---|
| タイトル | cryo-EM structure of human EMC and VDAC | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード |  MEMBRANE PROTEIN (膜タンパク質) / MEMBRANE PROTEIN (膜タンパク質) /  ER membrane protein complex (小胞体) ER membrane protein complex (小胞体) | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報negative regulation of calcium import into the mitochondrion / positive regulation of parkin-mediated stimulation of mitophagy in response to mitochondrial depolarization / inorganic cation transmembrane transporter activity /  extrinsic component of endoplasmic reticulum membrane / EMC complex / voltage-gated monoatomic anion channel activity / omegasome membrane / neuron-neuron synaptic transmission / protein insertion into ER membrane by stop-transfer membrane-anchor sequence / Mitochondrial calcium ion transport ...negative regulation of calcium import into the mitochondrion / positive regulation of parkin-mediated stimulation of mitophagy in response to mitochondrial depolarization / inorganic cation transmembrane transporter activity / extrinsic component of endoplasmic reticulum membrane / EMC complex / voltage-gated monoatomic anion channel activity / omegasome membrane / neuron-neuron synaptic transmission / protein insertion into ER membrane by stop-transfer membrane-anchor sequence / Mitochondrial calcium ion transport ...negative regulation of calcium import into the mitochondrion / positive regulation of parkin-mediated stimulation of mitophagy in response to mitochondrial depolarization / inorganic cation transmembrane transporter activity /  extrinsic component of endoplasmic reticulum membrane / EMC complex / voltage-gated monoatomic anion channel activity / omegasome membrane / neuron-neuron synaptic transmission / protein insertion into ER membrane by stop-transfer membrane-anchor sequence / Mitochondrial calcium ion transport / magnesium ion transport / cobalt ion transmembrane transporter activity / tail-anchored membrane protein insertion into ER membrane / Miscellaneous transport and binding events / extrinsic component of endoplasmic reticulum membrane / EMC complex / voltage-gated monoatomic anion channel activity / omegasome membrane / neuron-neuron synaptic transmission / protein insertion into ER membrane by stop-transfer membrane-anchor sequence / Mitochondrial calcium ion transport / magnesium ion transport / cobalt ion transmembrane transporter activity / tail-anchored membrane protein insertion into ER membrane / Miscellaneous transport and binding events /  ceramide binding / magnesium ion transmembrane transporter activity / ferrous iron transmembrane transporter activity / regulation of autophagy of mitochondrion / ceramide binding / magnesium ion transmembrane transporter activity / ferrous iron transmembrane transporter activity / regulation of autophagy of mitochondrion /  mitochondrial permeability transition pore complex / mitochondrial permeability transition pore complex /  ピルビン酸 / copper ion transport / ピルビン酸 / copper ion transport /  Mitochondrial protein import / Mitochondrial protein import /  phosphatidylcholine binding / phosphatidylcholine binding /  oxysterol binding / pyruvate metabolic process / monoatomic anion transport / oxysterol binding / pyruvate metabolic process / monoatomic anion transport /  cholesterol binding / cholesterol binding /  porin activity / mitochondrial nucleoid / pore complex / porin activity / mitochondrial nucleoid / pore complex /  autophagosome assembly / RHOA GTPase cycle / negative regulation of reactive oxygen species metabolic process / behavioral fear response / epithelial cell differentiation / PINK1-PRKN Mediated Mitophagy / positive regulation of endothelial cell proliferation / positive regulation of endothelial cell migration / autophagosome assembly / RHOA GTPase cycle / negative regulation of reactive oxygen species metabolic process / behavioral fear response / epithelial cell differentiation / PINK1-PRKN Mediated Mitophagy / positive regulation of endothelial cell proliferation / positive regulation of endothelial cell migration /  学習 / 学習 /  ミトコンドリア / positive regulation of angiogenesis / early endosome membrane / ミトコンドリア / positive regulation of angiogenesis / early endosome membrane /  carbohydrate binding / carbohydrate binding /  血管新生 / mitochondrial outer membrane / transmembrane transporter binding / 血管新生 / mitochondrial outer membrane / transmembrane transporter binding /  エンドソーム / Ub-specific processing proteases / エンドソーム / Ub-specific processing proteases /  脂質ラフト / 脂質ラフト /  ゴルジ体 / ゴルジ体 /  シナプス / apoptotic process / endoplasmic reticulum membrane / negative regulation of apoptotic process / シナプス / apoptotic process / endoplasmic reticulum membrane / negative regulation of apoptotic process /  protein kinase binding / protein kinase binding /  ゴルジ体 / ゴルジ体 /  小胞体 / protein-containing complex / 小胞体 / protein-containing complex /  ミトコンドリア / extracellular exosome / extracellular region / ミトコンドリア / extracellular exosome / extracellular region /  生体膜 / identical protein binding / 生体膜 / identical protein binding /  細胞核 / 細胞核 /  細胞膜 / 細胞膜 /  細胞質 細胞質類似検索 - 分子機能 | ||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.32 Å クライオ電子顕微鏡法 / 解像度: 3.32 Å | ||||||
 データ登録者 データ登録者 | Li, M. / Zhang, C. / Wu, J. / Lei, M. | ||||||
| 資金援助 |  中国, 1件 中国, 1件
| ||||||
 引用 引用 |  ジャーナル: Aging (Albany NY) / 年: 2024 ジャーナル: Aging (Albany NY) / 年: 2024タイトル: Structural insights into human EMC and its interaction with VDAC. 著者: Mingyue Li / Chunli Zhang / Yuntao Xu / Shaobai Li / Chenhui Huang / Jian Wu / Ming Lei /  要旨: The endoplasmic reticulum (ER) membrane protein complex (EMC) is a conserved, multi-subunit complex acting as an insertase at the ER membrane. Growing evidence shows that the EMC is also involved in ...The endoplasmic reticulum (ER) membrane protein complex (EMC) is a conserved, multi-subunit complex acting as an insertase at the ER membrane. Growing evidence shows that the EMC is also involved in stabilizing and trafficking membrane proteins. However, the structural basis and regulation of its multifunctionality remain elusive. Here, we report cryo-electron microscopy structures of human EMC in apo- and voltage-dependent anion channel (VDAC)-bound states at resolutions of 3.47 Å and 3.32 Å, respectively. We discovered a specific interaction between VDAC proteins and the EMC at mitochondria-ER contact sites, which is conserved from yeast to humans. Moreover, we identified a gating plug located inside the EMC hydrophilic vestibule, the substrate-binding pocket for client insertion. Conformation changes of this gating plug during the apo-to-VDAC-bound transition reveal that the EMC unlikely acts as an insertase in the VDAC1-bound state. Based on the data analysis, the gating plug may regulate EMC functions by modifying the hydrophilic vestibule in different states. Our discovery offers valuable insights into the structural basis of EMC's multifunctionality. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8j0o.cif.gz 8j0o.cif.gz | 533.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8j0o.ent.gz pdb8j0o.ent.gz | 427.6 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8j0o.json.gz 8j0o.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/j0/8j0o https://data.pdbj.org/pub/pdb/validation_reports/j0/8j0o ftp://data.pdbj.org/pub/pdb/validation_reports/j0/8j0o ftp://data.pdbj.org/pub/pdb/validation_reports/j0/8j0o | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ | 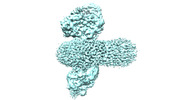 35907MC  8j0nC C: 同じ文献を引用 ( M: このデータのモデリングに利用したマップデータ |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-ER membrane protein complex subunit ... , 9種, 9分子 ABCDEFGHJ
| #1: タンパク質 |  小胞体 小胞体分子量: 111886.141 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q8N766 Homo sapiens (ヒト) / 参照: UniProt: Q8N766 |
|---|---|
| #2: タンパク質 |  小胞体 / Tetratricopeptide repeat protein 35 / TPR repeat protein 35 小胞体 / Tetratricopeptide repeat protein 35 / TPR repeat protein 35分子量: 34882.531 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q15006 Homo sapiens (ヒト) / 参照: UniProt: Q15006 |
| #3: タンパク質 |  小胞体 / Transmembrane protein 111 小胞体 / Transmembrane protein 111分子量: 29981.924 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q9P0I2 Homo sapiens (ヒト) / 参照: UniProt: Q9P0I2 |
| #4: タンパク質 |  小胞体 / Cell proliferation-inducing gene 17 protein / Transmembrane protein 85 小胞体 / Cell proliferation-inducing gene 17 protein / Transmembrane protein 85分子量: 20104.572 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q5J8M3 Homo sapiens (ヒト) / 参照: UniProt: Q5J8M3 |
| #5: タンパク質 |  小胞体 / Membrane magnesium transporter 1 / Transmembrane protein 32 小胞体 / Membrane magnesium transporter 1 / Transmembrane protein 32分子量: 14706.786 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q8N4V1 Homo sapiens (ヒト) / 参照: UniProt: Q8N4V1 |
| #6: タンパク質 |  小胞体 / Transmembrane protein 93 小胞体 / Transmembrane protein 93分子量: 12029.248 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q9BV81 Homo sapiens (ヒト) / 参照: UniProt: Q9BV81 |
| #7: タンパク質 |  小胞体 小胞体分子量: 26501.586 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q9NPA0 Homo sapiens (ヒト) / 参照: UniProt: Q9NPA0 |
| #8: タンパク質 |  小胞体 / Neighbor of COX4 / Protein FAM158B 小胞体 / Neighbor of COX4 / Protein FAM158B分子量: 23807.076 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: O43402 Homo sapiens (ヒト) / 参照: UniProt: O43402 |
| #9: タンパク質 |  小胞体 / Hematopoietic signal peptide-containing membrane domain-containing protein 1 小胞体 / Hematopoietic signal peptide-containing membrane domain-containing protein 1分子量: 21781.484 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: Q5UCC4 Homo sapiens (ヒト) / 参照: UniProt: Q5UCC4 |
-タンパク質 / 糖 , 2種, 4分子 K
| #10: タンパク質 | 分子量: 30807.521 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)   Homo sapiens (ヒト) / 参照: UniProt: P21796 Homo sapiens (ヒト) / 参照: UniProt: P21796 |
|---|---|
| #11: 多糖 |  オリゴ糖 / 分子量: 586.542 Da / 分子数: 3 / 由来タイプ: 組換発現 オリゴ糖 / 分子量: 586.542 Da / 分子数: 3 / 由来タイプ: 組換発現 |
-詳細
| 研究の焦点であるリガンドがあるか | N |
|---|
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: EMC_VDAC / タイプ: COMPLEX / Entity ID: #1-#10 / 由来: NATURAL |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 緩衝液 | pH: 7.5 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES |
急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 1200 nm Bright-field microscopy / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 1200 nm |
| 撮影 | 電子線照射量: 50 e/Å2 / フィルム・検出器のモデル: GATAN K3 (6k x 4k) |
- 解析
解析
| EMソフトウェア | 名称: PHENIX / バージョン: 1.20.1_4487: / カテゴリ: モデル精密化 | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||
3次元再構成 | 解像度: 3.32 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 455504 / 対称性のタイプ: POINT | ||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー




 PDBj
PDBj








