+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-9034 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | C-terminally truncated S. pombe Mdn1 (1-3911 aa) in the presence of AMPPNP (ring region) | |||||||||
 マップデータ マップデータ | C-terminally truncated S. pombe Mdn1 (1-3911 aa) in the presence of AMPPNP (ring region), primary map | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報preribosome, large subunit precursor / ribosomal large subunit export from nucleus / ribosomal large subunit biogenesis / ribosome biogenesis / calcium ion binding / nucleolus / ATP hydrolysis activity / nucleoplasm / ATP binding / nucleus 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
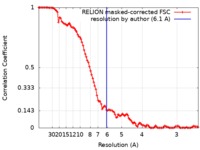
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 6.1 Å | |||||||||
 データ登録者 データ登録者 | Chen Z / Suzuki H / Wang AC / DiMaio F / Walz T / Kapoor TM | |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2018 ジャーナル: Cell / 年: 2018タイトル: Structural Insights into Mdn1, an Essential AAA Protein Required for Ribosome Biogenesis. 著者: Zhen Chen / Hiroshi Suzuki / Yuki Kobayashi / Ashley C Wang / Frank DiMaio / Shigehiro A Kawashima / Thomas Walz / Tarun M Kapoor /   要旨: Mdn1 is an essential AAA (ATPase associated with various activities) protein that removes assembly factors from distinct precursors of the ribosomal 60S subunit. However, Mdn1's large size (∼5,000 ...Mdn1 is an essential AAA (ATPase associated with various activities) protein that removes assembly factors from distinct precursors of the ribosomal 60S subunit. However, Mdn1's large size (∼5,000 amino acid [aa]) and its limited homology to other well-studied proteins have restricted our understanding of its remodeling function. Here, we present structures for S. pombe Mdn1 in the presence of AMPPNP at up to ∼4 Å or ATP plus Rbin-1, a chemical inhibitor, at ∼8 Å resolution. These data reveal that Mdn1's MIDAS domain is tethered to its ring-shaped AAA domain through an ∼20 nm long structured linker and a flexible ∼500 aa Asp/Glu-rich motif. We find that the MIDAS domain, which also binds other ribosome-assembly factors, docks onto the AAA ring in a nucleotide state-specific manner. Together, our findings reveal how conformational changes in the AAA ring can be directly transmitted to the MIDAS domain and thereby drive the targeted release of assembly factors from ribosomal 60S-subunit precursors. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_9034.map.gz emd_9034.map.gz | 6.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-9034-v30.xml emd-9034-v30.xml emd-9034.xml emd-9034.xml | 12.4 KB 12.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_9034_fsc.xml emd_9034_fsc.xml | 10.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_9034.png emd_9034.png | 87.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-9034 http://ftp.pdbj.org/pub/emdb/structures/EMD-9034 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9034 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9034 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_9034_validation.pdf.gz emd_9034_validation.pdf.gz | 78.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_9034_full_validation.pdf.gz emd_9034_full_validation.pdf.gz | 77.7 KB | 表示 | |
| XML形式データ |  emd_9034_validation.xml.gz emd_9034_validation.xml.gz | 493 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9034 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9034 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9034 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9034 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_9034.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_9034.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | C-terminally truncated S. pombe Mdn1 (1-3911 aa) in the presence of AMPPNP (ring region), primary map | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.3 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : N-terminal density map of the C-terminally truncated Mdn1 in the ...
| 全体 | 名称: N-terminal density map of the C-terminally truncated Mdn1 in the presence of AMPPNP |
|---|---|
| 要素 |
|
-超分子 #1: N-terminal density map of the C-terminally truncated Mdn1 in the ...
| 超分子 | 名称: N-terminal density map of the C-terminally truncated Mdn1 in the presence of AMPPNP タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 450 KDa |
| 組換発現 | 生物種:  Trichoplusia ni (イラクサキンウワバ) Trichoplusia ni (イラクサキンウワバ) |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.15 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - 画像ごとのフレーム数: 1-50 / 実像数: 2745 / 平均露光時間: 15.0 sec. / 平均電子線量: 88.8 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.4 µm / 倍率(公称値): 22500 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー