+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8076 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | The structure of microsomal glutathione transferase 1 | |||||||||
 マップデータ マップデータ | None | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cellular response to lipid hydroperoxide / Aflatoxin activation and detoxification / glutathione transport /  薬物代謝 / 薬物代謝 /  glutathione binding / Leydig cell differentiation / glutathione binding / Leydig cell differentiation /  glutathione peroxidase activity / peroxisomal membrane / Neutrophil degranulation / glutathione peroxidase activity / peroxisomal membrane / Neutrophil degranulation /  グルタチオン-S-トランスフェラーゼ ...cellular response to lipid hydroperoxide / Aflatoxin activation and detoxification / glutathione transport / グルタチオン-S-トランスフェラーゼ ...cellular response to lipid hydroperoxide / Aflatoxin activation and detoxification / glutathione transport /  薬物代謝 / 薬物代謝 /  glutathione binding / Leydig cell differentiation / glutathione binding / Leydig cell differentiation /  glutathione peroxidase activity / peroxisomal membrane / Neutrophil degranulation / glutathione peroxidase activity / peroxisomal membrane / Neutrophil degranulation /  グルタチオン-S-トランスフェラーゼ / グルタチオン-S-トランスフェラーゼ /  glutathione transferase activity / glutathione metabolic process / response to organonitrogen compound / apical part of cell / mitochondrial outer membrane / response to lipopolysaccharide / response to xenobiotic stimulus / endoplasmic reticulum membrane / glutathione transferase activity / glutathione metabolic process / response to organonitrogen compound / apical part of cell / mitochondrial outer membrane / response to lipopolysaccharide / response to xenobiotic stimulus / endoplasmic reticulum membrane /  小胞体 / 小胞体 /  ミトコンドリア / ミトコンドリア /  生体膜 / identical protein binding 生体膜 / identical protein binding類似検索 - 分子機能 | |||||||||
| 生物種 |   Rattus norvegicus (ドブネズミ) Rattus norvegicus (ドブネズミ) | |||||||||
| 手法 |  電子線結晶学 / 電子線結晶学 /  クライオ電子顕微鏡法 / 解像度: 3.5 Å クライオ電子顕微鏡法 / 解像度: 3.5 Å | |||||||||
 データ登録者 データ登録者 | Kuang Q / Purhonen P / Jegerschold C / Morgenstern R / Hebert H | |||||||||
 引用 引用 |  ジャーナル: Sci Rep / 年: 2017 ジャーナル: Sci Rep / 年: 2017タイトル: Dead-end complex, lipid interactions and catalytic mechanism of microsomal glutathione transferase 1, an electron crystallography and mutagenesis investigation. 著者: Qie Kuang / Pasi Purhonen / Johan Ålander / Richard Svensson / Veronika Hoogland / Jens Winerdal / Linda Spahiu / Astrid Ottosson-Wadlund / Caroline Jegerschöld / Ralf Morgenstern / Hans Hebert /  要旨: Microsomal glutathione transferase 1 (MGST1) is a detoxification enzyme belonging to the Membrane Associated Proteins in Eicosanoid and Glutathione Metabolism (MAPEG) superfamily. Here we have used ...Microsomal glutathione transferase 1 (MGST1) is a detoxification enzyme belonging to the Membrane Associated Proteins in Eicosanoid and Glutathione Metabolism (MAPEG) superfamily. Here we have used electron crystallography of two-dimensional crystals in order to determine an atomic model of rat MGST1 in a lipid environment. The model comprises 123 of the 155 amino acid residues, two structured phospholipid molecules, two aliphatic chains and one glutathione (GSH) molecule. The functional unit is a homotrimer centered on the crystallographic three-fold axes of the unit cell. The GSH substrate binds in an extended conformation at the interface between two subunits of the trimer supported by new in vitro mutagenesis data. Mutation of Arginine 130 to alanine resulted in complete loss of activity consistent with a role for Arginine 130 in stabilizing the strongly nucleophilic GSH thiolate required for catalysis. Based on the new model and an electron diffraction data set from crystals soaked with trinitrobenzene, that forms a dead-end Meisenheimer complex with GSH, a difference map was calculated. The map reveals side chain movements opening a cavity that defines the second substrate site. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8076.map.gz emd_8076.map.gz | 1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8076-v30.xml emd-8076-v30.xml emd-8076.xml emd-8076.xml | 11.9 KB 11.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_8076.png emd_8076.png | 119.5 KB | ||
| Filedesc structureFactors |  emd_8076_sf.cif.gz emd_8076_sf.cif.gz | 98.8 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8076 http://ftp.pdbj.org/pub/emdb/structures/EMD-8076 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8076 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8076 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  5i9kMC  8084C  5ia9C M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8076.map.gz / 形式: CCP4 / 大きさ: 1.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8076.map.gz / 形式: CCP4 / 大きさ: 1.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | None | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X: 1.1361 Å / Y: 1.1361 Å / Z: 1.1905 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 168 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Complex between microsomal glutathione transferase 1 and glutathione
| 全体 | 名称: Complex between microsomal glutathione transferase 1 and glutathione |
|---|---|
| 要素 |
|
-超分子 #1: Complex between microsomal glutathione transferase 1 and glutathione
| 超分子 | 名称: Complex between microsomal glutathione transferase 1 and glutathione タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Rattus norvegicus (ドブネズミ) Rattus norvegicus (ドブネズミ) |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) / 組換プラスミド: pSP19T7LT Escherichia coli (大腸菌) / 組換プラスミド: pSP19T7LT |
| 分子量 | 理論値: 52940 MDa |
-分子 #1: Microsomal glutathione S-transferase 1
| 分子 | 名称: Microsomal glutathione S-transferase 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO / EC番号:  グルタチオン-S-トランスフェラーゼ グルタチオン-S-トランスフェラーゼ |
|---|---|
| 由来(天然) | 生物種:   Rattus norvegicus (ドブネズミ) Rattus norvegicus (ドブネズミ) |
| 分子量 | 理論値: 17.492488 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 配列 | 文字列: MADLKQLMDN EVLMAFTSYA TIILAKMMFL SSATAFQRLT NKVFANPEDC AGFGKGENAK KFLRTDEKVE RVRRAHLNDL ENIVPFLGI GLLYSLSGPD LSTALIHFRI FVGARIYHTI AYLTPLPQPN RGLAFFVGYG VTLSMAYRLL RSRLYL |
-分子 #2: GLUTATHIONE
| 分子 | 名称: GLUTATHIONE / タイプ: ligand / ID: 2 / コピー数: 1 / 式: GSH |
|---|---|
| 分子量 | 理論値: 307.323 Da |
| Chemical component information | 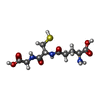 ChemComp-GSH: |
-分子 #3: 1,2-DIACYL-SN-GLYCERO-3-PHOSPHOCHOLINE
| 分子 | 名称: 1,2-DIACYL-SN-GLYCERO-3-PHOSPHOCHOLINE / タイプ: ligand / ID: 3 / コピー数: 2 / 式: PC1 |
|---|---|
| 分子量 | 理論値: 790.145 Da |
| Chemical component information | 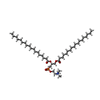 ChemComp-PC1: |
-分子 #4: PALMITIC ACID
| 分子 | 名称: PALMITIC ACID / タイプ: ligand / ID: 4 / コピー数: 2 / 式: PLM |
|---|---|
| 分子量 | 理論値: 256.424 Da |
| Chemical component information |  ChemComp-PLM: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  電子線結晶学 電子線結晶学 |
| 試料の集合状態 | 2D array |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 糖包埋 | 材質: trehalose |
| 凍結 | 凍結剤: NITROGEN |
| 結晶化 | 脂質・タンパク質比: 3 / 脂質混合液: bovine liver lecithin / 温度: 293.0 K / 時間: 7.0 DAY / 詳細: Dialysis of protein solubulized in Triton X-100 |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL 2100F |
|---|---|
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: DIFFRACTION 回折 / カメラ長: 200 mm 回折 / カメラ長: 200 mm |
| 撮影 | フィルム・検出器のモデル: TVIPS TEMCAM-F415 (4k x 4k) 回折像の数: 225 / 平均電子線量: 1.0 e/Å2 |
- 画像解析
画像解析
| 結晶パラメータ | 単位格子 - A: 81.8 Å / 単位格子 - B: 81.8 Å / 単位格子 - C: 100.0 Å / 単位格子 - γ: 120.0 ° / 面群: P 6 |
|---|---|
| Crystallography statistics | Number intensities measured: 97987 / Number structure factors: 6314 / Fourier space coverage: 82.5 / R sym: 0.126 / R merge: 0.396 / Overall phase error: 1.0E-5 / Overall phase residual: 1.0E-5 / Phase error rejection criteria: 0 / High resolution: 3.5 Å |
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 3.5 Å / 解像度の算出法: DIFFRACTION PATTERN/LAYERLINES |
 ムービー
ムービー コントローラー
コントローラー