+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 9g81 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
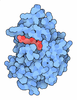
| タイトル | CTX-M-14 mixed with piperacillin at 3s delay time - serial crystallography temperature series; 30C, 303K | |||||||||||||||
 要素 要素 | Beta-lactamase | |||||||||||||||
 キーワード キーワード | HYDROLASE / catalytic activity / beta-lactamase activity / hydrolase activity | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報beta-lactam antibiotic catabolic process / beta-lactamase activity / beta-lactamase / response to antibiotic 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  Klebsiella pneumoniae (肺炎桿菌) Klebsiella pneumoniae (肺炎桿菌) | |||||||||||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 1.71 Å 分子置換 / 解像度: 1.71 Å | |||||||||||||||
 データ登録者 データ登録者 | Prester, A. / von Stetten, D. / Mehrabi, P. / Schulz, E.C. | |||||||||||||||
| 資金援助 |  ドイツ, European Union, 4件 ドイツ, European Union, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2025 ジャーナル: Nat Commun / 年: 2025タイトル: Probing the modulation of enzyme kinetics by multi-temperature, time-resolved serial crystallography. 著者: Schulz, E.C. / Prester, A. / von Stetten, D. / Gore, G. / Hatton, C.E. / Bartels, K. / Leimkohl, J.P. / Schikora, H. / Ginn, H.M. / Tellkamp, F. / Mehrabi, P. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  9g81.cif.gz 9g81.cif.gz | 156.1 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb9g81.ent.gz pdb9g81.ent.gz | 101.3 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  9g81.json.gz 9g81.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  9g81_validation.pdf.gz 9g81_validation.pdf.gz | 1.2 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  9g81_full_validation.pdf.gz 9g81_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  9g81_validation.xml.gz 9g81_validation.xml.gz | 17 KB | 表示 | |
| CIF形式データ |  9g81_validation.cif.gz 9g81_validation.cif.gz | 23.4 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/g8/9g81 https://data.pdbj.org/pub/pdb/validation_reports/g8/9g81 ftp://data.pdbj.org/pub/pdb/validation_reports/g8/9g81 ftp://data.pdbj.org/pub/pdb/validation_reports/g8/9g81 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  9g5sC  9g5wC  9g5xC  9g61C  9g6lC  9g6mC  9g6nC  9g6oC  9g6pC  9g7vC  9g7wC  9g7xC  9g7yC  9g7zC  9g80C  9g82C  9i7lC C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 31009.291 Da / 分子数: 1 / 由来タイプ: 組換発現 / 詳細: Residue 1- 27 signal peptide / 由来: (組換発現)  Klebsiella pneumoniae (肺炎桿菌) / 遺伝子: blaCTX-M-14, bla_2, SAMEA3512100_05103 / 発現宿主: Klebsiella pneumoniae (肺炎桿菌) / 遺伝子: blaCTX-M-14, bla_2, SAMEA3512100_05103 / 発現宿主:  |
|---|---|
| #2: 化合物 | ChemComp-WPP / |
| #3: 化合物 | ChemComp-YPP / |
| #4: 化合物 | ChemComp-SO4 / |
| #5: 水 | ChemComp-HOH / |
| 研究の焦点であるリガンドがあるか | Y |
| Has protein modification | N |
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.17 Å3/Da / 溶媒含有率: 43.35 % |
|---|---|
| 結晶化 | 温度: 293 K / 手法: batch mode / pH: 4.5 詳細: CTX-M-14 solution (22 mg/ml) was mixed with 45% precipitant solution (40% PEG8000, 200mM lithium sulfate, 100mM sodium acetate, pH 4.5) and with 5% undiluted seed stock in batch crystallization setups |
-データ収集
| 回折 | 平均測定温度: 303 K / Ambient temp details: environmental control box / Serial crystal experiment: Y |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  PETRA III, EMBL c/o DESY PETRA III, EMBL c/o DESY  / ビームライン: P14 (MX2) / 波長: 0.976 Å / ビームライン: P14 (MX2) / 波長: 0.976 Å |
| 検出器 | タイプ: DECTRIS EIGER X 4M / 検出器: PIXEL / 日付: 2022年6月21日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 0.976 Å / 相対比: 1 |
| 反射 | 解像度: 1.7→78.07 Å / Num. obs: 27982 / % possible obs: 100 % / 冗長度: 131.2 % / Biso Wilson estimate: 22.25 Å2 / CC1/2: 0.952 / CC star: 0.988 / Net I/σ(I): 4.46 |
| 反射 シェル | 解像度: 1.7→1.76 Å / Mean I/σ(I) obs: 1.04 / Num. unique obs: 2662 / CC1/2: 0.446 / CC star: 0.786 |
| Serial crystallography sample delivery | 手法: fixed target |
| Serial crystallography sample delivery fixed target | Sample holding: Hare-Chip , silicon |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 / 解像度: 1.71→78.07 Å / SU ML: 0.2149 / 交差検証法: FREE R-VALUE / σ(F): 1.34 / 位相誤差: 21.4306 分子置換 / 解像度: 1.71→78.07 Å / SU ML: 0.2149 / 交差検証法: FREE R-VALUE / σ(F): 1.34 / 位相誤差: 21.4306 立体化学のターゲット値: GeoStd + Monomer Library + CDL v1.2
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 減衰半径: 0.9 Å / VDWプローブ半径: 1.1 Å / 溶媒モデル: FLAT BULK SOLVENT MODEL | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 29.28 Å2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 1.71→78.07 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLS | 手法: refined / Origin x: -4.6330173106 Å / Origin y: 1.22059883285 Å / Origin z: 19.7835380174 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLSグループ | Selection details: all |
 ムービー
ムービー コントローラー
コントローラー



 PDBj
PDBj