+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8ufa | ||||||
|---|---|---|---|---|---|---|---|
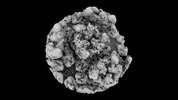
| タイトル | Eastern equine encephalitis virus (PE-6) VLP (asymmetric unit) | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | VIRAL PROTEIN / virus / Structural Genomics / Center for Structural Biology of Infectious Diseases / CSBID | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報T=4 icosahedral viral capsid / host cell cytoplasm / symbiont entry into host cell / serine-type endopeptidase activity / fusion of virus membrane with host endosome membrane / virion attachment to host cell / host cell plasma membrane / structural molecule activity / virion membrane / proteolysis ...T=4 icosahedral viral capsid / host cell cytoplasm / symbiont entry into host cell / serine-type endopeptidase activity / fusion of virus membrane with host endosome membrane / virion attachment to host cell / host cell plasma membrane / structural molecule activity / virion membrane / proteolysis / plasma membrane / cytoplasm 類似検索 - 分子機能 | ||||||
| 生物種 |   Eastern equine encephalitis virus (東部ウマ脳炎ウイルス) Eastern equine encephalitis virus (東部ウマ脳炎ウイルス) | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.86 Å | ||||||
 データ登録者 データ登録者 | Adams, L.J. / Fremont, D.H. / Center for Structural Biology of Infectious Diseases (CSBID) | ||||||
| 資金援助 |  米国, 1件 米国, 1件
| ||||||
 引用 引用 |  ジャーナル: Cell / 年: 2024 ジャーナル: Cell / 年: 2024タイトル: Structural and functional basis of VLDLR usage by Eastern equine encephalitis virus. 著者: Lucas J Adams / Saravanan Raju / Hongming Ma / Theron Gilliland / Douglas S Reed / William B Klimstra / Daved H Fremont / Michael S Diamond /  要旨: The very-low-density lipoprotein receptor (VLDLR) comprises eight LDLR type A (LA) domains and supports entry of distantly related alphaviruses, including Eastern equine encephalitis virus (EEEV) and ...The very-low-density lipoprotein receptor (VLDLR) comprises eight LDLR type A (LA) domains and supports entry of distantly related alphaviruses, including Eastern equine encephalitis virus (EEEV) and Semliki Forest virus (SFV). Here, by resolving multiple cryo-electron microscopy structures of EEEV-VLDLR complexes and performing mutagenesis and functional studies, we show that EEEV uses multiple sites (E1/E2 cleft and E2 A domain) to engage more than one LA domain simultaneously. However, no single LA domain is necessary or sufficient to support efficient EEEV infection. Whereas all EEEV strains show conservation of two VLDLR-binding sites, the EEEV PE-6 strain and a few other EEE complex members feature a single amino acid substitution that enables binding of LA domains to an additional site on the E2 B domain. These structural and functional analyses informed the design of a minimal VLDLR decoy receptor that neutralizes EEEV infection and protects mice from lethal challenge. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8ufa.cif.gz 8ufa.cif.gz | 666.4 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8ufa.ent.gz pdb8ufa.ent.gz | 531.5 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8ufa.json.gz 8ufa.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  8ufa_validation.pdf.gz 8ufa_validation.pdf.gz | 1.4 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  8ufa_full_validation.pdf.gz 8ufa_full_validation.pdf.gz | 1.5 MB | 表示 | |
| XML形式データ |  8ufa_validation.xml.gz 8ufa_validation.xml.gz | 103.1 KB | 表示 | |
| CIF形式データ |  8ufa_validation.cif.gz 8ufa_validation.cif.gz | 160.9 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/uf/8ufa https://data.pdbj.org/pub/pdb/validation_reports/uf/8ufa ftp://data.pdbj.org/pub/pdb/validation_reports/uf/8ufa ftp://data.pdbj.org/pub/pdb/validation_reports/uf/8ufa | HTTPS FTP |
-関連構造データ
| 関連構造データ |  42188MC  8ufbC  8ufcC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 47935.180 Da / 分子数: 4 / 断片: UNP residues 802-1242 / 由来タイプ: 組換発現 由来: (組換発現)   Eastern equine encephalitis virus (東部ウマ脳炎ウイルス) Eastern equine encephalitis virus (東部ウマ脳炎ウイルス)株: PE-6 / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: Q88678 Homo sapiens (ヒト) / 参照: UniProt: Q88678#2: タンパク質 | 分子量: 46378.191 Da / 分子数: 4 / 断片: UNP residues 325-738 / 由来タイプ: 組換発現 由来: (組換発現)   Eastern equine encephalitis virus (東部ウマ脳炎ウイルス) Eastern equine encephalitis virus (東部ウマ脳炎ウイルス)株: PE-6 / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: Q88678 Homo sapiens (ヒト) / 参照: UniProt: Q88678#3: タンパク質 | 分子量: 16540.656 Da / 分子数: 4 / 断片: UNP residues 111-261 / 由来タイプ: 組換発現 由来: (組換発現)   Eastern equine encephalitis virus (東部ウマ脳炎ウイルス) Eastern equine encephalitis virus (東部ウマ脳炎ウイルス)株: PE-6 / 遺伝子: SP / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: W8S146 Homo sapiens (ヒト) / 参照: UniProt: W8S146#4: 糖 | ChemComp-NAG / 研究の焦点であるリガンドがあるか | N | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Eastern equine encephalitis virus / タイプ: VIRUS / Entity ID: #1-#3 / 由来: RECOMBINANT |
|---|---|
| 由来(天然) | 生物種:   Eastern equine encephalitis virus (東部ウマ脳炎ウイルス) Eastern equine encephalitis virus (東部ウマ脳炎ウイルス)株: PE-6 |
| 由来(組換発現) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| ウイルスについての詳細 | 中空か: YES / エンベロープを持つか: YES / 単離: STRAIN / タイプ: VIRUS-LIKE PARTICLE |
| 緩衝液 | pH: 7.4 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2200 nm / 最小 デフォーカス(公称値): 700 nm |
| 撮影 | 電子線照射量: 37.93 e/Å2 フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) |
- 解析
解析
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 3次元再構成 | 解像度: 2.86 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 1038056 / 対称性のタイプ: POINT | ||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj




