| 登録情報 | データベース: PDB / ID: 6jju
|
|---|
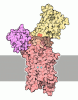
| タイトル | Structure of Ca2+ ATPase |
|---|
 要素 要素 | Sarcoplasmic/endoplasmic reticulum calcium ATPase 2 |
|---|
 キーワード キーワード | HYDROLASE / p-type atpase / calcium transport / endoplasmic reticulum |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
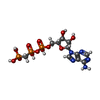
longitudinal sarcoplasmic reticulum / ER-nucleus signaling pathway / positive regulation of endoplasmic reticulum calcium ion concentration / P-type calcium transporter activity involved in regulation of cardiac muscle cell membrane potential / calcium ion transport from cytosol to endoplasmic reticulum / regulation of calcium ion-dependent exocytosis of neurotransmitter / calcium ion-transporting ATPase complex / T-tubule organization / regulation of cardiac muscle cell action potential involved in regulation of contraction / regulation of cardiac muscle cell membrane potential ...longitudinal sarcoplasmic reticulum / ER-nucleus signaling pathway / positive regulation of endoplasmic reticulum calcium ion concentration / P-type calcium transporter activity involved in regulation of cardiac muscle cell membrane potential / calcium ion transport from cytosol to endoplasmic reticulum / regulation of calcium ion-dependent exocytosis of neurotransmitter / calcium ion-transporting ATPase complex / T-tubule organization / regulation of cardiac muscle cell action potential involved in regulation of contraction / regulation of cardiac muscle cell membrane potential / sarcoplasmic reticulum calcium ion transport / platelet dense tubular network membrane / calcium ion import into sarcoplasmic reticulum / Pre-NOTCH Processing in Golgi / negative regulation of heart contraction / ribbon synapse / P-type Ca2+ transporter / P-type calcium transporter activity / regulation of the force of heart contraction / transition between fast and slow fiber / endoplasmic reticulum calcium ion homeostasis / cardiac muscle hypertrophy in response to stress / S100 protein binding / relaxation of cardiac muscle / regulation of cardiac muscle contraction by calcium ion signaling / Reduction of cytosolic Ca++ levels / organelle localization by membrane tethering / mitochondrion-endoplasmic reticulum membrane tethering / autophagosome membrane docking / lncRNA binding / Ion transport by P-type ATPases / autophagosome assembly / epidermis development / regulation of cardiac conduction / positive regulation of heart rate / positive regulation of cardiac muscle cell apoptotic process / Ion homeostasis / sarcoplasmic reticulum membrane / response to endoplasmic reticulum stress / sarcoplasmic reticulum / calcium channel regulator activity / neuron cellular homeostasis / calcium ion transmembrane transport / intracellular calcium ion homeostasis / cellular response to oxidative stress / monoatomic ion transmembrane transport / transmembrane transporter binding / cell adhesion / calcium ion binding / endoplasmic reticulum membrane / enzyme binding / endoplasmic reticulum / ATP hydrolysis activity / ATP binding / membrane / plasma membrane類似検索 - 分子機能 P-type ATPase, subfamily IIA, SERCA-type / haloacid dehalogenase-like hydrolase / Cation-transporting P-type ATPase, C-terminal / Cation transporting ATPase, C-terminus / Cation transporter/ATPase, N-terminus / Cation-transporting P-type ATPase, N-terminal / Cation transporter/ATPase, N-terminus / Cation transport ATPase (P-type) / E1-E2 ATPase / P-type ATPase, haloacid dehalogenase domain ...P-type ATPase, subfamily IIA, SERCA-type / haloacid dehalogenase-like hydrolase / Cation-transporting P-type ATPase, C-terminal / Cation transporting ATPase, C-terminus / Cation transporter/ATPase, N-terminus / Cation-transporting P-type ATPase, N-terminal / Cation transporter/ATPase, N-terminus / Cation transport ATPase (P-type) / E1-E2 ATPase / P-type ATPase, haloacid dehalogenase domain / P-type ATPase, phosphorylation site / P-type ATPase, cytoplasmic domain N / E1-E2 ATPases phosphorylation site. / P-type ATPase, A domain superfamily / P-type ATPase / P-type ATPase, transmembrane domain superfamily / haloacid dehalogenase-like hydrolase / HAD superfamily / HAD-like superfamily類似検索 - ドメイン・相同性 PHOSPHOMETHYLPHOSPHONIC ACID ADENYLATE ESTER / Sarcoplasmic/endoplasmic reticulum calcium ATPase 2類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 3.2 Å 分子置換 / 解像度: 3.2 Å |
|---|
 データ登録者 データ登録者 | Inoue, M. / Sakuta, N. / Watanabe, S. / Inaba, K. |
|---|
| 資金援助 |  日本, 1件 日本, 1件 | 組織 | 認可番号 | 国 |
|---|
| Japan Science and Technology | JPMJCR13M6 |  日本 日本 |
|
|---|
 引用 引用 |  ジャーナル: Cell Rep / 年: 2019 ジャーナル: Cell Rep / 年: 2019
タイトル: Structural Basis of Sarco/Endoplasmic Reticulum Ca2+-ATPase 2b Regulation via Transmembrane Helix Interplay.
著者: Inoue, M. / Sakuta, N. / Watanabe, S. / Zhang, Y. / Yoshikaie, K. / Tanaka, Y. / Ushioda, R. / Kato, Y. / Takagi, J. / Tsukazaki, T. / Nagata, K. / Inaba, K. |
|---|
| 履歴 | | 登録 | 2019年2月27日 | 登録サイト: PDBJ / 処理サイト: PDBJ |
|---|
| 改定 1.0 | 2019年5月22日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2023年11月22日 | Group: Data collection / Database references ...Data collection / Database references / Derived calculations / Refinement description
カテゴリ: chem_comp_atom / chem_comp_bond ...chem_comp_atom / chem_comp_bond / database_2 / pdbx_initial_refinement_model / struct_conn
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession ..._database_2.pdbx_DOI / _database_2.pdbx_database_accession / _struct_conn.pdbx_dist_value / _struct_conn.ptnr1_label_atom_id / _struct_conn.ptnr2_auth_seq_id / _struct_conn.ptnr2_label_asym_id |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  分子置換 / 解像度: 3.2 Å
分子置換 / 解像度: 3.2 Å  データ登録者
データ登録者 日本, 1件
日本, 1件  引用
引用 ジャーナル: Cell Rep / 年: 2019
ジャーナル: Cell Rep / 年: 2019 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 6jju.cif.gz
6jju.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb6jju.ent.gz
pdb6jju.ent.gz PDB形式
PDB形式 6jju.json.gz
6jju.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 6jju_validation.pdf.gz
6jju_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 6jju_full_validation.pdf.gz
6jju_full_validation.pdf.gz 6jju_validation.xml.gz
6jju_validation.xml.gz 6jju_validation.cif.gz
6jju_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/jj/6jju
https://data.pdbj.org/pub/pdb/validation_reports/jj/6jju ftp://data.pdbj.org/pub/pdb/validation_reports/jj/6jju
ftp://data.pdbj.org/pub/pdb/validation_reports/jj/6jju リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト) / 遺伝子: ATP2A2, ATP2B / 細胞株 (発現宿主): HEK293T / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: ATP2A2, ATP2B / 細胞株 (発現宿主): HEK293T / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: P16615, P-type Ca2+ transporter
Homo sapiens (ヒト) / 参照: UniProt: P16615, P-type Ca2+ transporter X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  SPring-8
SPring-8  / ビームライン: BL32XU / 波長: 1 Å
/ ビームライン: BL32XU / 波長: 1 Å 解析
解析 分子置換
分子置換 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj