+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 5vv1 | ||||||
|---|---|---|---|---|---|---|---|
| タイトル | Structure of human neuronal nitric oxide synthase heme domain in complex with 7-(((3-(4-Methoxypyridin-3-yl)propyl)amino)methyl)quinolin-2-amine | ||||||
 要素 要素 | Nitric oxide synthase, brain | ||||||
 キーワード キーワード | Oxidoreductase/Inhibitor / nitric oxide synthase / inhibitor complex / heme enzyme / Oxidoreductase-Inhibitor complex | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報positive regulation of membrane repolarization during ventricular cardiac muscle cell action potential / negative regulation of calcium ion transport into cytosol / Nitric oxide stimulates guanylate cyclase / myoblast fusion / ROS and RNS production in phagocytes / tetrahydrobiopterin binding / arginine binding / regulation of cardiac muscle contraction by calcium ion signaling / regulation of calcium ion transmembrane transport via high voltage-gated calcium channel / positive regulation of adenylate cyclase-activating G protein-coupled receptor signaling pathway ...positive regulation of membrane repolarization during ventricular cardiac muscle cell action potential / negative regulation of calcium ion transport into cytosol / Nitric oxide stimulates guanylate cyclase / myoblast fusion / ROS and RNS production in phagocytes / tetrahydrobiopterin binding / arginine binding / regulation of cardiac muscle contraction by calcium ion signaling / regulation of calcium ion transmembrane transport via high voltage-gated calcium channel / positive regulation of adenylate cyclase-activating G protein-coupled receptor signaling pathway / positive regulation of sodium ion transmembrane transport / peptidyl-cysteine S-nitrosylase activity / cadmium ion binding / positive regulation of the force of heart contraction / negative regulation of potassium ion transport / negative regulation of calcium ion transport / nitric oxide mediated signal transduction / nitric-oxide synthase (NADPH) / sodium channel regulator activity / negative regulation of serotonin uptake / regulation of cardiac muscle contraction / nitric-oxide synthase activity / multicellular organismal response to stress / xenobiotic catabolic process / L-arginine catabolic process / striated muscle contraction / regulation of sodium ion transport / Ion homeostasis / negative regulation of blood pressure / response to hormone / photoreceptor inner segment / calcium channel regulator activity / nitric oxide biosynthetic process / cell redox homeostasis / sarcoplasmic reticulum / cell periphery / sarcolemma / cellular response to growth factor stimulus / calcium-dependent protein binding / vasodilation / positive regulation of neuron apoptotic process / FMN binding / flavin adenine dinucleotide binding / NADP binding / response to heat / scaffold protein binding / dendritic spine / response to lipopolysaccharide / transmembrane transporter binding / cytoskeleton / response to hypoxia / calmodulin binding / postsynaptic density / membrane raft / synapse / heme binding / positive regulation of DNA-templated transcription / perinuclear region of cytoplasm / positive regulation of transcription by RNA polymerase II / protein-containing complex / mitochondrion / nucleoplasm / nucleus / plasma membrane / cytosol / cytoplasm 類似検索 - 分子機能 | ||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  フーリエ合成 / 解像度: 1.95 Å フーリエ合成 / 解像度: 1.95 Å | ||||||
 データ登録者 データ登録者 | Huiying, L. / Thomas, L.P. | ||||||
| 資金援助 |  米国, 1件 米国, 1件
| ||||||
 引用 引用 |  ジャーナル: J. Med. Chem. / 年: 2017 ジャーナル: J. Med. Chem. / 年: 2017タイトル: Hydrophilic, Potent, and Selective 7-Substituted 2-Aminoquinolines as Improved Human Neuronal Nitric Oxide Synthase Inhibitors. 著者: Pensa, A.V. / Cinelli, M.A. / Li, H. / Chreifi, G. / Mukherjee, P. / Roman, L.J. / Martasek, P. / Poulos, T.L. / Silverman, R.B. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  5vv1.cif.gz 5vv1.cif.gz | 363.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb5vv1.ent.gz pdb5vv1.ent.gz | 294.8 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  5vv1.json.gz 5vv1.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  5vv1_validation.pdf.gz 5vv1_validation.pdf.gz | 1.6 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  5vv1_full_validation.pdf.gz 5vv1_full_validation.pdf.gz | 1.6 MB | 表示 | |
| XML形式データ |  5vv1_validation.xml.gz 5vv1_validation.xml.gz | 37.4 KB | 表示 | |
| CIF形式データ |  5vv1_validation.cif.gz 5vv1_validation.cif.gz | 53.8 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/vv/5vv1 https://data.pdbj.org/pub/pdb/validation_reports/vv/5vv1 ftp://data.pdbj.org/pub/pdb/validation_reports/vv/5vv1 ftp://data.pdbj.org/pub/pdb/validation_reports/vv/5vv1 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  5vuiC  5vujC  5vukC  5vulC  5vumC  5vunC  5vuoC  5vupC  5vuqC  5vurC  5vusC  5vutC  5vuuC  5vuvC  5vuwC  5vuxC  5vuyC  5vuzC  5vv0C  5vv2C  5vv3C  5vv4C  5vv5C  5vv6C  5vv7C  5vv8C  5vv9C  5vvaC  5vvbC  5vvcC  5vvdC  5vvgC  5vvnC  4uh5S C: 同じ文献を引用 ( S: 精密化の開始モデル |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
|
- 要素
要素
-タンパク質 , 1種, 2分子 AB
| #1: タンパク質 | 分子量: 48784.496 Da / 分子数: 2 / 断片: UNP residues 302-722 / 変異: R354A, G357D / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: NOS1 / 器官: brain / プラスミド: pCWori / 発現宿主: Homo sapiens (ヒト) / 遺伝子: NOS1 / 器官: brain / プラスミド: pCWori / 発現宿主:  |
|---|
-非ポリマー , 5種, 530分子 
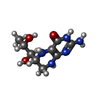
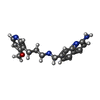






| #2: 化合物 | | #3: 化合物 | #4: 化合物 | #5: 化合物 | ChemComp-ZN / | #6: 水 | ChemComp-HOH / | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.74 Å3/Da / 溶媒含有率: 55.2 % / 解説: plate |
|---|---|
| 結晶化 | 温度: 277 K / 手法: 蒸気拡散法, シッティングドロップ法 / pH: 7.2 詳細: 8% PEG3350 35mM citric acid 65mM Bis-Tris-Propane 10% glycerol 5mM TCEP |
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  ALS ALS  / ビームライン: 8.2.2 / 波長: 1 Å / ビームライン: 8.2.2 / 波長: 1 Å |
| 検出器 | タイプ: ADSC QUANTUM 315 / 検出器: CCD / 日付: 2015年1月25日 / 詳細: mirrors |
| 放射 | モノクロメーター: graphite / プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 1 Å / 相対比: 1 |
| 反射 | 解像度: 1.95→60 Å / Num. obs: 76760 / % possible obs: 98.9 % / Observed criterion σ(I): -3 / 冗長度: 8.2 % / CC1/2: 0.997 / Rmerge(I) obs: 0.172 / Rpim(I) all: 0.092 / Rsym value: 0.172 / Net I/σ(I): 8.4 |
| 反射 シェル | 解像度: 1.95→2.01 Å / 冗長度: 7.9 % / Rmerge(I) obs: 4.151 / Mean I/σ(I) obs: 0.6 / Num. unique obs: 4368 / CC1/2: 0.283 / Rpim(I) all: 2.237 / Rsym value: 4.151 / % possible all: 96.9 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  フーリエ合成 フーリエ合成開始モデル: 4UH5 解像度: 1.95→57.232 Å / SU ML: 0.31 / 交差検証法: FREE R-VALUE / σ(F): 0.07 / 位相誤差: 29.12
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 減衰半径: 0.9 Å / VDWプローブ半径: 1.11 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 1.95→57.232 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLS | 手法: refined / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLSグループ |
|
 ムービー
ムービー コントローラー
コントローラー























 PDBj
PDBj









