[English] 日本語
 Yorodumi
Yorodumi- PDB-5n3c: cAMP-dependent Protein Kinase A from Cricetulus griseus in comple... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 5n3c | ||||||
|---|---|---|---|---|---|---|---|
| Title | cAMP-dependent Protein Kinase A from Cricetulus griseus in complex with fragment like molecule Thiophene-3-Carboximidamide | ||||||
 Components Components |
| ||||||
 Keywords Keywords | TRANSFERASE / fragment / complex / serine threonine kinase / cAMP / kinase / PKA | ||||||
| Function / homology |  Function and homology information Function and homology informationcAMP-dependent protein kinase inhibitor activity / histone H1-4S35 kinase activity / cAMP-dependent protein kinase / regulation of protein processing / cAMP-dependent protein kinase activity / cellular response to parathyroid hormone stimulus / protein localization to lipid droplet / regulation of bicellular tight junction assembly / cAMP-dependent protein kinase complex / dorsal/ventral neural tube patterning ...cAMP-dependent protein kinase inhibitor activity / histone H1-4S35 kinase activity / cAMP-dependent protein kinase / regulation of protein processing / cAMP-dependent protein kinase activity / cellular response to parathyroid hormone stimulus / protein localization to lipid droplet / regulation of bicellular tight junction assembly / cAMP-dependent protein kinase complex / dorsal/ventral neural tube patterning / interleukin-2-mediated signaling pathway / regulation of osteoblast differentiation / sperm capacitation / cellular response to cold / ciliary base / protein kinase A regulatory subunit binding / negative regulation of glycolytic process through fructose-6-phosphate / intracellular potassium ion homeostasis / mesoderm formation / TORC1 signaling / plasma membrane raft / axoneme / sperm flagellum / postsynaptic modulation of chemical synaptic transmission / negative regulation of TORC1 signaling / regulation of proteasomal protein catabolic process / protein serine/threonine/tyrosine kinase activity / protein export from nucleus / cellular response to glucagon stimulus / cellular response to nutrient levels / positive regulation of phagocytosis / positive regulation of gluconeogenesis / acrosomal vesicle / positive regulation of protein export from nucleus / negative regulation of smoothened signaling pathway / neuromuscular junction / neural tube closure / cellular response to glucose stimulus / positive regulation of cholesterol biosynthetic process / mRNA processing / adenylate cyclase-inhibiting G protein-coupled receptor signaling pathway / positive regulation of insulin secretion / manganese ion binding / cellular response to heat / adenylate cyclase-activating G protein-coupled receptor signaling pathway / regulation of cell cycle / nuclear speck / postsynapse / protein domain specific binding / protein serine kinase activity / protein serine/threonine kinase activity / ubiquitin protein ligase binding / centrosome / protein kinase binding / perinuclear region of cytoplasm / glutamatergic synapse / magnesium ion binding / mitochondrion / ATP binding / nucleus / cytoplasm / cytosol Similarity search - Function | ||||||
| Biological species |  | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.772 Å MOLECULAR REPLACEMENT / Resolution: 1.772 Å | ||||||
 Authors Authors | Siefker, C. / Heine, A. / Klebe, G. | ||||||
 Citation Citation |  Journal: Angew.Chem.Int.Ed.Engl. / Year: 2020 Journal: Angew.Chem.Int.Ed.Engl. / Year: 2020Title: Fragment Binding to Kinase Hinge: If Charge Distribution and Local pK a Shifts Mislead Popular Bioisosterism Concepts. Authors: Oebbeke, M. / Siefker, C. / Wagner, B. / Heine, A. / Klebe, G. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  5n3c.cif.gz 5n3c.cif.gz | 228.6 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb5n3c.ent.gz pdb5n3c.ent.gz | 186.3 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  5n3c.json.gz 5n3c.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/n3/5n3c https://data.pdbj.org/pub/pdb/validation_reports/n3/5n3c ftp://data.pdbj.org/pub/pdb/validation_reports/n3/5n3c ftp://data.pdbj.org/pub/pdb/validation_reports/n3/5n3c | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  5n33C  5n3dC  5n3eC  5n3hC  5n3jC  5n3qC  5n3sC  6snnC  6snxC  6soxC  6spmC  6spsC  6spuC  6spyC  6ypsC  6z08C  6z44C  6zn0C  4wihS S: Starting model for refinement C: citing same article ( |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| Unit cell |
|
- Components
Components
| #1: Protein | Mass: 41193.746 Da / Num. of mol.: 1 Source method: isolated from a genetically manipulated source Details: Phosphorylation of S11, S140, T198 and S339 / Source: (gene. exp.)   |
|---|---|
| #2: Protein/peptide | Mass: 1993.318 Da / Num. of mol.: 1 / Source method: obtained synthetically / Details: cAMP dependent protein kinase inhibitor peptide / Source: (synth.)  |
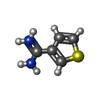
| #3: Chemical | ChemComp-8M2 / [ |
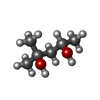
| #4: Chemical | ChemComp-MPD / ( |
| #5: Water | ChemComp-HOH / |
| Has protein modification | Y |
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.84 Å3/Da / Density % sol: 57 % |
|---|---|
| Crystal grow | Temperature: 277 K / Method: vapor diffusion, sitting drop / pH: 6.9 / Details: MES-BIS-TRIS Mega8-Solution DTT EDTA LiCl Methanol |
-Data collection
| Diffraction | Mean temperature: 100 K |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  ESRF ESRF  / Beamline: ID23-2 / Wavelength: 0.873 Å / Beamline: ID23-2 / Wavelength: 0.873 Å |
| Detector | Type: MARMOSAIC 225 mm CCD / Detector: CCD / Date: Jul 13, 2016 / Details: Silicon |
| Radiation | Monochromator: Si-111 crystal monochromator / Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength: 0.873 Å / Relative weight: 1 |
| Reflection | Resolution: 1.77→50 Å / Num. obs: 45623 / % possible obs: 99.8 % / Redundancy: 6.58 % / CC1/2: 0.99 / Rrim(I) all: 0.109 / Net I/σ(I): 13.24 |
| Reflection shell | Resolution: 1.77→1.88 Å / Redundancy: 6.41 % / Mean I/σ(I) obs: 3.06 / Num. unique obs: 7178 / CC1/2: 0.87 / Rrim(I) all: 0.595 / % possible all: 98.9 |
- Processing
Processing
| Software |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: 4WIH Resolution: 1.772→45.59 Å / SU ML: 0.17 / Cross valid method: FREE R-VALUE / σ(F): 1.37 / Phase error: 19.22
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.11 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 1.772→45.59 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller












 PDBj
PDBj