+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 4wmy | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
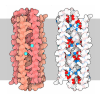
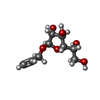
| タイトル | Structure of Human intelectin-1 in complex with allyl-beta-galactofuranose | |||||||||
 要素 要素 | Intelectin-1 | |||||||||
 キーワード キーワード | SUGAR BINDING PROTEIN / lectin / disulfide-linked / carbohydrate-binding / innate immunity / calcium / microbe-binding / microbe-specific / galactose / galactofuranose / diol | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報oligosaccharide binding / response to nematode / Antimicrobial peptides / protein homotrimerization / side of membrane / positive regulation of glucose import / brush border membrane / receptor complex / positive regulation of protein phosphorylation / membrane raft ...oligosaccharide binding / response to nematode / Antimicrobial peptides / protein homotrimerization / side of membrane / positive regulation of glucose import / brush border membrane / receptor complex / positive regulation of protein phosphorylation / membrane raft / calcium ion binding / extracellular space / extracellular exosome / extracellular region / identical protein binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / 解像度: 1.601 Å シンクロトロン / 解像度: 1.601 Å | |||||||||
 データ登録者 データ登録者 | Wangkanont, K. / Kiessling, L.L. / Forest, K.T. | |||||||||
 引用 引用 |  ジャーナル: Nat.Struct.Mol.Biol. / 年: 2015 ジャーナル: Nat.Struct.Mol.Biol. / 年: 2015タイトル: Recognition of microbial glycans by human intelectin-1. 著者: Wesener, D.A. / Wangkanont, K. / McBride, R. / Song, X. / Kraft, M.B. / Hodges, H.L. / Zarling, L.C. / Splain, R.A. / Smith, D.F. / Cummings, R.D. / Paulson, J.C. / Forest, K.T. / Kiessling, L.L. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  4wmy.cif.gz 4wmy.cif.gz | 146.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb4wmy.ent.gz pdb4wmy.ent.gz | 112.2 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  4wmy.json.gz 4wmy.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  4wmy_validation.pdf.gz 4wmy_validation.pdf.gz | 455.3 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  4wmy_full_validation.pdf.gz 4wmy_full_validation.pdf.gz | 458 KB | 表示 | |
| XML形式データ |  4wmy_validation.xml.gz 4wmy_validation.xml.gz | 29 KB | 表示 | |
| CIF形式データ |  4wmy_validation.cif.gz 4wmy_validation.cif.gz | 44.2 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/wm/4wmy https://data.pdbj.org/pub/pdb/validation_reports/wm/4wmy ftp://data.pdbj.org/pub/pdb/validation_reports/wm/4wmy ftp://data.pdbj.org/pub/pdb/validation_reports/wm/4wmy | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| |||||||||||||||
| 2 | 
| |||||||||||||||
| 単位格子 |
| |||||||||||||||
| Components on special symmetry positions |
| |||||||||||||||
| 詳細 | The biological assembly is a trimer. Application of the operations Z,X,Y and Y,Z,X will generate one trimer from the dimer in the asymmetric unit. The peripheral molecules correspond to another distinct trimer. |
- 要素
要素
| #1: タンパク質 | 分子量: 34258.516 Da / 分子数: 2 / 断片: carbohydrate-binding domain / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: ITLN1, INTL, ITLN, LFR, UNQ640/PRO1270 / プラスミド: pcDNA4 / 細胞株 (発現宿主): HEK293T / 発現宿主: Homo sapiens (ヒト) / 遺伝子: ITLN1, INTL, ITLN, LFR, UNQ640/PRO1270 / プラスミド: pcDNA4 / 細胞株 (発現宿主): HEK293T / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: Q8WWA0 Homo sapiens (ヒト) / 参照: UniProt: Q8WWA0#2: 化合物 | ChemComp-CA / #3: 糖 | #4: 水 | ChemComp-HOH / | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.17 Å3/Da / 溶媒含有率: 43.38 % |
|---|---|
| 結晶化 | 温度: 298 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 6 / 詳細: 100 mM Bis-Tris, 25% PEG 3350 |
-データ収集
| 回折 | 平均測定温度: 100 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  APS APS  / ビームライン: 21-ID-D / 波長: 1.00394 Å / ビームライン: 21-ID-D / 波長: 1.00394 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 検出器 | タイプ: MARMOSAIC 300 mm CCD / 検出器: CCD / 日付: 2014年7月20日 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 放射 | モノクロメーター: Si(111) / プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 放射波長 | 波長: 1.00394 Å / 相対比: 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 反射 | 解像度: 1.6→30.4 Å / Num. obs: 71869 / % possible obs: 100 % / 冗長度: 11.1 % / Biso Wilson estimate: 18.24 Å2 / Rmerge(I) obs: 0.078 / Rpim(I) all: 0.024 / Rrim(I) all: 0.082 / Χ2: 0.974 / Net I/av σ(I): 29.455 / Net I/σ(I): 9.7 / Num. measured all: 801024 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 反射 シェル | Diffraction-ID: 1 / Rejects: _
|
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 解像度: 1.601→28.586 Å / FOM work R set: 0.8915 / SU ML: 0.15 / 交差検証法: FREE R-VALUE / σ(F): 1.34 / 位相誤差: 17.68 / 立体化学のターゲット値: ML
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 減衰半径: 0.9 Å / VDWプローブ半径: 1.11 Å / 溶媒モデル: FLAT BULK SOLVENT MODEL | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso max: 77.02 Å2 / Biso mean: 21.68 Å2 / Biso min: 7.89 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: final / 解像度: 1.601→28.586 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル | Refine-ID: X-RAY DIFFRACTION / Total num. of bins used: 10 / % reflection obs: 100 %
|
 ムービー
ムービー コントローラー
コントローラー












 PDBj
PDBj