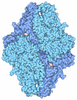
| 登録情報 | データベース: PDB / ID: 1wqv
|
|---|
| タイトル | Human Factor Viia-Tissue Factor Complexed with propylsulfonamide-D-Thr-Met-p-aminobenzamidine |
|---|
 要素 要素 | - (Coagulation factor ...) x 2
- Tissue factor
|
|---|
 キーワード キーワード | HYDROLASE/HYDROLASE INHIBITOR / SERINE PROTEASE / HYDROLASE-HYDROLASE INHIBITOR COMPLEX |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
activation of blood coagulation via clotting cascade / activation of plasma proteins involved in acute inflammatory response / coagulation factor VIIa / response to Thyroid stimulating hormone / response to 2,3,7,8-tetrachlorodibenzodioxine / response to astaxanthin / response to thyrotropin-releasing hormone / response to genistein / serine-type peptidase complex / positive regulation of platelet-derived growth factor receptor signaling pathway ...activation of blood coagulation via clotting cascade / activation of plasma proteins involved in acute inflammatory response / coagulation factor VIIa / response to Thyroid stimulating hormone / response to 2,3,7,8-tetrachlorodibenzodioxine / response to astaxanthin / response to thyrotropin-releasing hormone / response to genistein / serine-type peptidase complex / positive regulation of platelet-derived growth factor receptor signaling pathway / response to vitamin K / response to carbon dioxide / response to thyroxine / NGF-stimulated transcription / response to cholesterol / response to growth hormone / positive regulation of positive chemotaxis / Extrinsic Pathway of Fibrin Clot Formation / positive regulation of leukocyte chemotaxis / cytokine receptor activity / positive regulation of TOR signaling / positive regulation of blood coagulation / animal organ regeneration / Gamma-carboxylation of protein precursors / Transport of gamma-carboxylated protein precursors from the endoplasmic reticulum to the Golgi apparatus / Removal of aminoterminal propeptides from gamma-carboxylated proteins / positive regulation of endothelial cell proliferation / serine-type peptidase activity / BMAL1:CLOCK,NPAS2 activates circadian gene expression / positive regulation of interleukin-8 production / protein processing / phospholipid binding / cytokine-mediated signaling pathway / Golgi lumen / circadian rhythm / response to estrogen / positive regulation of angiogenesis / activation of cysteine-type endopeptidase activity involved in apoptotic process / blood coagulation / response to estradiol / collagen-containing extracellular matrix / protease binding / vesicle / response to hypoxia / positive regulation of cell migration / endoplasmic reticulum lumen / external side of plasma membrane / serine-type endopeptidase activity / signaling receptor binding / calcium ion binding / positive regulation of gene expression / cell surface / extracellular space / extracellular region / membrane / plasma membrane類似検索 - 分子機能 Tissue factor / Tissue factor, conserved site / Tissue factor signature. / Interferon/interleukin receptor domain / Interferon-alpha/beta receptor, fibronectin type III / Tissue factor / Peptidase S1A, coagulation factor VII/IX/X/C/Z / Coagulation factor-like, Gla domain superfamily / Coagulation Factor Xa inhibitory site / EGF-like domain ...Tissue factor / Tissue factor, conserved site / Tissue factor signature. / Interferon/interleukin receptor domain / Interferon-alpha/beta receptor, fibronectin type III / Tissue factor / Peptidase S1A, coagulation factor VII/IX/X/C/Z / Coagulation factor-like, Gla domain superfamily / Coagulation Factor Xa inhibitory site / EGF-like domain / EGF-type aspartate/asparagine hydroxylation site / EGF-like calcium-binding, conserved site / Calcium-binding EGF-like domain signature. / Aspartic acid and asparagine hydroxylation site. / EGF-like calcium-binding domain / Calcium-binding EGF-like domain / Vitamin K-dependent carboxylation/gamma-carboxyglutamic (GLA) domain / Gamma-carboxyglutamic acid-rich (GLA) domain / Gamma-carboxyglutamic acid-rich (GLA) domain superfamily / Vitamin K-dependent carboxylation domain. / Gla domain profile. / Domain containing Gla (gamma-carboxyglutamate) residues. / Epidermal growth factor-like domain. / EGF-like domain profile. / EGF-like domain signature 2. / EGF-like domain signature 1. / EGF-like domain / Fibronectin type III / Fibronectin type III superfamily / Serine proteases, trypsin family, histidine active site / Serine proteases, trypsin family, serine active site / Peptidase S1A, chymotrypsin family / Serine proteases, trypsin family, histidine active site. / Serine proteases, trypsin domain profile. / Serine proteases, trypsin family, serine active site. / Trypsin-like serine protease / Serine proteases, trypsin domain / Trypsin / Trypsin-like serine proteases / Thrombin, subunit H / Immunoglobulins / Peptidase S1, PA clan, chymotrypsin-like fold / Peptidase S1, PA clan / Immunoglobulin-like fold / Immunoglobulin-like / Beta Barrel / Sandwich / Mainly Beta類似検索 - ドメイン・相同性 beta-D-glucopyranose / alpha-L-fucopyranose / Chem-PSM / Coagulation factor VII / Tissue factor類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  フーリエ合成 / 解像度: 2.5 Å フーリエ合成 / 解像度: 2.5 Å |
|---|
 データ登録者 データ登録者 | Kadono, S. / Sakamoto, A. / Kikuchi, Y. / Oh-eda, M. / Yabuta, N. / Koga, T. / Hattori, K. / Shiraishi, T. / Haramura, M. / Kodama, H. |
|---|
 引用 引用 |  ジャーナル: Biochem.Biophys.Res.Commun. / 年: 2004 ジャーナル: Biochem.Biophys.Res.Commun. / 年: 2004
タイトル: Crystal structure of human factor VIIa/tissue factor in complex with peptide mimetic inhibitor
著者: Kadono, S. / Sakamoto, A. / Kikuchi, Y. / Oh-eda, M. / Yabuta, N. / Koga, T. / Hattori, K. / Shiraishi, T. / Haramura, M. / Kodama, H. / Esaki, T. / Sato, H. / Watanabe, Y. / Itoh, S. / Ohta, M. / Kozono, T. |
|---|
| 履歴 | | 登録 | 2004年10月2日 | 登録サイト: PDBJ / 処理サイト: PDBJ |
|---|
| 改定 1.0 | 2005年10月2日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2008年4月30日 | Group: Version format compliance |
|---|
| 改定 1.2 | 2011年7月13日 | Group: Atomic model / Database references ...Atomic model / Database references / Derived calculations / Non-polymer description / Structure summary / Version format compliance |
|---|
| 改定 1.3 | 2020年7月29日 | Group: Data collection / Derived calculations / Structure summary
カテゴリ: chem_comp / entity ...chem_comp / entity / pdbx_chem_comp_identifier / pdbx_entity_nonpoly / pdbx_struct_conn_angle / struct_conn / struct_site / struct_site_gen
Item: _chem_comp.name / _chem_comp.type ..._chem_comp.name / _chem_comp.type / _entity.pdbx_description / _pdbx_entity_nonpoly.name / _pdbx_struct_conn_angle.ptnr1_auth_asym_id / _pdbx_struct_conn_angle.ptnr1_auth_comp_id / _pdbx_struct_conn_angle.ptnr1_auth_seq_id / _pdbx_struct_conn_angle.ptnr1_label_asym_id / _pdbx_struct_conn_angle.ptnr1_label_atom_id / _pdbx_struct_conn_angle.ptnr1_label_comp_id / _pdbx_struct_conn_angle.ptnr1_label_seq_id / _pdbx_struct_conn_angle.ptnr2_auth_asym_id / _pdbx_struct_conn_angle.ptnr2_auth_seq_id / _pdbx_struct_conn_angle.ptnr2_label_asym_id / _pdbx_struct_conn_angle.ptnr3_auth_asym_id / _pdbx_struct_conn_angle.ptnr3_auth_comp_id / _pdbx_struct_conn_angle.ptnr3_auth_seq_id / _pdbx_struct_conn_angle.ptnr3_label_asym_id / _pdbx_struct_conn_angle.ptnr3_label_atom_id / _pdbx_struct_conn_angle.ptnr3_label_comp_id / _pdbx_struct_conn_angle.ptnr3_label_seq_id / _pdbx_struct_conn_angle.value / _struct_conn.conn_type_id / _struct_conn.id / _struct_conn.pdbx_dist_value / _struct_conn.pdbx_leaving_atom_flag / _struct_conn.pdbx_role / _struct_conn.ptnr1_auth_asym_id / _struct_conn.ptnr1_auth_comp_id / _struct_conn.ptnr1_auth_seq_id / _struct_conn.ptnr1_label_asym_id / _struct_conn.ptnr1_label_atom_id / _struct_conn.ptnr1_label_comp_id / _struct_conn.ptnr1_label_seq_id / _struct_conn.ptnr2_auth_asym_id / _struct_conn.ptnr2_auth_comp_id / _struct_conn.ptnr2_auth_seq_id / _struct_conn.ptnr2_label_asym_id / _struct_conn.ptnr2_label_atom_id / _struct_conn.ptnr2_label_comp_id / _struct_conn.ptnr2_label_seq_id
解説: Carbohydrate remediation / Provider: repository / タイプ: Remediation |
|---|
| 改定 1.4 | 2023年10月25日 | Group: Data collection / Database references ...Data collection / Database references / Refinement description / Structure summary
カテゴリ: chem_comp / chem_comp_atom ...chem_comp / chem_comp_atom / chem_comp_bond / database_2 / pdbx_initial_refinement_model
Item: _chem_comp.pdbx_synonyms / _database_2.pdbx_DOI / _database_2.pdbx_database_accession |
|---|
| 改定 1.5 | 2023年11月15日 | Group: Data collection / カテゴリ: chem_comp_atom / chem_comp_bond / Item: _chem_comp_atom.atom_id / _chem_comp_bond.atom_id_2 |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  フーリエ合成 / 解像度: 2.5 Å
フーリエ合成 / 解像度: 2.5 Å  データ登録者
データ登録者 引用
引用 ジャーナル: Biochem.Biophys.Res.Commun. / 年: 2004
ジャーナル: Biochem.Biophys.Res.Commun. / 年: 2004 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 1wqv.cif.gz
1wqv.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb1wqv.ent.gz
pdb1wqv.ent.gz PDB形式
PDB形式 1wqv.json.gz
1wqv.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 1wqv_validation.pdf.gz
1wqv_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 1wqv_full_validation.pdf.gz
1wqv_full_validation.pdf.gz 1wqv_validation.xml.gz
1wqv_validation.xml.gz 1wqv_validation.cif.gz
1wqv_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/wq/1wqv
https://data.pdbj.org/pub/pdb/validation_reports/wq/1wqv ftp://data.pdbj.org/pub/pdb/validation_reports/wq/1wqv
ftp://data.pdbj.org/pub/pdb/validation_reports/wq/1wqv
 リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト) / Cell (発現宿主): CHO / 発現宿主:
Homo sapiens (ヒト) / Cell (発現宿主): CHO / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: P08709, coagulation factor VIIa
Homo sapiens (ヒト) / 参照: UniProt: P08709, coagulation factor VIIa Homo sapiens (ヒト) / Cell (発現宿主): CHO / 発現宿主:
Homo sapiens (ヒト) / Cell (発現宿主): CHO / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: P08709, coagulation factor VIIa
Homo sapiens (ヒト) / 参照: UniProt: P08709, coagulation factor VIIa Homo sapiens (ヒト) / プラスミド: pKK223-3 / 発現宿主:
Homo sapiens (ヒト) / プラスミド: pKK223-3 / 発現宿主: 





 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  Photon Factory
Photon Factory  / ビームライン: BL-6B / 波長: 1 Å
/ ビームライン: BL-6B / 波長: 1 Å 解析
解析 フーリエ合成
フーリエ合成 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj