+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1taw | ||||||
|---|---|---|---|---|---|---|---|
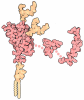
| タイトル | BOVINE TRYPSIN COMPLEXED TO APPI | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | COMPLEX (SERINE PROTEASE/INHIBITOR) / SERINE PROTEASE / KUNITZ TYPE INHIBITOR / COMPLEX / PROTEASE-SUBSTRATE INTERACTIONS / COMPLEX (SERINE PROTEASE-INHIBITOR) COMPLEX | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cytosolic mRNA polyadenylation / collateral sprouting in absence of injury / NMDA selective glutamate receptor signaling pathway / microglia development / regulation of Wnt signaling pathway / regulation of synapse structure or activity / Formyl peptide receptors bind formyl peptides and many other ligands / axo-dendritic transport / synaptic assembly at neuromuscular junction / signaling receptor activator activity ...cytosolic mRNA polyadenylation / collateral sprouting in absence of injury / NMDA selective glutamate receptor signaling pathway / microglia development / regulation of Wnt signaling pathway / regulation of synapse structure or activity / Formyl peptide receptors bind formyl peptides and many other ligands / axo-dendritic transport / synaptic assembly at neuromuscular junction / signaling receptor activator activity / axon midline choice point recognition / smooth endoplasmic reticulum calcium ion homeostasis / astrocyte activation involved in immune response / regulation of spontaneous synaptic transmission / mating behavior / ciliary rootlet / Lysosome Vesicle Biogenesis / PTB domain binding / Deregulated CDK5 triggers multiple neurodegenerative pathways in Alzheimer's disease models / Golgi-associated vesicle / Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / positive regulation of amyloid fibril formation / neuron remodeling / COPII-coated ER to Golgi transport vesicle / suckling behavior / nuclear envelope lumen / dendrite development / presynaptic active zone / modulation of excitatory postsynaptic potential / TRAF6 mediated NF-kB activation / The NLRP3 inflammasome / Advanced glycosylation endproduct receptor signaling / neuromuscular process controlling balance / negative regulation of long-term synaptic potentiation / regulation of presynapse assembly / transition metal ion binding / regulation of multicellular organism growth / negative regulation of neuron differentiation / intracellular copper ion homeostasis / trypsin / ECM proteoglycans / positive regulation of T cell migration / serpin family protein binding / spindle midzone / smooth endoplasmic reticulum / Purinergic signaling in leishmaniasis infection / protein serine/threonine kinase binding / regulation of peptidyl-tyrosine phosphorylation / clathrin-coated pit / positive regulation of chemokine production / forebrain development / serine protease inhibitor complex / digestion / Notch signaling pathway / neuron projection maintenance / Mitochondrial protein degradation / positive regulation of G2/M transition of mitotic cell cycle / positive regulation of protein metabolic process / cholesterol metabolic process / positive regulation of calcium-mediated signaling / ionotropic glutamate receptor signaling pathway / positive regulation of glycolytic process / response to interleukin-1 / extracellular matrix organization / positive regulation of mitotic cell cycle / axonogenesis / adult locomotory behavior / platelet alpha granule lumen / trans-Golgi network membrane / learning / positive regulation of interleukin-1 beta production / dendritic shaft / positive regulation of peptidyl-threonine phosphorylation / positive regulation of long-term synaptic potentiation / central nervous system development / endosome lumen / locomotory behavior / astrocyte activation / Post-translational protein phosphorylation / positive regulation of JNK cascade / microglial cell activation / synapse organization / regulation of long-term neuronal synaptic plasticity / TAK1-dependent IKK and NF-kappa-B activation / serine-type endopeptidase inhibitor activity / neuromuscular junction / visual learning / recycling endosome / cognition / Golgi lumen / positive regulation of inflammatory response / positive regulation of interleukin-6 production / neuron cellular homeostasis / positive regulation of non-canonical NF-kappaB signal transduction / Regulation of Insulin-like Growth Factor (IGF) transport and uptake by Insulin-like Growth Factor Binding Proteins (IGFBPs) / endocytosis / cellular response to amyloid-beta / G2/M transition of mitotic cell cycle / positive regulation of tumor necrosis factor production / neuron projection development 類似検索 - 分子機能 | ||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  X線回折 / X線回折 /  分子置換 / 解像度: 1.8 Å 分子置換 / 解像度: 1.8 Å | ||||||
 データ登録者 データ登録者 | Hynes, T.R. / Kossiakoff, A.A. | ||||||
 引用 引用 |  ジャーナル: Protein Sci. / 年: 1997 ジャーナル: Protein Sci. / 年: 1997タイトル: Crystal structures of bovine chymotrypsin and trypsin complexed to the inhibitor domain of Alzheimer's amyloid beta-protein precursor (APPI) and basic pancreatic trypsin inhibitor (BPTI) ...タイトル: Crystal structures of bovine chymotrypsin and trypsin complexed to the inhibitor domain of Alzheimer's amyloid beta-protein precursor (APPI) and basic pancreatic trypsin inhibitor (BPTI): engineering of inhibitors with altered specificities. 著者: Scheidig, A.J. / Hynes, T.R. / Pelletier, L.A. / Wells, J.A. / Kossiakoff, A.A. #1:  ジャーナル: Biochemistry / 年: 1990 ジャーナル: Biochemistry / 年: 1990タイトル: X-Ray Crystal Structure of the Protease Inhibitor Domain of Alzheimer'S Amyloid Beta-Protein Precursor 著者: Hynes, T.R. / Randal, M. / Kennedy, L.A. / Eigenbrot, C. / Kossiakoff, A.A. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1taw.cif.gz 1taw.cif.gz | 69.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1taw.ent.gz pdb1taw.ent.gz | 48.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1taw.json.gz 1taw.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  1taw_validation.pdf.gz 1taw_validation.pdf.gz | 416.6 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  1taw_full_validation.pdf.gz 1taw_full_validation.pdf.gz | 417.6 KB | 表示 | |
| XML形式データ |  1taw_validation.xml.gz 1taw_validation.xml.gz | 13.3 KB | 表示 | |
| CIF形式データ |  1taw_validation.cif.gz 1taw_validation.cif.gz | 18.5 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/ta/1taw https://data.pdbj.org/pub/pdb/validation_reports/ta/1taw ftp://data.pdbj.org/pub/pdb/validation_reports/ta/1taw ftp://data.pdbj.org/pub/pdb/validation_reports/ta/1taw | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 23310.303 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
|---|---|
| #2: タンパク質 | 分子量: 6420.147 Da / 分子数: 1 Fragment: RESIDUES 289 - 342 OF ALZHEIMER'S AMYLOID BETA-PROTEIN PRECURSOR 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: A4 / 器官: PANCREATIC / プラスミド: PA4G32R / 遺伝子 (発現宿主): A4 / 発現宿主: Homo sapiens (ヒト) / 遺伝子: A4 / 器官: PANCREATIC / プラスミド: PA4G32R / 遺伝子 (発現宿主): A4 / 発現宿主:  |
| #3: 化合物 | ChemComp-CA / |
| #4: 水 | ChemComp-HOH / |
| Has protein modification | Y |
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.74 Å3/Da / 溶媒含有率: 54.36 % | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | pH: 6.5 / 詳細: pH 6.5 | |||||||||||||||||||||||||
| 結晶化 | *PLUS 温度: 4 ℃ / 手法: 蒸気拡散法, ハンギングドロップ法 / 詳細: used to seeding | |||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 277 K |
|---|---|
| 放射光源 | 由来:  回転陽極 / タイプ: RIGAKU RUH2R / 波長: 1.5418 回転陽極 / タイプ: RIGAKU RUH2R / 波長: 1.5418 |
| 検出器 | タイプ: ENRAF-NONIUS FAST / 検出器: DIFFRACTOMETER / 日付: 1992年1月1日 |
| 放射 | モノクロメーター: GRAPHITE(002) / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 1.5418 Å / 相対比: 1 |
| 反射 | 解像度: 1.8→50 Å / Num. obs: 22374 / % possible obs: 76.6 % / Observed criterion σ(I): 0 / 冗長度: 3 % / Biso Wilson estimate: 31.5 Å2 / Rmerge(I) obs: 0.05 / Net I/σ(I): 10 |
| 反射 シェル | 解像度: 1.8→2 Å / 冗長度: 2 % / Rmerge(I) obs: 0.08 / Mean I/σ(I) obs: 2 / Rsym value: 0.25 / % possible all: 79.3 |
| 反射 | *PLUS Rmerge(I) obs: 0.059 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: PDB ENTRY 2PTC 解像度: 1.8→8 Å / Data cutoff high absF: 10000000 / Data cutoff low absF: 0.001 / σ(F): 0 /
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 39.23 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze | Luzzati coordinate error obs: 0.23 Å / Luzzati sigma a obs: 0.32 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 1.8→8 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Xplor file |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称:  X-PLOR / バージョン: 3.1 / 分類: refinement X-PLOR / バージョン: 3.1 / 分類: refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー
















 PDBj
PDBj