| 登録情報 | データベース: PDB / ID: 1svk
|
|---|
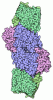
| タイトル | Structure of the K180P mutant of Gi alpha subunit bound to AlF4 and GDP |
|---|
 要素 要素 | Guanine nucleotide-binding protein G(i), alpha-1 subunit |
|---|
 キーワード キーワード | HYDROLASE / SIGNALING PROTEIN / Gi alpha subunit / K180P mutation / Active form |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
Extra-nuclear estrogen signaling / Adenylate cyclase inhibitory pathway / negative regulation of synaptic transmission / GTPase activating protein binding / Adrenaline,noradrenaline inhibits insulin secretion / ADP signalling through P2Y purinoceptor 12 / G alpha (i) signalling events / neurotransmitter receptor localization to postsynaptic specialization membrane / positive regulation of protein localization to cell cortex / T cell migration ...Extra-nuclear estrogen signaling / Adenylate cyclase inhibitory pathway / negative regulation of synaptic transmission / GTPase activating protein binding / Adrenaline,noradrenaline inhibits insulin secretion / ADP signalling through P2Y purinoceptor 12 / G alpha (i) signalling events / neurotransmitter receptor localization to postsynaptic specialization membrane / positive regulation of protein localization to cell cortex / T cell migration / D2 dopamine receptor binding / response to prostaglandin E / adenylate cyclase regulator activity / G protein-coupled serotonin receptor binding / adenylate cyclase-inhibiting serotonin receptor signaling pathway / cellular response to forskolin / regulation of mitotic spindle organization / positive regulation of cholesterol biosynthetic process / G protein-coupled receptor binding / adenylate cyclase-inhibiting G protein-coupled receptor signaling pathway / adenylate cyclase-modulating G protein-coupled receptor signaling pathway / G-protein beta/gamma-subunit complex binding / GDP binding / heterotrimeric G-protein complex / G protein activity / midbody / cell cortex / 加水分解酵素; 酸無水物に作用; GTPに作用・細胞または細胞小器官の運動に関与 / postsynapse / G protein-coupled receptor signaling pathway / cell division / GTPase activity / centrosome / GTP binding / glutamatergic synapse / magnesium ion binding / protein-containing complex / nucleus / plasma membrane / cytoplasm / cytosol類似検索 - 分子機能 GI Alpha 1, domain 2-like / GI Alpha 1, domain 2-like / G-protein alpha subunit, group I / Guanine nucleotide binding protein (G-protein), alpha subunit / G protein alpha subunit, helical insertion / G-protein alpha subunit / G-alpha domain profile. / G protein alpha subunit / P-loop containing nucleotide triphosphate hydrolases / Rossmann fold ...GI Alpha 1, domain 2-like / GI Alpha 1, domain 2-like / G-protein alpha subunit, group I / Guanine nucleotide binding protein (G-protein), alpha subunit / G protein alpha subunit, helical insertion / G-protein alpha subunit / G-alpha domain profile. / G protein alpha subunit / P-loop containing nucleotide triphosphate hydrolases / Rossmann fold / P-loop containing nucleoside triphosphate hydrolase / Orthogonal Bundle / 3-Layer(aba) Sandwich / Mainly Alpha / Alpha Beta類似検索 - ドメイン・相同性 TETRAFLUOROALUMINATE ION / GUANOSINE-5'-DIPHOSPHATE / Guanine nucleotide-binding protein G(i) subunit alpha-1類似検索 - 構成要素 |
|---|
| 生物種 |   Rattus norvegicus (ドブネズミ) Rattus norvegicus (ドブネズミ) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2 Å 分子置換 / 解像度: 2 Å |
|---|
 データ登録者 データ登録者 | Thomas, C.J. / Du, X. / Li, P. / Wang, Y. / Ross, E.M. / Sprang, S.R. |
|---|
 引用 引用 |  ジャーナル: Proc.Natl.Acad.Sci.USA / 年: 2004 ジャーナル: Proc.Natl.Acad.Sci.USA / 年: 2004
タイトル: Uncoupling conformational change from GTP hydrolysis in a heterotrimeric G protein {alpha}-subunit.
著者: Thomas, C.J. / Du, X. / Li, P. / Wang, Y. / Ross, E.M. / Sprang, S.R. |
|---|
| 履歴 | | 登録 | 2004年3月29日 | 登録サイト: RCSB / 処理サイト: RCSB |
|---|
| 改定 1.0 | 2004年6月1日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2008年4月30日 | Group: Version format compliance |
|---|
| 改定 1.2 | 2011年7月13日 | Group: Version format compliance |
|---|
| 改定 1.3 | 2021年10月27日 | Group: Database references / Derived calculations
カテゴリ: database_2 / pdbx_struct_conn_angle ...database_2 / pdbx_struct_conn_angle / struct_conn / struct_ref_seq_dif / struct_site
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession ..._database_2.pdbx_DOI / _database_2.pdbx_database_accession / _struct_conn.pdbx_dist_value / _struct_conn.pdbx_ptnr1_label_alt_id / _struct_conn.pdbx_ptnr2_label_alt_id / _struct_conn.ptnr1_auth_comp_id / _struct_conn.ptnr1_auth_seq_id / _struct_conn.ptnr1_label_asym_id / _struct_conn.ptnr1_label_atom_id / _struct_conn.ptnr1_label_comp_id / _struct_conn.ptnr1_label_seq_id / _struct_conn.ptnr2_auth_comp_id / _struct_conn.ptnr2_auth_seq_id / _struct_conn.ptnr2_label_asym_id / _struct_conn.ptnr2_label_atom_id / _struct_conn.ptnr2_label_comp_id / _struct_conn.ptnr2_label_seq_id / _struct_ref_seq_dif.details / _struct_site.pdbx_auth_asym_id / _struct_site.pdbx_auth_comp_id / _struct_site.pdbx_auth_seq_id |
|---|
| 改定 1.4 | 2023年8月23日 | Group: Data collection / Refinement description
カテゴリ: chem_comp_atom / chem_comp_bond / pdbx_initial_refinement_model |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報
 X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  分子置換 / 解像度: 2 Å
分子置換 / 解像度: 2 Å  データ登録者
データ登録者 引用
引用 ジャーナル: Proc.Natl.Acad.Sci.USA / 年: 2004
ジャーナル: Proc.Natl.Acad.Sci.USA / 年: 2004 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 1svk.cif.gz
1svk.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb1svk.ent.gz
pdb1svk.ent.gz PDB形式
PDB形式 1svk.json.gz
1svk.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 1svk_validation.pdf.gz
1svk_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 1svk_full_validation.pdf.gz
1svk_full_validation.pdf.gz 1svk_validation.xml.gz
1svk_validation.xml.gz 1svk_validation.cif.gz
1svk_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/sv/1svk
https://data.pdbj.org/pub/pdb/validation_reports/sv/1svk ftp://data.pdbj.org/pub/pdb/validation_reports/sv/1svk
ftp://data.pdbj.org/pub/pdb/validation_reports/sv/1svk リンク
リンク 集合体
集合体
 要素
要素

 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  ALS
ALS  / ビームライン: 5.0.1 / 波長: 0.9784
/ ビームライン: 5.0.1 / 波長: 0.9784  解析
解析 分子置換
分子置換 ムービー
ムービー コントローラー
コントローラー
















 PDBj
PDBj