+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1i10 | ||||||
|---|---|---|---|---|---|---|---|
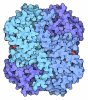
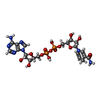
| タイトル | HUMAN MUSCLE L-LACTATE DEHYDROGENASE M CHAIN, TERNARY COMPLEX WITH NADH AND OXAMATE | ||||||
 要素 要素 | L-LACTATE DEHYDROGENASE M CHAIN | ||||||
 キーワード キーワード | OXIDOREDUCTASE / DEHYDROGENASE / ROSSMANN FOLD | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報sperm fibrous sheath / pyruvate catabolic process / oxidoreductase complex / L-lactate dehydrogenase / L-lactate dehydrogenase (NAD+) activity / Pyruvate metabolism / lactate metabolic process / : / substantia nigra development / Regulation of pyruvate metabolism ...sperm fibrous sheath / pyruvate catabolic process / oxidoreductase complex / L-lactate dehydrogenase / L-lactate dehydrogenase (NAD+) activity / Pyruvate metabolism / lactate metabolic process / : / substantia nigra development / Regulation of pyruvate metabolism / glycolytic process / cadherin binding / mitochondrion / extracellular exosome / membrane / identical protein binding / nucleus / cytosol 類似検索 - 分子機能 | ||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.3 Å 分子置換 / 解像度: 2.3 Å | ||||||
 データ登録者 データ登録者 | Read, J.A. / Winter, V.J. / Eszes, C.M. / Sessions, R.B. / Brady, R.L. | ||||||
 引用 引用 |  ジャーナル: Proteins / 年: 2001 ジャーナル: Proteins / 年: 2001タイトル: Structural basis for altered activity of M- and H-isozyme forms of human lactate dehydrogenase. 著者: Read, J.A. / Winter, V.J. / Eszes, C.M. / Sessions, R.B. / Brady, R.L. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1i10.cif.gz 1i10.cif.gz | 526.6 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1i10.ent.gz pdb1i10.ent.gz | 437.4 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1i10.json.gz 1i10.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/i1/1i10 https://data.pdbj.org/pub/pdb/validation_reports/i1/1i10 ftp://data.pdbj.org/pub/pdb/validation_reports/i1/1i10 ftp://data.pdbj.org/pub/pdb/validation_reports/i1/1i10 | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 単位格子 |
| ||||||||
| 詳細 | The biological assembly is composed of subunits A, B, C and D or E, F, G and H |
- 要素
要素
| #1: タンパク質 | 分子量: 36603.473 Da / 分子数: 8 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: LDHA / 器官: HEART / プラスミド: PKK223-3 / 生物種 (発現宿主): Escherichia coli / 発現宿主: Homo sapiens (ヒト) / 遺伝子: LDHA / 器官: HEART / プラスミド: PKK223-3 / 生物種 (発現宿主): Escherichia coli / 発現宿主:  #2: 化合物 | ChemComp-ACT / #3: 化合物 | ChemComp-NAI / #4: 化合物 | ChemComp-OXM / #5: 水 | ChemComp-HOH / | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.34 Å3/Da / 溶媒含有率: 47.42 % | ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | 温度: 291 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 7.5 詳細: protein solution: 28 mg/ml protein, 100 mM Na-HEPES pH 7.5, 2.5 mM NADH, 1 mM Na Oxamate. Well solution: 12% PEG 8K, 100 mM Na HEPES pH 7.5, 100 mM Na Acetate, VAPOR DIFFUSION, HANGING DROP, temperature 291K | ||||||||||||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 温度: 18 ℃詳細: drop consists of equal amounts of protein and reservoir solutions | ||||||||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  SRS SRS  / ビームライン: PX7.2 / 波長: 1.488 / ビームライン: PX7.2 / 波長: 1.488 |
| 検出器 | タイプ: MARRESEARCH / 検出器: IMAGE PLATE / 日付: 1999年9月13日 |
| 放射 | モノクロメーター: platinum mirrors/Ge 111 monochromator プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 1.488 Å / 相対比: 1 |
| 反射 | 解像度: 2.3→30 Å / Num. all: 121781 / Num. obs: 112344 / % possible obs: 92.3 % / Observed criterion σ(F): 2 / Observed criterion σ(I): 2 / 冗長度: 3.51 % / Rmerge(I) obs: 0.081 / Net I/σ(I): 14.18 |
| 反射 シェル | 解像度: 2.3→2.4 Å / 冗長度: 3.53 % / Rmerge(I) obs: 0.195 / Mean I/σ(I) obs: 5.36 / Num. unique all: 13397 / % possible all: 89 |
| 反射 シェル | *PLUS % possible obs: 89 % |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: 9ldt 解像度: 2.3→20 Å / SU B: 8.643 / SU ML: 0.211 / SU Rfree: 0.279 / 交差検証法: THROUGHOUT / σ(F): 0 / σ(I): 0 / ESU R: 0.487 / ESU R Free: 0.279 / 立体化学のターゲット値: ENGH AND HUBER 詳細: Scaling details: Babinet's principle for scaling has been used. Bulk solvent correction based on constant value has been used. Parameters for mask calculation: VDW prob radii = 1.40; ION prob ...詳細: Scaling details: Babinet's principle for scaling has been used. Bulk solvent correction based on constant value has been used. Parameters for mask calculation: VDW prob radii = 1.40; ION prob radii = 0.80; Shrinkage radii = 0.80. CNS was also used for refinement.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 27.066 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.3→20 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称: REFMAC / 分類: refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | *PLUS Rfactor obs: 0.2 / Rfactor Rfree: 0.257 / Rfactor Rwork: 0.197 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS |
 ムービー
ムービー コントローラー
コントローラー

















 PDBj
PDBj