| 登録情報 | データベース: PDB / ID: 1az2
|
|---|
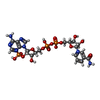
| タイトル | CITRATE BOUND, C298A/W219Y MUTANT HUMAN ALDOSE REDUCTASE |
|---|
 要素 要素 | ALDOSE REDUCTASE |
|---|
 キーワード キーワード | OXIDOREDUCTASE / ALDO-KETO REDUCTASE / INHIBITOR BINDING |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
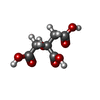
glyceraldehyde oxidoreductase activity / Fructose biosynthesis / fructose biosynthetic process / L-glucuronate reductase activity / aldose reductase / D/L-glyceraldehyde reductase / glycerol dehydrogenase (NADP+) activity / C21-steroid hormone biosynthetic process / NADP-retinol dehydrogenase / Pregnenolone biosynthesis ...glyceraldehyde oxidoreductase activity / Fructose biosynthesis / fructose biosynthetic process / L-glucuronate reductase activity / aldose reductase / D/L-glyceraldehyde reductase / glycerol dehydrogenase (NADP+) activity / C21-steroid hormone biosynthetic process / NADP-retinol dehydrogenase / Pregnenolone biosynthesis / allyl-alcohol dehydrogenase / allyl-alcohol dehydrogenase activity / Galactose catabolism / regulation of urine volume / prostaglandin H2 endoperoxidase reductase activity / all-trans-retinol dehydrogenase (NADP+) activity / metanephric collecting duct development / daunorubicin metabolic process / doxorubicin metabolic process / retinal dehydrogenase (NAD+) activity / epithelial cell maturation / aldose reductase (NADPH) activity / cellular hyperosmotic salinity response / retinoid metabolic process / renal water homeostasis / carbohydrate metabolic process / electron transfer activity / negative regulation of apoptotic process / mitochondrion / : / extracellular exosome / nucleoplasm / cytosol類似検索 - 分子機能 Aldo/keto reductase family putative active site signature. / Aldo/keto reductase family signature 1. / NADP-dependent oxidoreductase domain / Aldo/keto reductase family signature 2. / Aldo/keto reductase, conserved site / Aldo-keto reductase / NADP-dependent oxidoreductase domain / Aldo/keto reductase family / NADP-dependent oxidoreductase domain superfamily / TIM Barrel ...Aldo/keto reductase family putative active site signature. / Aldo/keto reductase family signature 1. / NADP-dependent oxidoreductase domain / Aldo/keto reductase family signature 2. / Aldo/keto reductase, conserved site / Aldo-keto reductase / NADP-dependent oxidoreductase domain / Aldo/keto reductase family / NADP-dependent oxidoreductase domain superfamily / TIM Barrel / Alpha-Beta Barrel / Alpha Beta類似検索 - ドメイン・相同性 CITRIC ACID / NADP NICOTINAMIDE-ADENINE-DINUCLEOTIDE PHOSPHATE / Aldo-keto reductase family 1 member B1類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 |  X線回折 / DIFFERENCE FOURIER / 解像度: 2.9 Å X線回折 / DIFFERENCE FOURIER / 解像度: 2.9 Å |
|---|
 データ登録者 データ登録者 | Harrison, D.H. / Bohren, K.M. / Ringe, D. / Petsko, G.A. / Gabbay, K.H. |
|---|
 引用 引用 |  ジャーナル: Biochemistry / 年: 1997 ジャーナル: Biochemistry / 年: 1997
タイトル: The alrestatin double-decker: binding of two inhibitor molecules to human aldose reductase reveals a new specificity determinant.
著者: Harrison, D.H. / Bohren, K.M. / Petsko, G.A. / Ringe, D. / Gabbay, K.H. |
|---|
| 履歴 | | 登録 | 1997年11月24日 | 処理サイト: BNL |
|---|
| 改定 1.0 | 1998年3月18日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2008年3月24日 | Group: Version format compliance |
|---|
| 改定 1.2 | 2011年7月13日 | Group: Version format compliance |
|---|
| 改定 1.3 | 2018年4月4日 | Group: Data collection / Other / カテゴリ: diffrn_source / pdbx_database_status
Item: _diffrn_source.type / _pdbx_database_status.process_site |
|---|
| 改定 1.4 | 2021年11月3日 | Group: Database references / Derived calculations / カテゴリ: database_2 / struct_ref_seq_dif / struct_site
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession ..._database_2.pdbx_DOI / _database_2.pdbx_database_accession / _struct_ref_seq_dif.details / _struct_site.pdbx_auth_asym_id / _struct_site.pdbx_auth_comp_id / _struct_site.pdbx_auth_seq_id |
|---|
| 改定 1.5 | 2023年8月2日 | Group: Refinement description / カテゴリ: pdbx_initial_refinement_model |
|---|
| 改定 1.6 | 2024年5月22日 | Group: Data collection / カテゴリ: chem_comp_atom / chem_comp_bond |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) X線回折 / DIFFERENCE FOURIER / 解像度: 2.9 Å
X線回折 / DIFFERENCE FOURIER / 解像度: 2.9 Å  データ登録者
データ登録者 引用
引用 ジャーナル: Biochemistry / 年: 1997
ジャーナル: Biochemistry / 年: 1997 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 1az2.cif.gz
1az2.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb1az2.ent.gz
pdb1az2.ent.gz PDB形式
PDB形式 1az2.json.gz
1az2.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード https://data.pdbj.org/pub/pdb/validation_reports/az/1az2
https://data.pdbj.org/pub/pdb/validation_reports/az/1az2 ftp://data.pdbj.org/pub/pdb/validation_reports/az/1az2
ftp://data.pdbj.org/pub/pdb/validation_reports/az/1az2 リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト) / 細胞株: BL21 / 遺伝子: ALR2 / プラスミド: PET / 生物種 (発現宿主): Escherichia coli / 遺伝子 (発現宿主): ALR2 / 発現宿主:
Homo sapiens (ヒト) / 細胞株: BL21 / 遺伝子: ALR2 / プラスミド: PET / 生物種 (発現宿主): Escherichia coli / 遺伝子 (発現宿主): ALR2 / 発現宿主: 
 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 回転陽極 / タイプ: ELLIOTT GX-6 / 波長: 1.5418
回転陽極 / タイプ: ELLIOTT GX-6 / 波長: 1.5418  解析
解析 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj