+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-9326 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | BEST1 calcium-bound open state | |||||||||
 マップデータ マップデータ | BEST1 calcium-bound open state | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | ion channel / calcium activated chloride channel / eukaryotic membrane protein / anion channel / transport protein / ligand gated ion channel / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 | Bestrophin-1 / Stimuli-sensing channels / Bestrophin / Bestrophin/UPF0187 / Bestrophin, RFP-TM, chloride channel / chloride channel activity / metal ion binding / membrane / Bestrophin 1 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Miller AN / Vaisey G | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2019 ジャーナル: Elife / 年: 2019タイトル: Molecular mechanisms of gating in the calcium-activated chloride channel bestrophin. 著者: Alexandria N Miller / George Vaisey / Stephen B Long /  要旨: Bestrophin (BEST1-4) ligand-gated chloride (Cl) channels are activated by calcium (Ca). Mutation of BEST1 causes retinal disease. Partly because bestrophin channels have no sequence or structural ...Bestrophin (BEST1-4) ligand-gated chloride (Cl) channels are activated by calcium (Ca). Mutation of BEST1 causes retinal disease. Partly because bestrophin channels have no sequence or structural similarity to other ion channels, the molecular mechanisms underlying gating are unknown. Here, we present a series of cryo-electron microscopy structures of chicken BEST1, determined at 3.1 Å resolution or better, that represent the channel's principal gating states. Unlike other channels, opening of the pore is due to the repositioning of tethered pore-lining helices within a surrounding protein shell that dramatically widens a neck of the pore through a concertina of amino acid rearrangements. The neck serves as both the activation and the inactivation gate. Ca binding instigates opening of the neck through allosteric means whereas inactivation peptide binding induces closing. An aperture within the otherwise wide pore controls anion permeability. The studies define a new molecular paradigm for gating among ligand-gated ion channels. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_9326.map.gz emd_9326.map.gz | 11.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-9326-v30.xml emd-9326-v30.xml emd-9326.xml emd-9326.xml | 12.5 KB 12.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_9326.png emd_9326.png | 181.6 KB | ||
| Filedesc metadata |  emd-9326.cif.gz emd-9326.cif.gz | 5.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-9326 http://ftp.pdbj.org/pub/emdb/structures/EMD-9326 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9326 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9326 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_9326_validation.pdf.gz emd_9326_validation.pdf.gz | 589.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_9326_full_validation.pdf.gz emd_9326_full_validation.pdf.gz | 589.4 KB | 表示 | |
| XML形式データ |  emd_9326_validation.xml.gz emd_9326_validation.xml.gz | 5.4 KB | 表示 | |
| CIF形式データ |  emd_9326_validation.cif.gz emd_9326_validation.cif.gz | 6.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9326 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9326 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9326 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9326 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6n28MC  9321C  9322C  9323C  9324C  9325C  6n23C  6n24C  6n25C  6n26C  6n27C M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_9326.map.gz / 形式: CCP4 / 大きさ: 12.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_9326.map.gz / 形式: CCP4 / 大きさ: 12.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | BEST1 calcium-bound open state | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.088 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
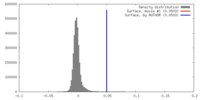
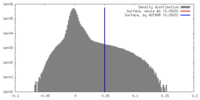
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : BEST1 calcium-bound open state
| 全体 | 名称: BEST1 calcium-bound open state |
|---|---|
| 要素 |
|
-超分子 #1: BEST1 calcium-bound open state
| 超分子 | 名称: BEST1 calcium-bound open state / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Bestrophin homolog
| 分子 | 名称: Bestrophin homolog / タイプ: protein_or_peptide / ID: 1 / コピー数: 5 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 40.761727 KDa |
| 組換発現 | 生物種:  Komagataella pastoris (菌類) Komagataella pastoris (菌類) |
| 配列 | 文字列: TVTYTNRVAD ARLGTFSQLL LQWKGSIYKL LYSEFLIFIS LYFAISLVYR LILSESQRLM FEKLALYCNS YAELIPVSFV LGFYVSLVV SRWWAQYESI PWPDRIMNLV SCNVDGEDEY GRLLRRTLMR YSNLCSVLIL RSVSTAVYKR FPSMEHVVRA G LMTPEEHK ...文字列: TVTYTNRVAD ARLGTFSQLL LQWKGSIYKL LYSEFLIFIS LYFAISLVYR LILSESQRLM FEKLALYCNS YAELIPVSFV LGFYVSLVV SRWWAQYESI PWPDRIMNLV SCNVDGEDEY GRLLRRTLMR YSNLCSVLIL RSVSTAVYKR FPSMEHVVRA G LMTPEEHK KFESLNSPHN KFWIPCVWFS NLAVKARNEG RIRDSVLLQG ILNELNTLRS QCGRLYGYDW ISIPLVYTQV VT VAVYSFF LACLIGRQFL DPEKAYPGHE LDLFVPVFTF LQFFFYAGWL KVAEQLINPF GEDDDDFETN WLIDRNLQVS LMA VDEMHQ DLPILEKDLY WNEPDPQEGE EF UniProtKB: Bestrophin 1 |
-分子 #2: CALCIUM ION
| 分子 | 名称: CALCIUM ION / タイプ: ligand / ID: 2 / コピー数: 5 / 式: CA |
|---|---|
| 分子量 | 理論値: 40.078 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| グリッド | 詳細: unspecified |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 293 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - 画像ごとのフレーム数: 1-40 / 撮影したグリッド数: 1 / 平均露光時間: 10.0 sec. / 平均電子線量: 76.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: OTHER / 撮影モード: BRIGHT FIELD |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー








 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)