+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM map of the intact shell of alpha-carboxysome from Prochlorococcus MED4 | ||||||||||||||||||
 マップデータ マップデータ | |||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||
 キーワード キーワード | alpha-carboxysome / carbon fixation / PHOTOSYNTHESIS | ||||||||||||||||||
| 生物種 |  Prochlorococcus sp. MED4 (バクテリア) / Prochlorococcus sp. MED4 (バクテリア) /  Prochlorococcus (バクテリア) Prochlorococcus (バクテリア) | ||||||||||||||||||
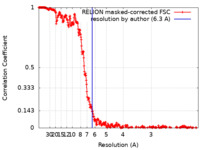
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 6.3 Å | ||||||||||||||||||
 データ登録者 データ登録者 | Jiang YL / Zhou RQ / Zhou CZ / Zeng QL | ||||||||||||||||||
| 資金援助 |  中国, 中国,  香港, 5件 香港, 5件
| ||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Plants / 年: 2024 ジャーナル: Nat Plants / 年: 2024タイトル: Structure and assembly of the α-carboxysome in the marine cyanobacterium Prochlorococcus. 著者: Rui-Qian Zhou / Yong-Liang Jiang / Haofu Li / Pu Hou / Wen-Wen Kong / Jia-Xin Deng / Yuxing Chen / Cong-Zhao Zhou / Qinglu Zeng /  要旨: Carboxysomes are bacterial microcompartments that encapsulate the enzymes RuBisCO and carbonic anhydrase in a proteinaceous shell to enhance the efficiency of photosynthetic carbon fixation. The self- ...Carboxysomes are bacterial microcompartments that encapsulate the enzymes RuBisCO and carbonic anhydrase in a proteinaceous shell to enhance the efficiency of photosynthetic carbon fixation. The self-assembly principles of the intact carboxysome remain elusive. Here we purified α-carboxysomes from Prochlorococcus and examined their intact structures using single-particle cryo-electron microscopy to solve the basic principles of their shell construction and internal RuBisCO organization. The 4.2 Å icosahedral-like shell structure reveals 24 CsoS1 hexamers on each facet and one CsoS4A pentamer at each vertex. RuBisCOs are organized into three concentric layers within the shell, consisting of 72, 32 and up to 4 RuBisCOs at the outer, middle and inner layers, respectively. We uniquely show how full-length and shorter forms of the scaffolding protein CsoS2 bind to the inner surface of the shell via repetitive motifs in the middle and C-terminal regions. Combined with previous reports, we propose a concomitant 'outside-in' assembly principle of α-carboxysomes: the inner surface of the self-assembled shell is reinforced by the middle and C-terminal motifs of the scaffolding protein, while the free N-terminal motifs cluster to recruit RuBisCO in concentric, three-layered spherical arrangements. These new insights into the coordinated assembly of α-carboxysomes may guide the rational design and repurposing of carboxysome structures for improving plant photosynthetic efficiency. | ||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_38544.map.gz emd_38544.map.gz | 469 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-38544-v30.xml emd-38544-v30.xml emd-38544.xml emd-38544.xml | 15.6 KB 15.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_38544_fsc.xml emd_38544_fsc.xml | 34.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_38544.png emd_38544.png | 80.8 KB | ||
| Filedesc metadata |  emd-38544.cif.gz emd-38544.cif.gz | 5.1 KB | ||
| その他 |  emd_38544_half_map_1.map.gz emd_38544_half_map_1.map.gz emd_38544_half_map_2.map.gz emd_38544_half_map_2.map.gz | 2.7 GB 2.7 GB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-38544 http://ftp.pdbj.org/pub/emdb/structures/EMD-38544 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-38544 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-38544 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_38544_validation.pdf.gz emd_38544_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_38544_full_validation.pdf.gz emd_38544_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_38544_validation.xml.gz emd_38544_validation.xml.gz | 39.6 KB | 表示 | |
| CIF形式データ |  emd_38544_validation.cif.gz emd_38544_validation.cif.gz | 55.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38544 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38544 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38544 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38544 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_38544.map.gz / 形式: CCP4 / 大きさ: 3.3 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_38544.map.gz / 形式: CCP4 / 大きさ: 3.3 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.06 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_38544_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_38544_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : alpha-carboxysome shell
| 全体 | 名称: alpha-carboxysome shell |
|---|---|
| 要素 |
|
-超分子 #1: alpha-carboxysome shell
| 超分子 | 名称: alpha-carboxysome shell / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Prochlorococcus sp. MED4 (バクテリア) Prochlorococcus sp. MED4 (バクテリア) |
| 分子量 | 理論値: 39.6 MDa |
-分子 #1: the shell hexamer CsoS1
| 分子 | 名称: the shell hexamer CsoS1 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 配列 | 文字列: MGIALGMIET RGLVPAIEAA DAMTKAAEVR LIGREFVGGG YVTVLVRGET GAVNA AVRA GADACERVGD GLVAAHIIAR PHREVEPALG NGDFLGQKD |
-分子 #2: The shell pentamer CsoS4A
| 分子 | 名称: The shell pentamer CsoS4A / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Prochlorococcus (バクテリア) Prochlorococcus (バクテリア) |
| 配列 | 文字列: MLICKVLKPL VSTNRIPGFE HKHLQVVLDG SSNKVAVDAV GCKPGDWVIC VGSSAAREAA GSKSYPSDL TIVGIIDHWD PDSPKQIEV |
-分子 #3: The scaffolding protein CsoS2
| 分子 | 名称: The scaffolding protein CsoS2 / タイプ: protein_or_peptide / ID: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Prochlorococcus (バクテリア) Prochlorococcus (バクテリア) |
| 配列 | 文字列: MSTKTSREIA LERRKAMSDG GKKAALHSSS TKDRVRSSQD INSTGATSSN KKVLTSPSKS NIPANKIAR KSTSSKLSSK ELGIERRKAM STHGKSAINS SDRTRTDVKS DIKVNKVIST E KPQALKDH NNNIKDNQVV KQNIKRRINQ KRKPITNTSR DIVLARREAQ ...文字列: MSTKTSREIA LERRKAMSDG GKKAALHSSS TKDRVRSSQD INSTGATSSN KKVLTSPSKS NIPANKIAR KSTSSKLSSK ELGIERRKAM STHGKSAINS SDRTRTDVKS DIKVNKVIST E KPQALKDH NNNIKDNQVV KQNIKRRINQ KRKPITNTSR DIVLARREAQ SKHGKSASKQ NT SAASLAR RGDPDLSSRE ISQRVRELRS KTGSTSKQGN GKCRPCGPNK NGSKLNIADA SWK VGKSET DSGQTVTGTQ ANRSLKTTGN EASTCRTVTG TQYMGAEVTG QFCQDKPKYK QPIR ASVTT TTSGNKVTGN EVGRSEKVTG DEPGTCKNLT GTEYISANQS KKYCGEVIKK PSKVM QSIT TDGLKVSGSL PGRSSLVTGD ESGSGKQLTG DQYLGSEPSP KGKSFEKVGS YDTLNG NNV TGTGVGRSDY VTGNEYGSCK NLTGDEYIGS QQYEKFCGST PKPEARKVGL SLSSKSN LI SGTMTGRSKI VTGDEPGSCK VLTGTPYAGL DQINDNCNAE IADDMKSRAT VNSGNNSN A RLTGLQPGIG GVMTGATKGS CKNLTGTPYI GGDQFLSNCE TPPNDASYAN QEKSASNSW KEFSVNSPSR EKYSAKNTEG VTGNRYEDSS KITGPFDMAE DKVTGTEQFR FEPNKNMTYK QKMKQEESQ NIDIPTDKKE PSKITGEGQS AGNITGDDWD RGDKVTGTEG VSARKRNPSR A GFMGAMPP VDNKRNDETE KPDFLITGSS GNTRDGQLVT FSGGARG |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8.5 詳細: 10 mM Bicine, 1 mM EDTA, 10 mM MgCl2, and dissolved in natural sea water, pH 8.5, supplemented with 0.6 mM PMSF and 20 mM NaHCO3 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー








 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)