+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Sulfur Oxygenase Reductase from Acidianus ambivalens | |||||||||
 マップデータ マップデータ | CryoEM map of Sulfur Oxygenase reductase at 2.8 Angstroms resolution | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Thermostable Oxidoreductase / OXIDOREDUCTASE | |||||||||
| 機能・相同性 | sulfur oxygenase/reductase / sulfur oxygenase/reductase activity / Sulphur oxygenase reductase / Sulphur oxygenase reductase / Dimeric alpha-beta barrel / metal ion binding / cytoplasm / Sulfur oxygenase/reductase 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Acidianus ambivalens (古細菌) Acidianus ambivalens (古細菌) | |||||||||
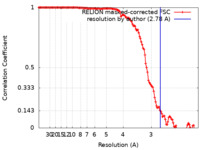
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.78 Å | |||||||||
 データ登録者 データ登録者 | Sobhy MA / Hamdan SM | |||||||||
| 資金援助 |  サウジアラビア, 1件 サウジアラビア, 1件
| |||||||||
 引用 引用 |  ジャーナル: PLoS One / 年: 2022 ジャーナル: PLoS One / 年: 2022タイトル: Cryo-electron structures of the extreme thermostable enzymes Sulfur Oxygenase Reductase and Lumazine Synthase. 著者: Mohamed A Sobhy / Lingyun Zhao / Dalaver Anjum / Ali Behzad / Masateru Takahashi / Muhammad Tehseen / Alfredo De Biasio / Rachid Sougrat / Samir Hamdan /  要旨: Thermostable enzymes have the potential for use in a wide variety of biotechnological applications. Cryo-electron microscopy (cryo-EM) enables the imaging of biomolecules in their native aqueous ...Thermostable enzymes have the potential for use in a wide variety of biotechnological applications. Cryo-electron microscopy (cryo-EM) enables the imaging of biomolecules in their native aqueous environment. Here, we present high resolution cryo-EM structures of two thermostable enzymes that exhibit multimeric cage-like structures arranged into two different point-group symmetries. First, we determined the structure of the Sulfur Oxygenase Reductase (SOR) enzyme that catalyzes both the oxygenation and disproportionation of elemental sulfur in Archea and is composed of 24 homomeric units each of MW ≃ 35 kDa arranged in octahedral symmetry. The structure of SOR from Acidianus ambivalens (7X9W) was determined at 2.78 Å resolution. The active site of each subunit inside the central nanocompartment is composed of Fe3+ coordinated to two water molecules and the three amino acids (H86, H90 and E114). Second, we determined the structure of Lumazine Synthase (LS) from Aquifex aeolicus (7X7M) at 2.33 Å resolution. LS forms a cage-like structure consisting of 60 identical subunits each of MW ≃ 15 kDa arranged in a strict icosahedral symmetry. The LS subunits are interconnected by ion-pair network. Due to their thermostability and relatively easy purification scheme, both SOR and LS can serve as a model for the catalytic and structural characterization of biocatalysts as well as a benchmark for cryo-EM sample preparation, optimization of the acquisition parameters and 3D reconstruction. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_33084.map.gz emd_33084.map.gz | 164.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-33084-v30.xml emd-33084-v30.xml emd-33084.xml emd-33084.xml | 19.9 KB 19.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_33084_fsc.xml emd_33084_fsc.xml | 12.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_33084.png emd_33084.png | 293.7 KB | ||
| Filedesc metadata |  emd-33084.cif.gz emd-33084.cif.gz | 6.6 KB | ||
| その他 |  emd_33084_half_map_1.map.gz emd_33084_half_map_1.map.gz emd_33084_half_map_2.map.gz emd_33084_half_map_2.map.gz | 135.2 MB 135.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-33084 http://ftp.pdbj.org/pub/emdb/structures/EMD-33084 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-33084 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-33084 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7x9wMC  7x7mC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_33084.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_33084.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | CryoEM map of Sulfur Oxygenase reductase at 2.8 Angstroms resolution | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.06 Å | ||||||||||||||||||||||||||||||||||||
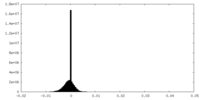
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: half map 1
| ファイル | emd_33084_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
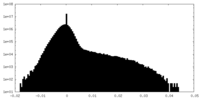
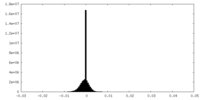
| 密度ヒストグラム |
-ハーフマップ: half map 2
| ファイル | emd_33084_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
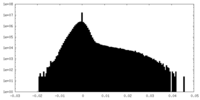
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : CryoEM structure of Sulfur Oxygenase Reductase composed of 24 ide...
| 全体 | 名称: CryoEM structure of Sulfur Oxygenase Reductase composed of 24 identical subunits |
|---|---|
| 要素 |
|
-超分子 #1: CryoEM structure of Sulfur Oxygenase Reductase composed of 24 ide...
| 超分子 | 名称: CryoEM structure of Sulfur Oxygenase Reductase composed of 24 identical subunits タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Acidianus ambivalens (古細菌) Acidianus ambivalens (古細菌) |
-分子 #1: Sulfur oxygenase/reductase
| 分子 | 名称: Sulfur oxygenase/reductase / タイプ: protein_or_peptide / ID: 1 / コピー数: 24 / 光学異性体: LEVO / EC番号: sulfur oxygenase/reductase |
|---|---|
| 由来(天然) | 生物種:  Acidianus ambivalens (古細菌) Acidianus ambivalens (古細菌) |
| 分子量 | 理論値: 35.128555 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: PKPYVAINMA ELKNEPKTFE MFASVGPKV(CSS) MVTARHPGFV GFQNHIQIGI LPFGNRYGGA KMDMTKESST VRVLQY TFW KDWKDHEEMH RQNWSYLFRL CYSCASQMIW GPWEPIYEII YANMPINTEM TDFTAVVGKK FAEGKPLDIP VISQPYG KR ...文字列: PKPYVAINMA ELKNEPKTFE MFASVGPKV(CSS) MVTARHPGFV GFQNHIQIGI LPFGNRYGGA KMDMTKESST VRVLQY TFW KDWKDHEEMH RQNWSYLFRL CYSCASQMIW GPWEPIYEII YANMPINTEM TDFTAVVGKK FAEGKPLDIP VISQPYG KR VVAFAEHSVI PGKEKQFEDA IVRTLEMLKK APGFLGAMVL KEIGVSGIGS MQFGAKGFHQ VLENPGSLEP DPNNVMYS V PEAKNTPQQY IVHVEWANTD ALMFGMGRVL LYPELRQVHD EVLDTLVYGP YIRILNPMME GTFWREYLNE UniProtKB: Sulfur oxygenase/reductase |
-分子 #2: FE (III) ION
| 分子 | 名称: FE (III) ION / タイプ: ligand / ID: 2 / コピー数: 24 / 式: FE |
|---|---|
| 分子量 | 理論値: 55.845 Da |
-分子 #3: water
| 分子 | 名称: water / タイプ: ligand / ID: 3 / コピー数: 48 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 6 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| |||||||||
| グリッド | モデル: Quantifoil R2/2 / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK I 詳細: The purified protein was applied to the glow discharged grids inside the chamber, blotted for a duration of 1.5 s, and then plunge-frozen in liquid ethane cooled by liquid nitrogen.. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / 平均電子線量: 68.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 130000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)