+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-30778 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Acidic stable capsid structure of Helicobacter pylori bacteriophage KHP30 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | CAPSID / PHAGE / PHAGE HEAD / CRYOEM / VIRUS | |||||||||
| 機能・相同性 | Protein of unknown function DUF4043 / Phage capsid protein / Major structural protein ORF14 / Uncharacterized protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Helicobacter pylori bacteriophage KHP30 (ファージ) / Helicobacter pylori bacteriophage KHP30 (ファージ) /  Helicobacter phage KHP (ファージ) Helicobacter phage KHP (ファージ) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.7 Å | |||||||||
 データ登録者 データ登録者 | Kamiya R / Uchiyama J | |||||||||
| 資金援助 |  日本, 2件 日本, 2件
| |||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2022 ジャーナル: Structure / 年: 2022タイトル: Acid-stable capsid structure of Helicobacter pylori bacteriophage KHP30 by single-particle cryoelectron microscopy. 著者: Ryosuke Kamiya / Jumpei Uchiyama / Shigenobu Matsuzaki / Kazuyoshi Murata / Kenji Iwasaki / Naoyuki Miyazaki /  要旨: The acid-stable capsid structures of Helicobacter pylori phages KHP30 and KHP40 are solved at 2.7 and 3.0 Å resolutions by cryoelectron microscopy, respectively. The capsids have icosahedral T = 9 ...The acid-stable capsid structures of Helicobacter pylori phages KHP30 and KHP40 are solved at 2.7 and 3.0 Å resolutions by cryoelectron microscopy, respectively. The capsids have icosahedral T = 9 symmetry and consist of each 540 copies of 2 structural proteins, a major capsid protein, and a cement protein. The major capsid proteins form 12 pentagonal capsomeres occupying icosahedral vertexes and 80 hexagonal capsomeres located at icosahedral faces and edges. The major capsid protein has a unique protruding loop extending to the neighboring subunit that stabilizes hexagonal capsomeres. Furthermore, the capsid is decorated with trimeric cement proteins with a jelly roll motif. The cement protein trimer sits on the quasi-three-fold axis formed by three major capsid protein capsomeres, thereby enhancing the particle stability by connecting these capsomeres. Sequence and structure comparisons between the related Helicobacter pylori phages suggest a possible mechanism of phage adaptation to the human gastric environment. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_30778.map.gz emd_30778.map.gz | 308 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-30778-v30.xml emd-30778-v30.xml emd-30778.xml emd-30778.xml | 13.7 KB 13.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
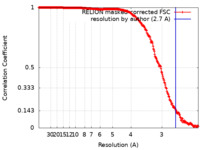
| FSC (解像度算出) |  emd_30778_fsc.xml emd_30778_fsc.xml | 26.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_30778.png emd_30778.png | 254.9 KB | ||
| Filedesc metadata |  emd-30778.cif.gz emd-30778.cif.gz | 5.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-30778 http://ftp.pdbj.org/pub/emdb/structures/EMD-30778 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-30778 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-30778 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_30778.map.gz / 形式: CCP4 / 大きさ: 1.6 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_30778.map.gz / 形式: CCP4 / 大きさ: 1.6 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.16 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Helicobacter phage KHP
| 全体 | 名称:  Helicobacter phage KHP (ファージ) Helicobacter phage KHP (ファージ) |
|---|---|
| 要素 |
|
-超分子 #1: Helicobacter phage KHP
| 超分子 | 名称: Helicobacter phage KHP / タイプ: virus / ID: 1 / 親要素: 0 / 含まれる分子: all / NCBI-ID: 1208236 / 生物種: Helicobacter phage KHP / ウイルスタイプ: VIRION / ウイルス・単離状態: OTHER / ウイルス・エンベロープ: No / ウイルス・中空状態: No |
|---|---|
| ウイルス殻 | Shell ID: 1 / 名称: Head / 直径: 700.0 Å / T番号(三角分割数): 9 |
-分子 #1: Major structural protein ORF14
| 分子 | 名称: Major structural protein ORF14 / タイプ: protein_or_peptide / ID: 1 / コピー数: 9 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Helicobacter pylori bacteriophage KHP30 (ファージ) Helicobacter pylori bacteriophage KHP30 (ファージ) |
| 分子量 | 理論値: 42.465922 KDa |
| 配列 | 文字列: MLEKLNNINF NNISNNLNLG IEVGREIQNA SWIKSPFFSI TGTGADRGVR LFSVASQQPF RPRIKAQLSG SGVSGNTDFE ANYDNLEIL SQTIYPDAFG NSLRSKIKAY SELERIDFIK ESVDSLTTWM NEERDKRIVA SLTNDFTNYL YTQTMNVATI R KAIFHARN ...文字列: MLEKLNNINF NNISNNLNLG IEVGREIQNA SWIKSPFFSI TGTGADRGVR LFSVASQQPF RPRIKAQLSG SGVSGNTDFE ANYDNLEIL SQTIYPDAFG NSLRSKIKAY SELERIDFIK ESVDSLTTWM NEERDKRIVA SLTNDFTNYL YTQTMNVATI R KAIFHARN GLKGDNSKAF PIKPIRATMQ SVGNVMVQNT SYIILLDSYQ ANQLKADSEF KELRKLYAFA GEDKGMLYSG LL GVIDNCP VIDAGVWNKF NVGMPNSSIS DSDFMRYLNK ANVSSIVTPR QFKEKLNQEK DEKKRSINKE ISIGCLIGAS AVL LAGSKE TRFYIDETVD AGRKSLVGVD CLLGVSKARY QSTDGVVTPY DNQDYAVIGL VSDME UniProtKB: Major structural protein ORF14 |
-分子 #2: Cement protein gp15
| 分子 | 名称: Cement protein gp15 / タイプ: protein_or_peptide / ID: 2 / コピー数: 9 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Helicobacter pylori bacteriophage KHP30 (ファージ) Helicobacter pylori bacteriophage KHP30 (ファージ) |
| 分子量 | 理論値: 13.721461 KDa |
| 配列 | 文字列: MKQKVHSVSY LAKAEFKFNN GVYNLVALPS GAEVVKVSLE VVGNPIATST TSVSVGFEDE TTKNYFLTLD NLAVDDASKK HTTSAKDYT ATSNKVVVAE VKNANDNNVK GVLRVLYFLP SVIEVEY UniProtKB: Uncharacterized protein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.2 |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON II (4k x 4k) 平均露光時間: 1.0 sec. / 平均電子線量: 20.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)