+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3033 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of PhnGHIJK complex by negative stain electron microscopy | |||||||||
 マップデータ マップデータ | 3D reconstruction of C-P lyase core complex including K subunit | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | phosphorus metabolism / carbon-phosphorous lyase / phosphonate / PhnG / PhnH / PhnI / PhnJ / PhnK | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / ネガティブ染色法 / 解像度: 16.0 Å | |||||||||
 データ登録者 データ登録者 | Seweryn P / Bich Van L / Kjeldgaard M / Russo CJ / Passmore LA / Hove-Jensen B / Jochimsen B / Brodersen DE | |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2015 ジャーナル: Nature / 年: 2015タイトル: Structural insights into the bacterial carbon-phosphorus lyase machinery. 著者: Paulina Seweryn / Lan Bich Van / Morten Kjeldgaard / Christopher J Russo / Lori A Passmore / Bjarne Hove-Jensen / Bjarne Jochimsen / Ditlev E Brodersen /   要旨: Phosphorus is required for all life and microorganisms can extract it from their environment through several metabolic pathways. When phosphate is in limited supply, some bacteria are able to use ...Phosphorus is required for all life and microorganisms can extract it from their environment through several metabolic pathways. When phosphate is in limited supply, some bacteria are able to use phosphonate compounds, which require specialized enzymatic machinery to break the stable carbon-phosphorus (C-P) bond. Despite its importance, the details of how this machinery catabolizes phosphonates remain unknown. Here we determine the crystal structure of the 240-kilodalton Escherichia coli C-P lyase core complex (PhnG-PhnH-PhnI-PhnJ; PhnGHIJ), and show that it is a two-fold symmetric hetero-octamer comprising an intertwined network of subunits with unexpected self-homologies. It contains two potential active sites that probably couple phosphonate compounds to ATP and subsequently hydrolyse the C-P bond. We map the binding site of PhnK on the complex using electron microscopy, and show that it binds to a conserved insertion domain of PhnJ. Our results provide a structural basis for understanding microbial phosphonate breakdown. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3033.map.gz emd_3033.map.gz | 253.2 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3033-v30.xml emd-3033-v30.xml emd-3033.xml emd-3033.xml | 12.4 KB 12.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
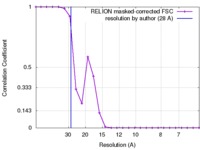
| FSC (解像度算出) |  emd_3033_fsc.xml emd_3033_fsc.xml | 2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  EMD-3033.png EMD-3033.png | 55 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3033 http://ftp.pdbj.org/pub/emdb/structures/EMD-3033 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3033 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3033 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3033_validation.pdf.gz emd_3033_validation.pdf.gz | 226.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3033_full_validation.pdf.gz emd_3033_full_validation.pdf.gz | 225.9 KB | 表示 | |
| XML形式データ |  emd_3033_validation.xml.gz emd_3033_validation.xml.gz | 6.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3033 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3033 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3033 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3033 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3033.map.gz / 形式: CCP4 / 大きさ: 670.9 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3033.map.gz / 形式: CCP4 / 大きさ: 670.9 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | 3D reconstruction of C-P lyase core complex including K subunit | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3.07 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Escherichia coli PhnGHIJK complex
| 全体 | 名称: Escherichia coli PhnGHIJK complex |
|---|---|
| 要素 |
|
-超分子 #1000: Escherichia coli PhnGHIJK complex
| 超分子 | 名称: Escherichia coli PhnGHIJK complex / タイプ: sample / ID: 1000 / Number unique components: 5 |
|---|---|
| 分子量 | 理論値: 268 KDa |
-分子 #1: PhnG
| 分子 | 名称: PhnG / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 集合状態: heterodimer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 21 KDa |
| 組換発現 | 生物種:  |
-分子 #2: PhnH
| 分子 | 名称: PhnH / タイプ: protein_or_peptide / ID: 2 / コピー数: 2 / 集合状態: heterodimer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 21 KDa |
| 組換発現 | 生物種:  |
-分子 #3: PhnI
| 分子 | 名称: PhnI / タイプ: protein_or_peptide / ID: 3 / コピー数: 2 / 集合状態: heterodimer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 39 KDa |
| 組換発現 | 生物種:  |
-分子 #4: PhnJ
| 分子 | 名称: PhnJ / タイプ: protein_or_peptide / ID: 4 / コピー数: 2 / 集合状態: heterodimer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 32 KDa |
| 組換発現 | 生物種:  |
-分子 #5: PhnK
| 分子 | 名称: PhnK / タイプ: protein_or_peptide / ID: 5 / コピー数: 2 / 集合状態: monomer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 28 KDa |
| 組換発現 | 生物種:  |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 染色 | タイプ: NEGATIVE 詳細: 3% ammonium molybdate pH 8.0 followed by 2% uranyl acetate |
|---|---|
| グリッド | 詳細: Quantifoil R2/2 holey carbon on copper mesh grids, covered with an additional thin film of amorphous carbon |
| 凍結 | 凍結剤: NONE / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI 12 |
|---|---|
| 日付 | 2013年7月26日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 実像数: 105 / 平均電子線量: 20 e/Å2 |
| 電子線 | 加速電圧: 120 kV / 電子線源: TUNGSTEN HAIRPIN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.974 µm / 最小 デフォーカス(公称値): 0.832 µm / 倍率(公称値): 44000 |
| 試料ステージ | 試料ホルダーモデル: SIDE ENTRY, EUCENTRIC |
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)