+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | MicroED structure of Proteinase K from xenon milled lamellae | |||||||||
 マップデータ マップデータ | Proteinase K structure from xenon milled lamellae | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Hydrolase | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報phosphorelay signal transduction system / regulation of DNA-templated transcription / DNA binding / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Parengyodontium album (菌類) Parengyodontium album (菌類) | |||||||||
| 手法 | 電子線結晶学 / クライオ電子顕微鏡法 / 解像度: 1.45 Å | |||||||||
 データ登録者 データ登録者 | Martynowycz MW / Shiriaeva A / Clabbers MTB / Nicolas WJ / Weaver SJ / Hattne J / Gonen T | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: A robust approach for MicroED sample preparation of lipidic cubic phase embedded membrane protein crystals. 著者: Michael W Martynowycz / Anna Shiriaeva / Max T B Clabbers / William J Nicolas / Sara J Weaver / Johan Hattne / Tamir Gonen /  要旨: Crystallizing G protein-coupled receptors (GPCRs) in lipidic cubic phase (LCP) often yields crystals suited for the cryogenic electron microscopy (cryoEM) method microcrystal electron diffraction ...Crystallizing G protein-coupled receptors (GPCRs) in lipidic cubic phase (LCP) often yields crystals suited for the cryogenic electron microscopy (cryoEM) method microcrystal electron diffraction (MicroED). However, sample preparation is challenging. Embedded crystals cannot be targeted topologically. Here, we use an integrated fluorescence light microscope (iFLM) inside of a focused ion beam and scanning electron microscope (FIB-SEM) to identify fluorescently labeled GPCR crystals. Crystals are targeted using the iFLM and LCP is milled using a plasma focused ion beam (pFIB). The optimal ion source for preparing biological lamellae is identified using standard crystals of proteinase K. Lamellae prepared using either argon or xenon produced the highest quality data and structures. MicroED data are collected from the milled lamellae and the structures are determined. This study outlines a robust approach to identify and mill membrane protein crystals for MicroED and demonstrates plasma ion-beam milling is a powerful tool for preparing biological lamellae. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_29588.map.gz emd_29588.map.gz | 11.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-29588-v30.xml emd-29588-v30.xml emd-29588.xml emd-29588.xml | 14.5 KB 14.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_29588.png emd_29588.png | 88.4 KB | ||
| Filedesc metadata |  emd-29588.cif.gz emd-29588.cif.gz | 5.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-29588 http://ftp.pdbj.org/pub/emdb/structures/EMD-29588 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29588 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29588 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_29588_validation.pdf.gz emd_29588_validation.pdf.gz | 621.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_29588_full_validation.pdf.gz emd_29588_full_validation.pdf.gz | 621.4 KB | 表示 | |
| XML形式データ |  emd_29588_validation.xml.gz emd_29588_validation.xml.gz | 4.2 KB | 表示 | |
| CIF形式データ |  emd_29588_validation.cif.gz emd_29588_validation.cif.gz | 4.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29588 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29588 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29588 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29588 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_29588.map.gz / 形式: CCP4 / 大きさ: 12.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_29588.map.gz / 形式: CCP4 / 大きさ: 12.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Proteinase K structure from xenon milled lamellae | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 これらの図は立方格子座標系で作成されたものです | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X: 0.34922 Å / Y: 0.34922 Å / Z: 0.35673 Å | ||||||||||||||||||||||||||||||||||||
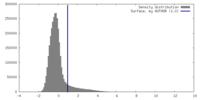
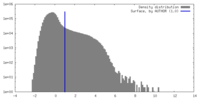
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 96 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Proteinase K
| 全体 | 名称: Proteinase K |
|---|---|
| 要素 |
|
-超分子 #1: Proteinase K
| 超分子 | 名称: Proteinase K / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Parengyodontium album (菌類) Parengyodontium album (菌類) |
| 分子量 | 理論値: 28.9 KDa |
-分子 #1: Proteinase K
| 分子 | 名称: Proteinase K / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO / EC番号: peptidase K |
|---|---|
| 由来(天然) | 生物種:  Parengyodontium album (菌類) Parengyodontium album (菌類) |
| 分子量 | 理論値: 28.958791 KDa |
| 配列 | 文字列: AAQTNAPWGL ARISSTSPGT STYYYDESAG QGSCVYVIDT GIEASHPEFE GRAQMVKTYY YSSRDGNGHG THCAGTVGSR TYGVAKKTQ LFGVKVLDDN GSGQYSTIIA GMDFVASDKN NRNCPKGVVA SLSLGGGYSS SVNSAAARLQ SSGVMVAVAA G NNNADARN ...文字列: AAQTNAPWGL ARISSTSPGT STYYYDESAG QGSCVYVIDT GIEASHPEFE GRAQMVKTYY YSSRDGNGHG THCAGTVGSR TYGVAKKTQ LFGVKVLDDN GSGQYSTIIA GMDFVASDKN NRNCPKGVVA SLSLGGGYSS SVNSAAARLQ SSGVMVAVAA G NNNADARN YSPASEPSVC TVGASDRYDR RSSFSNYGSV LDIFGPGTDI LSTWIGGSTR SISGTSMATP HVAGLAAYLM TL GKTTAAS ACRYIADTAN KGDLSNIPFG TVNLLAYNNY QA UniProtKB: Putative transcriptional regulator ToxR |
-分子 #2: NITRATE ION
| 分子 | 名称: NITRATE ION / タイプ: ligand / ID: 2 / コピー数: 2 / 式: NO3 |
|---|---|
| 分子量 | 理論値: 62.005 Da |
| Chemical component information |  ChemComp-NO3: |
-分子 #3: CALCIUM ION
| 分子 | 名称: CALCIUM ION / タイプ: ligand / ID: 3 / コピー数: 2 / 式: CA |
|---|---|
| 分子量 | 理論値: 40.078 Da |
-分子 #4: water
| 分子 | 名称: water / タイプ: ligand / ID: 4 / コピー数: 294 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 電子線結晶学 |
| 試料の集合状態 | 3D array |
- 試料調製
試料調製
| 濃度 | 5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| グリッド | モデル: Quantifoil R2/2 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 支持フィルム - Film thickness: 10 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 277 K / 装置: LEICA PLUNGER |
| 詳細 | Milled microcrystals |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 77.0 K / 最高: 90.0 K |
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) デジタル化 - サイズ - 横: 2048 pixel / デジタル化 - サイズ - 縦: 2048 pixel / 撮影したグリッド数: 1 / 実像数: 1 / 回折像の数: 840 / 平均露光時間: 0.5 sec. / 平均電子線量: 0.001 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 最小 デフォーカス(補正後): 0.0 µm / 照射モード: FLOOD BEAM / 撮影モード: DIFFRACTION / Cs: 2.7 mm / 最大 デフォーカス(公称値): 0.0 µm / 最小 デフォーカス(公称値): 0.0 µm / カメラ長: 1202 mm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN / 傾斜角度: -30.0, 30.0 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 詳細 | Binned by 2 |
|---|---|
| 最終 再構成 | アルゴリズム: FOURIER SPACE / 解像度のタイプ: BY AUTHOR / 解像度: 1.45 Å / 解像度の算出法: DIFFRACTION PATTERN/LAYERLINES |
| Merging software list | ソフトウェア - 名称: AIMLESS |
| Crystallography statistics | Number intensities measured: 569407 / Number structure factors: 64974 / Fourier space coverage: 87.58 / R sym: 0.073 / R merge: 0.236 / Overall phase error: 30 / Overall phase residual: 0 / Phase error rejection criteria: None / High resolution: 0.87 Å / 殻 - Shell ID: 1 / 殻 - High resolution: 0.87 Å / 殻 - Low resolution: 0.9 Å / 殻 - Number structure factors: 2783 / 殻 - Phase residual: 30 / 殻 - Fourier space coverage: 37.64 / 殻 - Multiplicity: 2.1 |
-原子モデル構築 1
| 精密化 | 空間: RECIPROCAL / プロトコル: AB INITIO MODEL / 温度因子: 12.65 / 当てはまり具合の基準: Maximum likelihood |
|---|---|
| 得られたモデル |  PDB-8fyp: |
 ムービー
ムービー コントローラー
コントローラー















 X (Sec.)
X (Sec.) Y (Row.)
Y (Row.) Z (Col.)
Z (Col.)