+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-23726 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | ATP-bound TnsC-TniQ complex from ShCAST system | |||||||||
 マップデータ マップデータ | local resolution filtered map | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Scytonema hofmannii (バクテリア) Scytonema hofmannii (バクテリア) | |||||||||
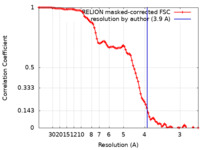
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.9 Å | |||||||||
 データ登録者 データ登録者 | Park J / Tsai AWL / Mehrotra E / Kellogg EH | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Science / 年: 2021 ジャーナル: Science / 年: 2021タイトル: Structural basis for target site selection in RNA-guided DNA transposition systems. 著者: Jung-Un Park / Amy Wei-Lun Tsai / Eshan Mehrotra / Michael T Petassi / Shan-Chi Hsieh / Ailong Ke / Joseph E Peters / Elizabeth H Kellogg /  要旨: CRISPR-associated transposition systems allow guide RNA-directed integration of a single DNA cargo in one orientation at a fixed distance from a programmable target sequence. We used cryo-electron ...CRISPR-associated transposition systems allow guide RNA-directed integration of a single DNA cargo in one orientation at a fixed distance from a programmable target sequence. We used cryo-electron microscopy (cryo-EM) to define the mechanism that underlies this process by characterizing the transposition regulator, TnsC, from a type V-K CRISPR-transposase system. In this scenario, polymerization of adenosine triphosphate-bound TnsC helical filaments could explain how polarity information is passed to the transposase. TniQ caps the TnsC filament, representing a universal mechanism for target information transfer in Tn7/Tn7-like elements. Transposase-driven disassembly establishes delivery of the element only to unused protospacers. Finally, TnsC transitions to define the fixed point of insertion, as revealed by structures with the transition state mimic ADP•AlF These mechanistic findings provide the underpinnings for engineering CRISPR-associated transposition systems for research and therapeutic applications. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_23726.map.gz emd_23726.map.gz | 1.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-23726-v30.xml emd-23726-v30.xml emd-23726.xml emd-23726.xml | 25.8 KB 25.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_23726_fsc.xml emd_23726_fsc.xml | 9.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_23726.png emd_23726.png | 70.5 KB | ||
| マスクデータ |  emd_23726_msk_1.map emd_23726_msk_1.map | 64 MB |  マスクマップ マスクマップ | |
| その他 |  emd_23726_additional_1.map.gz emd_23726_additional_1.map.gz emd_23726_additional_2.map.gz emd_23726_additional_2.map.gz emd_23726_half_map_1.map.gz emd_23726_half_map_1.map.gz emd_23726_half_map_2.map.gz emd_23726_half_map_2.map.gz | 49.7 MB 5.6 MB 49.7 MB 49.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-23726 http://ftp.pdbj.org/pub/emdb/structures/EMD-23726 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-23726 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-23726 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_23726_validation.pdf.gz emd_23726_validation.pdf.gz | 510.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_23726_full_validation.pdf.gz emd_23726_full_validation.pdf.gz | 509.7 KB | 表示 | |
| XML形式データ |  emd_23726_validation.xml.gz emd_23726_validation.xml.gz | 16 KB | 表示 | |
| CIF形式データ |  emd_23726_validation.cif.gz emd_23726_validation.cif.gz | 20.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23726 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23726 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23726 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23726 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_23726.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_23726.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | local resolution filtered map | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.33 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_23726_msk_1.map emd_23726_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
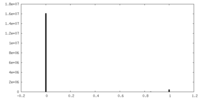
| 投影像・断面図 |
| ||||||||||||
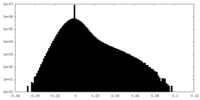
| 密度ヒストグラム |
-追加マップ: Full map
| ファイル | emd_23726_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Full map | ||||||||||||
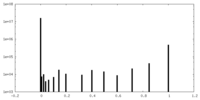
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: sharpened map using uniform B-factor
| ファイル | emd_23726_additional_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | sharpened map using uniform B-factor | ||||||||||||
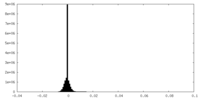
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: half map 1
| ファイル | emd_23726_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 1 | ||||||||||||
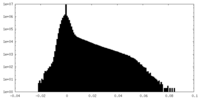
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: half map 2
| ファイル | emd_23726_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Helical filament of TnsC monomers bound to DNA and TniQ
| 全体 | 名称: Helical filament of TnsC monomers bound to DNA and TniQ |
|---|---|
| 要素 |
|
-超分子 #1: Helical filament of TnsC monomers bound to DNA and TniQ
| 超分子 | 名称: Helical filament of TnsC monomers bound to DNA and TniQ タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: Reconstituted with ATP |
|---|---|
| 由来(天然) | 生物種:  Scytonema hofmannii (バクテリア) Scytonema hofmannii (バクテリア) |
| 組換発現 | 生物種:  |
| 分子量 | 理論値: 400 KDa |
-分子 #1: TnsC
| 分子 | 名称: TnsC / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Scytonema hofmannii (バクテリア) Scytonema hofmannii (バクテリア) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MTEAQAIAKQ LGGVKPDDEW LQAEIARLKG KSIVPLQQVK TLHDWLDGKR KARKSCRVVG ESRTGKTVAC DAYRYRHKPQ QEAGRPPTVP VVYIRPHQKC GPKDLFKKIT EYLKYRVTKG TVSDFRDRTI EVLKGCGVEM LIIDEADRLK PETFADVRDI AEDLGIAVVL ...文字列: MTEAQAIAKQ LGGVKPDDEW LQAEIARLKG KSIVPLQQVK TLHDWLDGKR KARKSCRVVG ESRTGKTVAC DAYRYRHKPQ QEAGRPPTVP VVYIRPHQKC GPKDLFKKIT EYLKYRVTKG TVSDFRDRTI EVLKGCGVEM LIIDEADRLK PETFADVRDI AEDLGIAVVL VGTDRLDAVI KRDEQVLERF RAHLRFGKLS GEDFKNTVEM WEQMVLKLPV SSNLKSKEML RILTSATEGY IGRLDEILRE AAIRSLSRGL KKIDKAVLQE VAKEYK |
-分子 #2: TniQ
| 分子 | 名称: TniQ / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Scytonema hofmannii (バクテリア) Scytonema hofmannii (バクテリア) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MIEAPDVKPW LFLIKPYEGE SLSHFLGRFR RANHLSASGL GTLAGIGAIV ARWERFHFNP RPSQQELEAI ASVVEVAAQR LAQMLPPAGV GMQHEPIRLC GACYAESPCH RIEWQYKSVW KCDRHQLKIL AKCPNCQAPF KMPALWEDGC CHRCRMPFAE MAKLQKV |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1 mg/mL | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.4 構成要素:
| |||||||||||||||||||||
| グリッド | モデル: UltrAuFoil R2/2 / 材質: GOLD / メッシュ: 400 / 支持フィルム - 材質: GOLD / 支持フィルム - トポロジー: HOLEY / 支持フィルム - Film thickness: 50.0 nm / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.038 kPa | |||||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV / 詳細: Blot for 7 seconds before plunging. | |||||||||||||||||||||
| 詳細 | Excess of TniQ was added to ATP-bound TnsC filaments |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) デジタル化 - サイズ - 横: 5760 pixel / デジタル化 - サイズ - 縦: 4092 pixel / 撮影したグリッド数: 1 / 実像数: 4172 / 平均露光時間: 3.0 sec. / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 63000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | プロトコル: RIGID BODY FIT |
|---|---|
| 得られたモデル |  PDB-7n6i: |
 ムービー
ムービー コントローラー
コントローラー






















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)