+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | In vitro Nitrosopumilus maritimus S-layer with NH4Cl | |||||||||
 マップデータ マップデータ | PostProcessed map with B-factor sharpening | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Nmar_1547 S-layer / STRUCTURAL PROTEIN | |||||||||
| 機能・相同性 | membrane / Uncharacterized protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Nitrosopumilus maritimus SCM1 (古細菌) Nitrosopumilus maritimus SCM1 (古細菌) | |||||||||
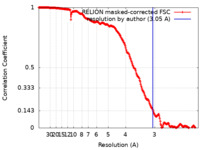
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.05 Å | |||||||||
 データ登録者 データ登録者 | von Kuegelgen A / van Dorst S / Bharat TAM | |||||||||
| 資金援助 |  英国, 2件 英国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2024 ジャーナル: Nature / 年: 2024タイトル: Membraneless channels sieve cations in ammonia-oxidizing marine archaea. 著者: Andriko von Kügelgen / C Keith Cassidy / Sofie van Dorst / Lennart L Pagani / Christopher Batters / Zephyr Ford / Jan Löwe / Vikram Alva / Phillip J Stansfeld / Tanmay A M Bharat /    要旨: Nitrosopumilus maritimus is an ammonia-oxidizing archaeon that is crucial to the global nitrogen cycle. A critical step for nitrogen oxidation is the entrapment of ammonium ions from a dilute marine ...Nitrosopumilus maritimus is an ammonia-oxidizing archaeon that is crucial to the global nitrogen cycle. A critical step for nitrogen oxidation is the entrapment of ammonium ions from a dilute marine environment at the cell surface and their subsequent channelling to the cell membrane of N. maritimus. Here we elucidate the structure of the molecular machinery responsible for this process, comprising the surface layer (S-layer), using electron cryotomography and subtomogram averaging from cells. We supplemented our in situ structure of the ammonium-binding S-layer array with a single-particle electron cryomicroscopy structure, revealing detailed features of this immunoglobulin-rich and glycan-decorated S-layer. Biochemical analyses showed strong ammonium binding by the cell surface, which was lost after S-layer disassembly. Sensitive bioinformatic analyses identified similar S-layers in many ammonia-oxidizing archaea, with conserved sequence and structural characteristics. Moreover, molecular simulations and structure determination of ammonium-enriched specimens enabled us to examine the cation-binding properties of the S-layer, revealing how it concentrates ammonium ions on its cell-facing side, effectively acting as a multichannel sieve on the cell membrane. This in situ structural study illuminates the biogeochemically essential process of ammonium binding and channelling, common to many marine microorganisms that are fundamental to the nitrogen cycle. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_16486.map.gz emd_16486.map.gz | 114 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-16486-v30.xml emd-16486-v30.xml emd-16486.xml emd-16486.xml | 26.2 KB 26.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_16486_fsc.xml emd_16486_fsc.xml | 22.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_16486.png emd_16486.png | 267.7 KB | ||
| マスクデータ |  emd_16486_msk_1.map emd_16486_msk_1.map | 125 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-16486.cif.gz emd-16486.cif.gz | 7.7 KB | ||
| その他 |  emd_16486_additional_1.map.gz emd_16486_additional_1.map.gz emd_16486_half_map_1.map.gz emd_16486_half_map_1.map.gz emd_16486_half_map_2.map.gz emd_16486_half_map_2.map.gz | 112 MB 113.9 MB 113.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-16486 http://ftp.pdbj.org/pub/emdb/structures/EMD-16486 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-16486 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-16486 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_16486_validation.pdf.gz emd_16486_validation.pdf.gz | 1.4 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_16486_full_validation.pdf.gz emd_16486_full_validation.pdf.gz | 1.4 MB | 表示 | |
| XML形式データ |  emd_16486_validation.xml.gz emd_16486_validation.xml.gz | 22.4 KB | 表示 | |
| CIF形式データ |  emd_16486_validation.cif.gz emd_16486_validation.cif.gz | 30.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16486 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16486 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16486 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-16486 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_16486.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_16486.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | PostProcessed map with B-factor sharpening | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.092 Å | ||||||||||||||||||||||||||||||||||||
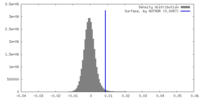
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_16486_msk_1.map emd_16486_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
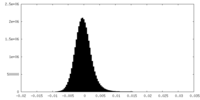
| 投影像・断面図 |
| ||||||||||||
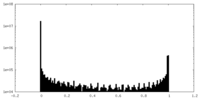
| 密度ヒストグラム |
-追加マップ: Refine3D main map without B-factor sharpening
| ファイル | emd_16486_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Refine3D main map without B-factor sharpening | ||||||||||||
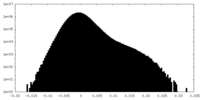
| 投影像・断面図 |
| ||||||||||||
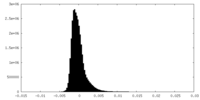
| 密度ヒストグラム |
-ハーフマップ: Half map 1
| ファイル | emd_16486_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map 1 | ||||||||||||
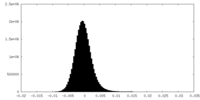
| 投影像・断面図 |
| ||||||||||||
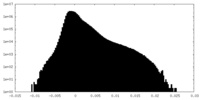
| 密度ヒストグラム |
-ハーフマップ: Half map 2
| ファイル | emd_16486_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map 2 | ||||||||||||
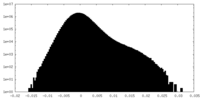
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Nitrosopumilus maritimus S-layer
| 全体 | 名称: Nitrosopumilus maritimus S-layer |
|---|---|
| 要素 |
|
-超分子 #1: Nitrosopumilus maritimus S-layer
| 超分子 | 名称: Nitrosopumilus maritimus S-layer / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: Nitrosopumilus maritimus S-layer C2 symmetrised |
|---|---|
| 由来(天然) | 生物種:  Nitrosopumilus maritimus SCM1 (古細菌) / 株: SCM1 / 細胞中の位置: extracellular Nitrosopumilus maritimus SCM1 (古細菌) / 株: SCM1 / 細胞中の位置: extracellular |
-分子 #1: In vitro Nitrosopumilus maritimus S-layer with increased NH4Cl - ...
| 分子 | 名称: In vitro Nitrosopumilus maritimus S-layer with increased NH4Cl - C2 symmetrised タイプ: protein_or_peptide / ID: 1 / 詳細: NH4Cl (ammonium chloride) / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Nitrosopumilus maritimus SCM1 (古細菌) / 株: SCM1 Nitrosopumilus maritimus SCM1 (古細菌) / 株: SCM1 |
| 配列 | 文字列: MNNEIGRKIT SLTLMTIMVA GGLTFAIPGV MPEAMAANAN LFVSAENSQF DNYMSGPQVI EVVVIDSDIN DTDEAKGEPD VTVNGKVLRM VQAVDGNWYG YFADRDQAQI ADSTATTADS GLDFGVFCAS SSGTAALGFS TTETDGIAIP ITIANATATG NGTQTGSSSG ...文字列: MNNEIGRKIT SLTLMTIMVA GGLTFAIPGV MPEAMAANAN LFVSAENSQF DNYMSGPQVI EVVVIDSDIN DTDEAKGEPD VTVNGKVLRM VQAVDGNWYG YFADRDQAQI ADSTATTADS GLDFGVFCAS SSGTAALGFS TTETDGIAIP ITIANATATG NGTQTGSSSG GAITTTCAAN TLDASTANGT INVVREAKDP VAASGSVSVG QIGLKNGTAN SGPNWPFIQL YELNPTGNVV VQYNKGGGVQ STTLTFDTVD QFAELSLDRT VFPRVSQVHA TITDLWLNID PTDEDSWTFA TNTKNTTSSF NVDTFYQVFD ENGASGGSAL TLRTTLSSLM CEDNCVLTLD VDAQSSGTPV VTIQDNGDSI LTQLNASSNT NANNASAFGI STETAKLGTG SIPVTITEQG PNSGVFGTYD ESDKSVLKIT DNAKRGTSAS LDYNETPQTI LVGFSFASID IQPVTDEWTS GQEIPVVIVD ADQNKNSRAD EDLDLNNPDV TLIPALRTGD PFTIDEGGTP SLIFTNGTNG DDSIFDTGAI NNTSAGQVGN FTLNINVTRF SSATNITSTE SIDTFSKRLI SAQTANSSAN FDVDFAIIDL GSATLETLKE TVVDEDNTAV GFNFFNYDVR SLGADTVSIA LLNTTGNILP WVNNDTRNVD KNNAILLVSN STNSQAYVDL TNAVSDAVYG STNTDSNVNI GFAMYFTGVG DLAAKEVIVM DFFSFGFTDD GVQSSERFAN QIIRIEAEET GDNTSTFEGS LEYVMVNQIN IQDAGTFSGI TPIADDPSFI VIEDLTDEDA PRVNYNDLGA DGVTTPVSDQ EEAPSHSGVV SLNADSYKIA DTVVITVEDL DLNVDSDLID IFTVVSDNSK ATDDAVGSAT TQSLSFGELG RLLDVTFDDV IWSTPDGANN TATGNDSDTC STELSNAGIT DTGLGATGFT LVETGAATGV FVGDFQIPSF WCRVSDTTTT PYTYAGDEET TTGLDIEVNY VDFRDASGEI VEVGDSAGVR ANTGSVSLDR TVYPVPFGTI ADSSKAANAA PNGRSVFPIH ATGITSTIDS TEELPTGDLT IHVRINDPDF DENPAGEDAM DQDNALKISV IRGSDSVVLG YAGASERTGK IDVGGNNGTI SNIRSFGEMD EIAPDAGIFE LDVNIKFTDG PASAQCNSHD TLYTALDGTT GKADTNRFDD GAASGQEYCI LQGDILQVEY TDPADASGDA NTVTDSATFD LRNGVLQSDK SVYIIGSDMI LTLIEPDFDL DNDSAETYDL DLIEWDSDAA TTTMGNKGVT GAAAAFDPEP TDFRETGDST GIFQIVIEIP ESLSNDKLER GEEIILEYTD WGPSGSDYVG DEDEDVNLTI YTSNFGATVE LDQKVYSWTD KVYITIVAPD HNFDSDLVDE IGETDSDPIK VSTRGFDLDN YKLVETGTDT GIFTGEVILT GFTAHDADGD GNTGDATGTT SGSGPTDGLL ATDDDDGLTV SFEFSEDETI VGSALIRWNI GEVQWLEASY PASGTGVVRV IDPDMNLDPE AVDNFEVDVW SDSDAGGIDL TVTETNEATG IFEGTVFFTT LDESSGHRLR VSEGDTVTAE YEDNTLPDPY TTADELDITA TSLIGTVVPP LERAPAANLR TVDAFGNSLD SVSVDQQVQI SADLANGQDR EQSFAYLVQI QDANGVTVSL AWITGSLSSG QSFSPALSWI PTEAGTYTAT AFVWESVDNP TALSPPVSTT VNVS UniProtKB: Uncharacterized protein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | 2D array |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 構成要素:
詳細: 50 mM HEPES/NaOH pH=7.5, 500 mM NaCl, 50 mM MgCl2, 10 mM CaCl2, 2.5 mM NHCl4 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER/RHODIUM / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 20 sec. / 前処理 - 雰囲気: AIR / 詳細: 15 mA | ||||||||||||||||||
| 凍結 | 凍結剤: NITROGEN / チャンバー内湿度: 100 % / チャンバー内温度: 283.15 K / 装置: FEI VITROBOT MARK IV 詳細: absorption for 60 sec and blotted for 5 sec with blot force -10. | ||||||||||||||||||
| 詳細 | In vitro isolate S-layer cell envelopes |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 70.0 K / 最高: 70.0 K |
| 特殊光学系 | 球面収差補正装置: not used / 色収差補正装置: not used / エネルギーフィルター - 名称: GIF Quantum LS / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) デジタル化 - サイズ - 横: 5760 pixel / デジタル化 - サイズ - 縦: 4092 pixel / 撮影したグリッド数: 3 / 実像数: 9435 / 平均露光時間: 4.2 sec. / 平均電子線量: 49.863 e/Å2 詳細: collected over two sessions, one session with the stage tilted by 30 deg |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 最大 デフォーカス(補正後): 5.0 µm / 最小 デフォーカス(補正後): 2.0 µm / 倍率(補正後): 81000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 5.0 µm / 最小 デフォーカス(公称値): 2.0 µm / 倍率(公称値): 81000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: RECIPROCAL / プロトコル: AB INITIO MODEL / 温度因子: 52.5 / 当てはまり具合の基準: Best Fit |
|---|
 ムービー
ムービー コントローラー
コントローラー
















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)