+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1566 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Activator bound RNA polymerase holoenzyme | |||||||||
 マップデータ マップデータ | Activator bound RNA polymerase holoenzyme | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | RNA polymerase / RNAP / Sigma 54 / PspF / transcription initiation / AAA ATPase / sigma factor | |||||||||
| 生物種 |   Klebsiella pneumoniae (肺炎桿菌) Klebsiella pneumoniae (肺炎桿菌) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 21.0 Å | |||||||||
 データ登録者 データ登録者 | Bose D / Pape T / Burrows PC / Rappas M / Wigneshweraraj SR / Buck M / Zhang X | |||||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2008 ジャーナル: Mol Cell / 年: 2008タイトル: Organization of an activator-bound RNA polymerase holoenzyme. 著者: Daniel Bose / Tillmann Pape / Patricia C Burrows / Mathieu Rappas / Siva R Wigneshweraraj / Martin Buck / Xiaodong Zhang /  要旨: Transcription initiation involves the conversion from closed promoter complexes, comprising RNA polymerase (RNAP) and double-stranded promoter DNA, to open complexes, in which the enzyme is able to ...Transcription initiation involves the conversion from closed promoter complexes, comprising RNA polymerase (RNAP) and double-stranded promoter DNA, to open complexes, in which the enzyme is able to access the DNA template in a single-stranded form. The complex between bacterial RNAP and its major variant sigma factor sigma(54) remains as a closed complex until ATP hydrolysis-dependent remodeling by activator proteins occurs. This remodeling facilitates DNA melting and allows the transition to the open complex. Here we present cryoelectron microscopy reconstructions of bacterial RNAP in complex with sigma(54) alone, and of RNAP-sigma(54) with an AAA+ activator. Together with photo-crosslinking data that establish the location of promoter DNA within the complexes, we explain why the RNAP-sigma(54) closed complex is unable to access the DNA template and propose how the structural changes induced by activator binding can initiate conformational changes that ultimately result in formation of the open complex. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1566.map.gz emd_1566.map.gz | 7.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1566-v30.xml emd-1566-v30.xml emd-1566.xml emd-1566.xml | 12 KB 12 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1566.gif 1566.gif | 31.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1566 http://ftp.pdbj.org/pub/emdb/structures/EMD-1566 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1566 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1566 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_1566_validation.pdf.gz emd_1566_validation.pdf.gz | 194.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_1566_full_validation.pdf.gz emd_1566_full_validation.pdf.gz | 193.4 KB | 表示 | |
| XML形式データ |  emd_1566_validation.xml.gz emd_1566_validation.xml.gz | 5.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1566 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1566 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1566 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1566 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1566.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1566.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Activator bound RNA polymerase holoenzyme | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.6 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
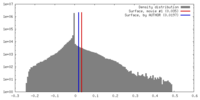
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Complex of E.coli RNA polymerase, Sigma 54 and PspF1-275 trapped ...
| 全体 | 名称: Complex of E.coli RNA polymerase, Sigma 54 and PspF1-275 trapped with ADP.AlFx |
|---|---|
| 要素 |
|
-超分子 #1000: Complex of E.coli RNA polymerase, Sigma 54 and PspF1-275 trapped ...
| 超分子 | 名称: Complex of E.coli RNA polymerase, Sigma 54 and PspF1-275 trapped with ADP.AlFx タイプ: sample / ID: 1000 / 詳細: All components are present on SDS-PAGE. 集合状態: monomer of RNAP sigma 54 holoenzyme bound to hexamer of PspF Number unique components: 3 |
|---|---|
| 分子量 | 理論値: 630 KDa |
-分子 #1: RNA polymerase
| 分子 | 名称: RNA polymerase / タイプ: protein_or_peptide / ID: 1 / Name.synonym: RNAP / コピー数: 1 / 集合状態: pentamer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 390 KDa |
| 組換発現 | 生物種:  |
-分子 #2: Sigma 54
| 分子 | 名称: Sigma 54 / タイプ: protein_or_peptide / ID: 2 / Name.synonym: s45 / コピー数: 1 / 集合状態: monomer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Klebsiella pneumoniae (肺炎桿菌) Klebsiella pneumoniae (肺炎桿菌) |
| 分子量 | 理論値: 54 KDa |
| 組換発現 | 生物種:  |
-分子 #3: Phage shock protein F
| 分子 | 名称: Phage shock protein F / タイプ: protein_or_peptide / ID: 3 / Name.synonym: PspF / コピー数: 1 / 集合状態: hexamer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 180 KDa |
| 組換発現 | 生物種:  |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 / 詳細: 10mM Tris-HCl pH8.0, 150mM NaCl, 10mM MgCl2, |
|---|---|
| グリッド | 詳細: Copper 400 mesh |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 83 K / 装置: OTHER / 詳細: Vitrification instrument: Vitrobot |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI/PHILIPS CM200FEG/UT |
|---|---|
| 温度 | 平均: 91 K |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM デジタル化 - スキャナー: NIKON SUPER COOLSCAN 9000 デジタル化 - サンプリング間隔: 6.35 µm / 実像数: 50 / 平均電子線量: 10 e/Å2 / Od range: 4.8 / ビット/ピクセル: 16 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 48700 / 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / Cs: 2.1 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 50000 |
| 試料ステージ | 試料ホルダー: eucentric / 試料ホルダーモデル: GATAN LIQUID NITROGEN |
- 画像解析
画像解析
| CTF補正 | 詳細: particles |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 21.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: Imagic V / 使用した粒子像数: 19581 |
| 最終 2次元分類 | クラス数: 695 |
-原子モデル構築 1
| 初期モデル | PDB ID: |
|---|---|
| ソフトウェア | 名称: Situs |
| 詳細 | Protocol: Rigid body. Structure positioned by hand and fitting refined in Situs |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 温度因子: 0.6 |
-原子モデル構築 2
| 初期モデル | PDB ID: |
|---|---|
| ソフトウェア | 名称: Situs |
| 詳細 | Protocol: Rigid body. Structure positioned by hand and fitting refined in Situs |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT |
 ムービー
ムービー コントローラー
コントローラー











 Y (Sec.)
Y (Sec.) X (Row.)
X (Row.) Z (Col.)
Z (Col.)