+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1411 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Interaction of decay-accelerating factor with coxsackievirus B3. | |||||||||
 マップデータ マップデータ | surface rendered coxsackievirus B3, M strain | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Coxsackievirus (コクサッキーウイルス) Coxsackievirus (コクサッキーウイルス) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / ネガティブ染色法 / 解像度: 27.0 Å | |||||||||
 データ登録者 データ登録者 | Hafenstein S | |||||||||
 引用 引用 |  ジャーナル: J Virol / 年: 2007 ジャーナル: J Virol / 年: 2007タイトル: Interaction of decay-accelerating factor with coxsackievirus B3. 著者: Susan Hafenstein / Valorie D Bowman / Paul R Chipman / Carol M Bator Kelly / Feng Lin / M Edward Medof / Michael G Rossmann /  要旨: Many entero-, parecho-, and rhinoviruses use immunoglobulin (Ig)-like receptors that bind into the viral canyon and are required to initiate viral uncoating during infection. However, some of these ...Many entero-, parecho-, and rhinoviruses use immunoglobulin (Ig)-like receptors that bind into the viral canyon and are required to initiate viral uncoating during infection. However, some of these viruses use an alternative or additional receptor that binds outside the canyon. Both the coxsackievirus-adenovirus receptor (CAR), an Ig-like molecule that binds into the viral canyon, and decay-accelerating factor (DAF) have been identified as cellular receptors for coxsackievirus B3 (CVB3). A cryoelectron microscopy reconstruction of a variant of CVB3 complexed with DAF shows full occupancy of the DAF receptor in each of 60 binding sites. The DAF molecule bridges the canyon, blocking the CAR binding site and causing the two receptors to compete with one another. The binding site of DAF on CVB3 differs from the binding site of DAF on the surface of echoviruses, suggesting independent evolutionary processes. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1411.map.gz emd_1411.map.gz | 8.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1411-v30.xml emd-1411-v30.xml emd-1411.xml emd-1411.xml | 9.7 KB 9.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1411.gif 1411.gif | 116.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1411 http://ftp.pdbj.org/pub/emdb/structures/EMD-1411 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1411 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1411 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_1411_validation.pdf.gz emd_1411_validation.pdf.gz | 217.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_1411_full_validation.pdf.gz emd_1411_full_validation.pdf.gz | 216.9 KB | 表示 | |
| XML形式データ |  emd_1411_validation.xml.gz emd_1411_validation.xml.gz | 6.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1411 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1411 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1411 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1411 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1411.map.gz / 形式: CCP4 / 大きさ: 22.1 MB / タイプ: IMAGE STORED AS SIGNED INTEGER (2 BYTES) ダウンロード / ファイル: emd_1411.map.gz / 形式: CCP4 / 大きさ: 22.1 MB / タイプ: IMAGE STORED AS SIGNED INTEGER (2 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | surface rendered coxsackievirus B3, M strain | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.22 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
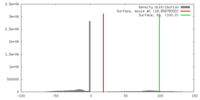
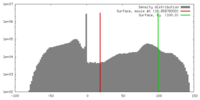
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : coxsackievirus B3, M strain
| 全体 | 名称: coxsackievirus B3, M strain |
|---|---|
| 要素 |
|
-超分子 #1000: coxsackievirus B3, M strain
| 超分子 | 名称: coxsackievirus B3, M strain / タイプ: sample / ID: 1000 / Number unique components: 1 |
|---|
-超分子 #1: Coxsackievirus
| 超分子 | 名称: Coxsackievirus / タイプ: virus / ID: 1 / Name.synonym: cvb3 / 詳細: Native virus control / NCBI-ID: 12066 / 生物種: Coxsackievirus / ウイルスタイプ: VIRION / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: No / ウイルス・中空状態: No / Syn species name: cvb3 |
|---|---|
| 宿主 | 生物種:  Homo sapiens (ヒト) / 別称: VERTEBRATES Homo sapiens (ヒト) / 別称: VERTEBRATES |
| 分子量 | 実験値: 7.0 MDa / 理論値: 7.0 MDa |
| ウイルス殻 | Shell ID: 1 / 名称: VP1 / 直径: 300 Å / T番号(三角分割数): 1 |
| ウイルス殻 | Shell ID: 2 / 名称: VP2 / 直径: 300 Å / T番号(三角分割数): 1 |
| ウイルス殻 | Shell ID: 3 / 名称: VP3 / 直径: 300 Å / T番号(三角分割数): 1 |
-実験情報
-構造解析
| 手法 | ネガティブ染色法, クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL |
|---|---|
| 緩衝液 | pH: 6 / 詳細: 50mM MES, pH 6.0 |
| 染色 | タイプ: NEGATIVE / 詳細: small aliquotes were applied to grids and vitrified |
| 凍結 | 凍結剤: ETHANE / チャンバー内温度: 120 K / 装置: HOMEMADE PLUNGER / 詳細: Vitrification instrument: plunger / 手法: blot before plunging |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI/PHILIPS CM300FEG/T |
|---|---|
| 温度 | 最低: 83 K / 最高: 83 K / 平均: 93 K |
| アライメント法 | Legacy - 非点収差: lens astigmatism was corrected at 98,000 times mag |
| 日付 | 2000年8月23日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: ZEISS SCAI / デジタル化 - サンプリング間隔: 7 µm / 実像数: 9 / 平均電子線量: 37 e/Å2 / 詳細: scanned at 7 microns and bin averaged to 14 / Od range: 0.9 / ビット/ピクセル: 8 |
| Tilt angle min | 0 |
| Tilt angle max | 0 |
| 電子線 | 加速電圧: 300 kV / 電子線源: TUNGSTEN HAIRPIN |
| 電子光学系 | 倍率(補正後): 63100 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm / 最大 デフォーカス(公称値): 3.5 µm / 最小 デフォーカス(公称値): 0.7 µm / 倍率(公称値): 61000 |
| 試料ステージ | 試料ホルダー: side mounted nitrogen cooled / 試料ホルダーモデル: GATAN LIQUID NITROGEN |
- 画像解析
画像解析
| CTF補正 | 詳細: robem |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: I (正20面体型対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 27.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: EMPFT, EM3DR / 使用した粒子像数: 600 |
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera












 Z (Sec.)
Z (Sec.) X (Row.)
X (Row.) Y (Col.)
Y (Col.)