+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1280 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-electron microscopy study of bacteriophage T4 displaying anthrax toxin proteins. | |||||||||
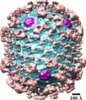
 マップデータ マップデータ | Bacteriophage T4 capsid decorated with anthrax toxin proteins. N-terminal domain of the anhrax lethal factor (nLF) was fused with T4 Soc protein. nLF-Soc molecules were attached to the surface of Hoc-minus Soc-minus T4 phage mutant. Then the anthrax protective antigen, PA63, heptamers were attached to the capsid-exposed LFn domains. | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |   Enterobacteria phage T4 (ファージ) Enterobacteria phage T4 (ファージ) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 35.0 Å | |||||||||
 データ登録者 データ登録者 | Fokine A / Bowman VD / Battisti AJ / Li Q / Chipman PR / Rao VB / Rossmann MG | |||||||||
 引用 引用 |  ジャーナル: Virology / 年: 2007 ジャーナル: Virology / 年: 2007タイトル: Cryo-electron microscopy study of bacteriophage T4 displaying anthrax toxin proteins. 著者: Andrei Fokine / Valorie D Bowman / Anthony J Battisti / Qin Li / Paul R Chipman / Venigalla B Rao / Michael G Rossmann /  要旨: The bacteriophage T4 capsid contains two accessory surface proteins, the small outer capsid protein (Soc, 870 copies) and the highly antigenic outer capsid protein (Hoc, 155 copies). As these are ...The bacteriophage T4 capsid contains two accessory surface proteins, the small outer capsid protein (Soc, 870 copies) and the highly antigenic outer capsid protein (Hoc, 155 copies). As these are dispensable for capsid formation, they can be used for displaying proteins and macromolecular complexes on the T4 capsid surface. Anthrax toxin components were attached to the T4 capsid as a fusion protein of the N-terminal domain of the anthrax lethal factor (LFn) with Soc. The LFn-Soc fusion protein was complexed in vitro with Hoc(-)Soc(-)T4 phage. Subsequently, cleaved anthrax protective antigen heptamers (PA63)(7) were attached to the exposed LFn domains. A cryo-electron microscopy study of the decorated T4 particles shows the complex of PA63 heptamers with LFn-Soc on the phage surface. Although the cryo-electron microscopy reconstruction is unable to differentiate on its own between different proposed models of the anthrax toxin, the density is consistent with a model that had predicted the orientation and position of three LFn molecules bound to one PA63 heptamer. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1280.map.gz emd_1280.map.gz | 19.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1280-v30.xml emd-1280-v30.xml emd-1280.xml emd-1280.xml | 10.9 KB 10.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1280.gif 1280.gif | 148.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1280 http://ftp.pdbj.org/pub/emdb/structures/EMD-1280 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1280 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1280 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_1280_validation.pdf.gz emd_1280_validation.pdf.gz | 239.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_1280_full_validation.pdf.gz emd_1280_full_validation.pdf.gz | 238.9 KB | 表示 | |
| XML形式データ |  emd_1280_validation.xml.gz emd_1280_validation.xml.gz | 6.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1280 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1280 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1280 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1280 | HTTPS FTP |
-関連構造データ
| 類似構造データ |
|---|
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1280.map.gz / 形式: CCP4 / 大きさ: 78.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1280.map.gz / 形式: CCP4 / 大きさ: 78.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Bacteriophage T4 capsid decorated with anthrax toxin proteins. N-terminal domain of the anhrax lethal factor (nLF) was fused with T4 Soc protein. nLF-Soc molecules were attached to the surface of Hoc-minus Soc-minus T4 phage mutant. Then the anthrax protective antigen, PA63, heptamers were attached to the capsid-exposed LFn domains. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 5.96 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Bacteriophage T4 decorated with anthrax toxin proteins
| 全体 | 名称: Bacteriophage T4 decorated with anthrax toxin proteins |
|---|---|
| 要素 |
|
-超分子 #1000: Bacteriophage T4 decorated with anthrax toxin proteins
| 超分子 | 名称: Bacteriophage T4 decorated with anthrax toxin proteins タイプ: sample / ID: 1000 詳細: Bacteriophage T4 decorated with anthrax toxin proteins. N-terminal domain of the anhrax lethal factor (nLF) was fused with T4 Soc protein. nLF-Soc molecules were attached to the surface of ...詳細: Bacteriophage T4 decorated with anthrax toxin proteins. N-terminal domain of the anhrax lethal factor (nLF) was fused with T4 Soc protein. nLF-Soc molecules were attached to the surface of Hoc-minus Soc-minus T4 phage mutant. Then the anthrax protective antigen, PA63, heptamers were attached to the capsid-exposed LFn domains. Number unique components: 3 |
|---|
-超分子 #1: Enterobacteria phage T4
| 超分子 | 名称: Enterobacteria phage T4 / タイプ: virus / ID: 1 / NCBI-ID: 10665 / 生物種: Enterobacteria phage T4 / ウイルスタイプ: VIRION / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: No / ウイルス・中空状態: No |
|---|---|
| 宿主 | 生物種: |
| ウイルス殻 | Shell ID: 1 / 名称: capsid shell / 直径: 1200 Å / T番号(三角分割数): 20 |
| ウイルス殻 | Shell ID: 2 / 直径: 850 Å / T番号(三角分割数): 13 |
-分子 #1: LFn-Soc fusion protein
| 分子 | 名称: LFn-Soc fusion protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 700 / 集合状態: monomer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #2: anthrax PA63
| 分子 | 名称: anthrax PA63 / タイプ: protein_or_peptide / ID: 2 / コピー数: 700 / 集合状態: heptamer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 40 % / 装置: HOMEMADE PLUNGER / 詳細: Vitrification instrument: in house manufactured / 手法: hand blot 3 seconds, plunging during blot |
|---|
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI/PHILIPS CM300FEG/T |
|---|---|
| アライメント法 | Legacy - 非点収差: live fft at 190,000x |
| 日付 | 2006年2月12日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: ZEISS SCAI / デジタル化 - サンプリング間隔: 7 µm / 実像数: 50 / 平均電子線量: 20 e/Å2 / ビット/ピクセル: 8 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 47000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.7 µm / 最小 デフォーカス(公称値): 1.1 µm / 倍率(公称値): 45000 |
| 試料ステージ | 試料ホルダーモデル: GATAN LIQUID NITROGEN |
- 画像解析
画像解析
| CTF補正 | 詳細: Each particle |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C5 (5回回転対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 35.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: Spider 詳細: The reconstruction was performed imposing D5 symmetry 使用した粒子像数: 722 |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)





















