+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-12273 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the human FERRY complex | |||||||||
 マップデータ マップデータ | Cryo-EM structure of the FERRY complex core | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Human FERRY complex / Five-subunit Early endosome RNA and Ribosome intermediarY complex / Intracellular RNA transport / Early Endosome-associated transport of RNA / RNA BINDING PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報quinone metabolic process / glyoxalase III activity / quinone reductase (NADPH) activity / methylglyoxal catabolic process to D-lactate via S-lactoyl-glutathione / 酸化還元酵素 / NADP binding / early endosome / RNA binding / extracellular exosome / identical protein binding ...quinone metabolic process / glyoxalase III activity / quinone reductase (NADPH) activity / methylglyoxal catabolic process to D-lactate via S-lactoyl-glutathione / 酸化還元酵素 / NADP binding / early endosome / RNA binding / extracellular exosome / identical protein binding / membrane / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.0 Å | |||||||||
 データ登録者 データ登録者 | Quentin D / Klink BU / Raunser S | |||||||||
| 資金援助 | 1件
| |||||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2023 ジャーナル: Mol Cell / 年: 2023タイトル: Structural basis of mRNA binding by the human FERRY Rab5 effector complex. 著者: Dennis Quentin / Jan S Schuhmacher / Björn U Klink / Jeni Lauer / Tanvir R Shaikh / Pim J Huis In 't Veld / Luisa M Welp / Henning Urlaub / Marino Zerial / Stefan Raunser /  要旨: The pentameric FERRY Rab5 effector complex is a molecular link between mRNA and early endosomes in mRNA intracellular distribution. Here, we determine the cryo-EM structure of human FERRY. It reveals ...The pentameric FERRY Rab5 effector complex is a molecular link between mRNA and early endosomes in mRNA intracellular distribution. Here, we determine the cryo-EM structure of human FERRY. It reveals a unique clamp-like architecture that bears no resemblance to any known structure of Rab effectors. A combination of functional and mutational studies reveals that while the Fy-2 C-terminal coiled-coil acts as binding region for Fy-1/3 and Rab5, both coiled-coils and Fy-5 concur to bind mRNA. Mutations causing truncations of Fy-2 in patients with neurological disorders impair Rab5 binding or FERRY complex assembly. Thus, Fy-2 serves as a binding hub connecting all five complex subunits and mediating the binding to mRNA and early endosomes via Rab5. Our study provides mechanistic insights into long-distance mRNA transport and demonstrates that the particular architecture of FERRY is closely linked to a previously undescribed mode of RNA binding, involving coiled-coil domains. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_12273.map.gz emd_12273.map.gz | 4.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-12273-v30.xml emd-12273-v30.xml emd-12273.xml emd-12273.xml | 21.5 KB 21.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_12273.png emd_12273.png | 106.3 KB | ||
| Filedesc metadata |  emd-12273.cif.gz emd-12273.cif.gz | 7.5 KB | ||
| その他 |  emd_12273_additional_1.map.gz emd_12273_additional_1.map.gz | 66.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-12273 http://ftp.pdbj.org/pub/emdb/structures/EMD-12273 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12273 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12273 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_12273_validation.pdf.gz emd_12273_validation.pdf.gz | 346.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_12273_full_validation.pdf.gz emd_12273_full_validation.pdf.gz | 345.7 KB | 表示 | |
| XML形式データ |  emd_12273_validation.xml.gz emd_12273_validation.xml.gz | 6 KB | 表示 | |
| CIF形式データ |  emd_12273_validation.cif.gz emd_12273_validation.cif.gz | 6.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12273 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12273 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12273 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12273 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_12273.map.gz / 形式: CCP4 / 大きさ: 70.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_12273.map.gz / 形式: CCP4 / 大きさ: 70.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Cryo-EM structure of the FERRY complex core | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.08 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
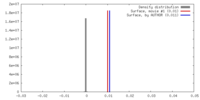
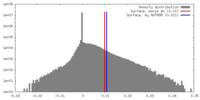
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-追加マップ: L-AFTER filtered Cryo-EM density map of the FERRY complex core
| ファイル | emd_12273_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | L-AFTER filtered Cryo-EM density map of the FERRY complex core | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
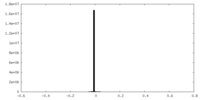
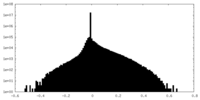
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Human FERRY (Five-subunit Early endosome RNA and Ribosome interme...
| 全体 | 名称: Human FERRY (Five-subunit Early endosome RNA and Ribosome intermediarY) complex |
|---|---|
| 要素 |
|
-超分子 #1: Human FERRY (Five-subunit Early endosome RNA and Ribosome interme...
| 超分子 | 名称: Human FERRY (Five-subunit Early endosome RNA and Ribosome intermediarY) complex タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|
-超分子 #2: Protein phosphatase 1 regulatory subunit 21
| 超分子 | 名称: Protein phosphatase 1 regulatory subunit 21 / タイプ: complex / ID: 2 / 親要素: 1 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-超分子 #3: Quinone oxidoreductase-like protein 1
| 超分子 | 名称: Quinone oxidoreductase-like protein 1 / タイプ: complex / ID: 3 / 親要素: 1 / 含まれる分子: #2 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-超分子 #4: Glutamine amidotransferase-like class 1 domain-containing protein 1
| 超分子 | 名称: Glutamine amidotransferase-like class 1 domain-containing protein 1 タイプ: complex / ID: 4 / 親要素: 1 / 含まれる分子: #3 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Protein phosphatase 1 regulatory subunit 21
| 分子 | 名称: Protein phosphatase 1 regulatory subunit 21 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 88.782836 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MAAAMASAEL QGKYQKLAQE YSKLRAQNQV LKKGVVDEQA NSAALKEQLK MKDQSLRKLQ QEMDSLTFRN LQLAKRVELL QDELALSEP RGKKNKKSGE SSSQLSQEQK SVFDEDLQKK IEENERLHIQ FFEADEQHKH VEAELRSRLA TLETEAAQHQ A VVDGLTRK ...文字列: MAAAMASAEL QGKYQKLAQE YSKLRAQNQV LKKGVVDEQA NSAALKEQLK MKDQSLRKLQ QEMDSLTFRN LQLAKRVELL QDELALSEP RGKKNKKSGE SSSQLSQEQK SVFDEDLQKK IEENERLHIQ FFEADEQHKH VEAELRSRLA TLETEAAQHQ A VVDGLTRK YMETIEKLQN DKAKLEVKSQ TLEKEAKECR LRTEECQLQL KTLHEDLSGR LEESLSIINE KVPFNDTKYS QY NALNVPL HNRRHQLKMR DIAGQALAFV QDLVTALLNF HTYTEQRIQI FPVDSAIDTI SPLNQKFSQY LHENASYVRP LEE GMLHLF ESITEDTVTV LETTVKLKTF SEHLTSYICF LRKILPYQLK SLEEECESSL CTSALRARNL ELSQDMKKMT AVFE KLQTY IALLALPSTE PDGLLRTNYS SVLTNVGAAL HGFHDVMKDI SKHYSQKAAI EHELPTATQK LITTNDCILS SVVAL TNGA GKIASFFSNN LDYFIASLSY GPKAASGFIS PLSAECMLQY KKKAAAYMKS LRKPLLESVP YEEALANRRI LLSSTE SRE GLAQQVQQSL EKISKLEQEK EHWMLEAQLA KIKLEKENQR IADKLKNTGS AQLVGLAQEN AAVSNTAGQD EATAKAV LE PIQSTSLIGT LTRTSDSEVP DVESREDLIK NHYMARIVEL TSQLQLADSK SVHFYAECRA LSKRLALAEK SKEALTEE M KLASQNISRL QDELTTTKRS YEDQLSMMSD HLCSMNETLS KQREEIDTLK MSSKGNSKKN KSR UniProtKB: Protein phosphatase 1 regulatory subunit 21 |
-分子 #2: Quinone oxidoreductase-like protein 1
| 分子 | 名称: Quinone oxidoreductase-like protein 1 / タイプ: protein_or_peptide / ID: 2 / 詳細: N-terminal His-6 tag / コピー数: 2 / 光学異性体: LEVO / EC番号: 酸化還元酵素 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 39.661414 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSHHHHHHKG LYFQQSSTDE EITFVFQEKE DLPVTEDNFV KLQVKACALS QINTKLLAEM KMKKDLFPVG REIAGIVLDV GSKVSFFQP DDEVVGILPL DSEDPGLCEV VRVHEHYLVH KPEKVTWTEA AGSIRDGVRA YTALHYLSHL SPGKSVLIMD G ASAFGTIA ...文字列: MSHHHHHHKG LYFQQSSTDE EITFVFQEKE DLPVTEDNFV KLQVKACALS QINTKLLAEM KMKKDLFPVG REIAGIVLDV GSKVSFFQP DDEVVGILPL DSEDPGLCEV VRVHEHYLVH KPEKVTWTEA AGSIRDGVRA YTALHYLSHL SPGKSVLIMD G ASAFGTIA IQLAHHRGAK VISTACSLED KQCLERFRPP IARVIDVSNG KVHVAESCLE ETGGLGVDIV LDAGVRLYSK DD EPAVKLQ LLPHKHDIIT LLGVGGHWVT TEENLQLDPP DSHCLFLKGA TLAFLNDEVW NLSNVQQGKY LCILKDVMEK LST GVFRPQ LDEPIPLYEA KVSMEAVQKN QGRKKQVVQF UniProtKB: Quinone oxidoreductase-like protein 1 |
-分子 #3: Glutamine amidotransferase-like class 1 domain-containing protein 1
| 分子 | 名称: Glutamine amidotransferase-like class 1 domain-containing protein 1 タイプ: protein_or_peptide / ID: 3 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 24.237488 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSHHHHHHAS ERLPNRPACL LVASGAAEGV SAQSFLHCFT MASTAFNLQV ATPGGKAMEF VDVTESNARW VQDFRLKAYA SPAKLESID GARYHALLIP SCPGALTDLA SSGSLARILQ HFHSESKPIC AVGHGVAALC CATNEDRSWV FDSYSLTGPS V CELVRAPG ...文字列: MSHHHHHHAS ERLPNRPACL LVASGAAEGV SAQSFLHCFT MASTAFNLQV ATPGGKAMEF VDVTESNARW VQDFRLKAYA SPAKLESID GARYHALLIP SCPGALTDLA SSGSLARILQ HFHSESKPIC AVGHGVAALC CATNEDRSWV FDSYSLTGPS V CELVRAPG FARLPLVVED FVKDSGACFS ASEPDAVHVV LDRHLVTGQN ASSTVPAVQN LLFLCGSRK UniProtKB: Glutamine amidotransferase-like class 1 domain-containing protein 1 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.7 mg/mL | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| ||||||||||
| グリッド | モデル: UltrAuFoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 40 sec. / 前処理 - 雰囲気: AIR | ||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 286 K / 装置: FEI VITROBOT MARK III / 詳細: 3s blotting time. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 実像数: 1879 / 平均露光時間: 15.0 sec. / 平均電子線量: 75.8 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 最大 デフォーカス(補正後): 2.8000000000000003 µm 最小 デフォーカス(補正後): 1.6 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 詳細 | To build the model for the (CRYZL1)2(PPP1r21)2(GATD1)4 core of the FERRY complex, the obtained crystal structures of CRYZL1 and GATD1 were initially fitted into the corresponding density using the rigid body fitting tool in Chimera. trRosetta, a de novo protein structure prediction algorithm that is based on direct energy minimization with restrained Rosetta, was used to obtain initial models for PPP1r21. The predicted model for the 6-helix bundle domain, containing residues 246 to 498, that matched our experimental density best was subsequently fitted similar as CRYZL1 and GATD1 using rigid body fit. Manual model building for the regions N- and C-terminal 6-helix bundle, which comprise residues 218 to 245 and 499 to 552, respectively, was further guided by secondary structure predictions of individual trRosetta runs for these regions, that include the vertical helix as well as the beginning of the two terminal coiled-coils of PPP1r21. With the resulting combined model, containing residues 2 to 349, 218 to 552 and 8 to 217 of CRYZL1, PPP1r21 and GATD1, respectively, a restrained refinement in PHENIX was performed. In the next step, the model was further refined using a combination of manual building in COOT and real-space refinement in PHENIX. |
|---|---|
| 得られたモデル |  PDB-7nd2: |
 ムービー
ムービー コントローラー
コントローラー


















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)