+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0409 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Single-particle cryo-EM reconstruction of the catalytic subunit of protein kinase A bound to ATP and IP20 using 200 keV | |||||||||
 マップデータ マップデータ | Single-particle cryo-EM reconstruction of the catalytic subunit of protein kinase A bound to ATP and IP20 (unsharpened) | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  | |||||||||
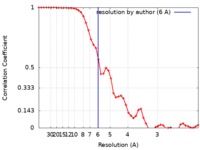
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 6.0 Å | |||||||||
 データ登録者 データ登録者 | Herzik Jr MA / Wu M / Lander GC | |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2019 ジャーナル: Nat Commun / 年: 2019タイトル: High-resolution structure determination of sub-100 kDa complexes using conventional cryo-EM. 著者: Mark A Herzik / Mengyu Wu / Gabriel C Lander /  要旨: Determining high-resolution structures of biological macromolecules amassing less than 100 kilodaltons (kDa) has been a longstanding goal of the cryo-electron microscopy (cryo-EM) community. While ...Determining high-resolution structures of biological macromolecules amassing less than 100 kilodaltons (kDa) has been a longstanding goal of the cryo-electron microscopy (cryo-EM) community. While the Volta phase plate has enabled visualization of specimens in this size range, this instrumentation is not yet fully automated and can present technical challenges. Here, we show that conventional defocus-based cryo-EM methodologies can be used to determine high-resolution structures of specimens amassing less than 100 kDa using a transmission electron microscope operating at 200 keV coupled with a direct electron detector. Our ~2.7 Å structure of alcohol dehydrogenase (82 kDa) proves that bound ligands can be resolved with high fidelity to enable investigation of drug-target interactions. Our ~2.8 Å and ~3.2 Å structures of methemoglobin demonstrate that distinct conformational states can be identified within a dataset for proteins as small as 64 kDa. Furthermore, we provide the sub-nanometer cryo-EM structure of a sub-50 kDa protein. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0409.map.gz emd_0409.map.gz | 6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0409-v30.xml emd-0409-v30.xml emd-0409.xml emd-0409.xml | 21.2 KB 21.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_0409_fsc.xml emd_0409_fsc.xml | 5.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_0409.png emd_0409.png | 35.8 KB | ||
| その他 |  emd_0409_additional.map.gz emd_0409_additional.map.gz emd_0409_half_map_1.map.gz emd_0409_half_map_1.map.gz emd_0409_half_map_2.map.gz emd_0409_half_map_2.map.gz | 7.4 MB 6 MB 6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0409 http://ftp.pdbj.org/pub/emdb/structures/EMD-0409 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0409 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0409 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_0409_validation.pdf.gz emd_0409_validation.pdf.gz | 78.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_0409_full_validation.pdf.gz emd_0409_full_validation.pdf.gz | 77.9 KB | 表示 | |
| XML形式データ |  emd_0409_validation.xml.gz emd_0409_validation.xml.gz | 494 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0409 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0409 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0409 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0409 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  0406C  0407C  0408C  6nbbC  6nbcC  6nbdC C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10252 (タイトル: Catalytic subunit of protein kinase A bound to ATP, manganese, and IP20 movies obtained using Talos Arctica operating at 200 kV equipped with a K2 EMPIAR-10252 (タイトル: Catalytic subunit of protein kinase A bound to ATP, manganese, and IP20 movies obtained using Talos Arctica operating at 200 kV equipped with a K2Data size: 5.5 TB Data #1: Raw, unaligned movie stacks of the catalytic subunit of protein kinase A bound to ATP, manganese, and IP20 acquired on a Talos Arctica using a K2 direct electron detector [micrographs - multiframe]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0409.map.gz / 形式: CCP4 / 大きさ: 8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0409.map.gz / 形式: CCP4 / 大きさ: 8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Single-particle cryo-EM reconstruction of the catalytic subunit of protein kinase A bound to ATP and IP20 (unsharpened) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.1172 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
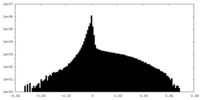
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-追加マップ: Single-particle cryo-EM reconstruction of the catalytic subunit of...
| ファイル | emd_0409_additional.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Single-particle cryo-EM reconstruction of the catalytic subunit of protein kinase A bound to ATP and IP20 (sharpened) | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Odd half map
| ファイル | emd_0409_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Odd half map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Even half map
| ファイル | emd_0409_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Even half map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : catalytic subunit of mouse protein kinase A bound to ATP and IP20
| 全体 | 名称: catalytic subunit of mouse protein kinase A bound to ATP and IP20 |
|---|---|
| 要素 |
|
-超分子 #1: catalytic subunit of mouse protein kinase A bound to ATP and IP20
| 超分子 | 名称: catalytic subunit of mouse protein kinase A bound to ATP and IP20 タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 分子量 | 理論値: 43 KDa |
-分子 #1: catalytic subunit of protein kinase A
| 分子 | 名称: catalytic subunit of protein kinase A / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO / EC番号: non-specific serine/threonine protein kinase |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: GNAAAAKKGS EQESVKEFLA KAKEDFLKKW ETPSQNTAQL DQFDRIKTLG TGSFGRVMLV KHKESGNHYA MKILDKQKVV KLKQIEHTL NEKRILQAVN FPFLVKLEFS FKDNSNLYMV MEYVAGGEMF SHLRRIGRFS EPHARFYAAQ IVLTFEYLHS L DLIYRDLK ...文字列: GNAAAAKKGS EQESVKEFLA KAKEDFLKKW ETPSQNTAQL DQFDRIKTLG TGSFGRVMLV KHKESGNHYA MKILDKQKVV KLKQIEHTL NEKRILQAVN FPFLVKLEFS FKDNSNLYMV MEYVAGGEMF SHLRRIGRFS EPHARFYAAQ IVLTFEYLHS L DLIYRDLK PENLLIDQQG YIQVTDFGFA KRVKGRTWTL CGTPEYLAPE IILSKGYNKA VDWWALGVLI YEMAAGYPPF FA DQPIQIY EKIVSGKVRF PSHFSSDLKD LLRNLLQVDL TKRFGNLKNG VNDIKNHKWF ATTDWIAIYQ RKVEAPFIPK FKG PGDTSN FDDYEEEEIR VSINEKCGKE FTEF |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 5 mg/mL | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7 構成要素:
| |||||||||||||||||||||
| グリッド | モデル: Quantifoil, UltrAuFoil, R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 雰囲気: OTHER 詳細: Grids were plasma cleaned using a Solarus plasma cleaner (Gatan, Inc.) | |||||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 277.15 K / 装置: HOMEMADE PLUNGER 詳細: Sample was manually blotted for 4-5 seconds using Whatman No. 1 filter paper immediately prior to plunge-freezing.. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | #0 - Image recording ID: 1 #0 - フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) #0 - 検出モード: COUNTING / #0 - 撮影したグリッド数: 2 / #0 - 実像数: 3176 / #0 - 平均露光時間: 11.0 sec. / #0 - 平均電子線量: 69.0 e/Å2 / #1 - Image recording ID: 2 #1 - フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) #1 - 検出モード: COUNTING / #1 - デジタル化 - サイズ - 横: 3710 pixel / #1 - デジタル化 - サイズ - 縦: 3838 pixel / #1 - デジタル化 - サンプリング間隔: 5.0 µm / #1 - デジタル化 - 画像ごとのフレーム数: 1-44 / #1 - 撮影したグリッド数: 2 / #1 - 実像数: 2402 / #1 - 平均露光時間: 11.0 sec. / #1 - 平均電子線量: 69.0 e/Å2 / #1 - 詳細: Specimen was tilted at 30 degrees |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 16.0 µm / 最小 デフォーカス(公称値): 5.0 µm / 倍率(公称値): 73000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)