+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 9gxt | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
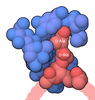
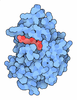
| タイトル | C. thermocellum UvrA in complex with DNA with a fluorescein modification and AMPPNP (ATP-bound conformation 1) | |||||||||||||||||||||||||||||||||
 要素 要素 |
| |||||||||||||||||||||||||||||||||
 キーワード キーワード | DNA BINDING PROTEIN / DNA Repair pathway / Nucleotide excision repair pathway / NER | |||||||||||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報excinuclease ABC activity / excinuclease repair complex / SOS response / nucleotide-excision repair / ATP hydrolysis activity / DNA binding / zinc ion binding / ATP binding / cytoplasm 類似検索 - 分子機能 | |||||||||||||||||||||||||||||||||
| 生物種 |  Acetivibrio thermocellus (バクテリア) Acetivibrio thermocellus (バクテリア)synthetic construct (人工物) | |||||||||||||||||||||||||||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||||||||||||||||||||||||||
 データ登録者 データ登録者 | Nirwal, S. / Czarnocki-Cieciura, M. / Nowotny, M. | |||||||||||||||||||||||||||||||||
| 資金援助 |  ポーランド, 1件 ポーランド, 1件
| |||||||||||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2025 ジャーナル: Nat Commun / 年: 2025タイトル: Structural snapshots of the mechanism of ATP-dependent DNA damage recognition by UvrA. 著者: Shivlee Nirwal / Mariusz Czarnocki-Cieciura / Weronika Zajko / Krzysztof Skowronek / Roman H Szczepanowski / Marcin Nowotny /  要旨: Nucleotide excision repair is a DNA repair pathway which detects and fixes various DNA lesions that distort the structure of DNA. In bacteria, the pathway starts with the UvrA protein which has two ...Nucleotide excision repair is a DNA repair pathway which detects and fixes various DNA lesions that distort the structure of DNA. In bacteria, the pathway starts with the UvrA protein which has two adenosine triphosphatase modules and forms dimers. The DNA is handed over from UvrA to UvrB, which is a weak helicase that verifies the presence of damage. Despite intense studies, the role of the ATPase activity of UvrA in damage recognition is unclear. Here, we present a series of cryo-electron microscopy structures of UvrA in complex with three different DNAs and in the presence and absence of nucleotides. We also present a structure of UvrA:UvrB:DNA complex. These structures reveal a major rearrangement of the UvrA dimer upon ATP binding. We propose that these conformational changes are used to mechanically probe the integrity of DNA for damage localization. Collectively, our results present snapshots of UvrA's ATP-dependent DNA damage detection. | |||||||||||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  9gxt.cif.gz 9gxt.cif.gz | 371.5 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb9gxt.ent.gz pdb9gxt.ent.gz | 227.2 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  9gxt.json.gz 9gxt.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/gx/9gxt https://data.pdbj.org/pub/pdb/validation_reports/gx/9gxt ftp://data.pdbj.org/pub/pdb/validation_reports/gx/9gxt ftp://data.pdbj.org/pub/pdb/validation_reports/gx/9gxt | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  51674MC  9gxkC  9gxlC  9gxmC  9gxnC  9gxoC  9gxpC  9gxqC  9gxrC  9gxsC  9gxuC  9gxvC  9gxwC  9gy7C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 107144.773 Da / 分子数: 2 / 由来タイプ: 組換発現 由来: (組換発現)  Acetivibrio thermocellus (バクテリア) Acetivibrio thermocellus (バクテリア)遺伝子: uvrA, Cthe_0311 / 発現宿主:  #2: DNA鎖 | 分子量: 15411.887 Da / 分子数: 2 / 由来タイプ: 合成 / 詳細: Random sequence built in model. / 由来: (合成) synthetic construct (人工物) #3: 化合物 | #4: 化合物 | ChemComp-ANP / 研究の焦点であるリガンドがあるか | Y | Has protein modification | N | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: C. thermocellum UvrA in complex with DNA with a fluorescein modification and AMPPNP タイプ: COMPLEX / Entity ID: #1-#2 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 0.247 MDa / 実験値: NO |
| 由来(天然) | 生物種:  Acetivibrio thermocellus (バクテリア) Acetivibrio thermocellus (バクテリア) |
| 由来(組換発現) | 生物種:  |
| 緩衝液 | pH: 7.5 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES 詳細: Sample fixed with 0.01% glutaraldehyde and concentrated prior to vitrification; exact concentration cannot be estimated accurately. |
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 200 divisions/in. / グリッドのタイプ: C-flat-2/1 |
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 95 % / 凍結前の試料温度: 277 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: TFS KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 105000 X / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 600 nm / Cs: 2.7 mm / C2レンズ絞り径: 50 µm |
| 撮影 | 電子線照射量: 40.54 e/Å2 フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 撮影したグリッド数: 1 / 実像数: 10348 / 詳細: 4860 images were collected with 30 deg stage tilt |
| 電子光学装置 | エネルギーフィルター名称: GIF Bioquantum / エネルギーフィルタースリット幅: 20 eV |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 3577433 | ||||||||||||||||||||||||||||
| 対称性 | 点対称性: C2 (2回回転対称) | ||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.1 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 126432 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: AB INITIO MODEL | ||||||||||||||||||||||||||||
| 精密化 | 交差検証法: NONE 立体化学のターゲット値: GeoStd + Monomer Library + CDL v1.2 | ||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 71.13 Å2 | ||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー


















 PDBj
PDBj