+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8jem | ||||||
|---|---|---|---|---|---|---|---|
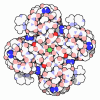
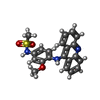
| タイトル | DltB tetramer in complex with inhibitor m-AMSA | ||||||
 要素 要素 | Teichoic acid D-alanyltransferase | ||||||
 キーワード キーワード | MEMBRANE PROTEIN/INHIBITOR / channel / anti-virulence / MBOAT / DltB / MEMBRANE PROTEIN / MEMBRANE PROTEIN-INHIBITOR complex | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報lipoteichoic acid biosynthetic process / acyltransferase activity / 転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの / plasma membrane 類似検索 - 分子機能 | ||||||
| 生物種 |  Streptococcus thermophilus LMG 18311 (ストレプトコッカス・サリバリウス 亜種 サーモフィラス) Streptococcus thermophilus LMG 18311 (ストレプトコッカス・サリバリウス 亜種 サーモフィラス) | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.23 Å | ||||||
 データ登録者 データ登録者 | Zhang, P. / Liu, Z. | ||||||
| 資金援助 | 1件
| ||||||
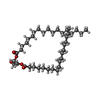
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Structural insights into the transporting and catalyzing mechanism of DltB in LTA D-alanylation. 著者: Pingfeng Zhang / Zheng Liu /  要旨: DltB, a model member of the Membrane-Bound O-AcylTransferase (MBOAT) superfamily, plays a crucial role in D-alanylation of the lipoteichoic acid (LTA), a significant component of the cell wall of ...DltB, a model member of the Membrane-Bound O-AcylTransferase (MBOAT) superfamily, plays a crucial role in D-alanylation of the lipoteichoic acid (LTA), a significant component of the cell wall of gram-positive bacteria. This process stabilizes the cell wall structure, influences bacterial virulence, and modulates the host immune response. Despite its significance, the role of DltB is not well understood. Through biochemical analysis and cryo-EM imaging, we discover that Streptococcus thermophilus DltB forms a homo-tetramer on the cell membrane. We further visualize DltB in an apo form, in complex with DltC, and in complex with its inhibitor amsacrine (m-AMSA). Each tetramer features a central hole. The C-tunnel of each protomer faces the intratetramer interface and provides access to the periphery membrane. Each protomer binds a DltC without changing the tetrameric organization. A phosphatidylglycerol (PG) molecule in the substrate-binding site may serve as an LTA carrier. The inhibitor m-AMSA bound to the L-tunnel of each protomer blocks the active site. The tetrameric organization of DltB provides a scaffold for catalyzing D-alanyl transfer and regulating the channel opening and closing. Our findings unveil DltB's dual function in the D-alanylation pathway, and provide insight for targeting DltB as a anti-virulence antibiotic. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8jem.cif.gz 8jem.cif.gz | 486 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8jem.ent.gz pdb8jem.ent.gz | 330.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8jem.json.gz 8jem.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  8jem_validation.pdf.gz 8jem_validation.pdf.gz | 3.6 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  8jem_full_validation.pdf.gz 8jem_full_validation.pdf.gz | 3.7 MB | 表示 | |
| XML形式データ |  8jem_validation.xml.gz 8jem_validation.xml.gz | 75 KB | 表示 | |
| CIF形式データ |  8jem_validation.cif.gz 8jem_validation.cif.gz | 100.4 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/je/8jem https://data.pdbj.org/pub/pdb/validation_reports/je/8jem ftp://data.pdbj.org/pub/pdb/validation_reports/je/8jem ftp://data.pdbj.org/pub/pdb/validation_reports/je/8jem | HTTPS FTP |
-関連構造データ
| 関連構造データ |  36192MC  8jesC  8jf2C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 51780.027 Da / 分子数: 4 / 由来タイプ: 組換発現 由来: (組換発現)  Streptococcus thermophilus LMG 18311 (ストレプトコッカス・サリバリウス 亜種 サーモフィラス) Streptococcus thermophilus LMG 18311 (ストレプトコッカス・サリバリウス 亜種 サーモフィラス)株: LMG 18311 / 遺伝子: dltB, stu0762 / 発現宿主:  参照: UniProt: Q5M4V4, 転移酵素; アシル基を移すもの; アミノアシル基以外のアシル基を移すもの #2: 化合物 | ChemComp-ASW / #3: 化合物 | ChemComp-PGT / ( #4: 糖 | ChemComp-LMT / #5: 化合物 | 研究の焦点であるリガンドがあるか | Y | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: DltB tetramer in complex with inhibitor m-AMSA. / タイプ: COMPLEX / Entity ID: #1 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 48 kDa/nm / 実験値: YES |
| 由来(天然) | 生物種:  Streptococcus thermophilus (ストレプトコッカス・サリバリウス 亜種 サーモフィラス) Streptococcus thermophilus (ストレプトコッカス・サリバリウス 亜種 サーモフィラス)株: LMG 18311 |
| 由来(組換発現) | 生物種:  |
| 緩衝液 | pH: 7.5 / 詳細: 20 mM Hopes-Na, pH7.5, 0.03% DDM |
| 緩衝液成分 | 濃度: 25 mM / 名称: Hepes |
| 試料 | 濃度: 9 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES 詳細: The DltB protein was purified in DDM, the tetramer fractions from gel filtration column were concentrated to about 10 mg/ml. |
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil R1.2/1.3 |
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 277 K 詳細: After incubation on the grids at 277K under 100% humidity for 10 s, the grids were bloted for 3.0 s and then plunged frozen into liquid ethane cooled by liquid nitrogen using a Vitrobot. |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1800 nm / 最小 デフォーカス(公称値): 1100 nm |
| 撮影 | 電子線照射量: 55 e/Å2 フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.23 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 294021 / 対称性のタイプ: POINT | ||||||||||||||||||||||||
| 原子モデル構築 | 空間: REAL | ||||||||||||||||||||||||
| 精密化 | 交差検証法: NONE 立体化学のターゲット値: GeoStd + Monomer Library + CDL v1.2 | ||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 93.19 Å2 | ||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー






 PDBj
PDBj