+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8g4w | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM consensus structure of Escherichia coli que-PEC (paused elongation complex) RNA Polymerase plus preQ1 ligand | |||||||||||||||
 要素 要素 |
| |||||||||||||||
 キーワード キーワード | TRANSCRIPTION / RNA Polymerase / Riboswitch / preQ1 | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報DNA-directed RNA polymerase complex / ribonucleoside binding / DNA-directed 5'-3' RNA polymerase activity / DNA-directed RNA polymerase / protein dimerization activity / DNA-templated transcription / magnesium ion binding / DNA binding / zinc ion binding / cytoplasm 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  | |||||||||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.8 Å | |||||||||||||||
 データ登録者 データ登録者 | Porta, J.C. / Chauvier, A. / Deb, I. / Ellinger, E. / Frank, A.T. / Meze, K. / Ohi, M.D. / Walter, N.G. | |||||||||||||||
| 資金援助 |  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2023 ジャーナル: Nat Struct Mol Biol / 年: 2023タイトル: Structural basis for control of bacterial RNA polymerase pausing by a riboswitch and its ligand. 著者: Adrien Chauvier / Jason C Porta / Indrajit Deb / Emily Ellinger / Katarina Meze / Aaron T Frank / Melanie D Ohi / Nils G Walter /   要旨: Folding of nascent transcripts can be modulated by the RNA polymerase (RNAP) that carries out their transcription, and vice versa. A pause of RNAP during transcription of a preQ riboswitch (termed ...Folding of nascent transcripts can be modulated by the RNA polymerase (RNAP) that carries out their transcription, and vice versa. A pause of RNAP during transcription of a preQ riboswitch (termed que-PEC) is stabilized by a previously characterized template consensus sequence and the ligand-free conformation of the nascent RNA. Ligand binding to the riboswitch induces RNAP pause release and downstream transcription termination; however, the mechanism by which riboswitch folding modulates pausing is unclear. Here, we report single-particle cryo-electron microscopy reconstructions of que-PEC in ligand-free and ligand-bound states. In the absence of preQ, the RNA transcript is in an unexpected hyper-translocated state, preventing downstream nucleotide incorporation. Strikingly, on ligand binding, the riboswitch rotates around its helical axis, expanding the surrounding RNAP exit channel and repositioning the transcript for elongation. Our study reveals the tight coupling by which nascent RNA structures and their ligands can functionally regulate the macromolecular transcription machinery. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8g4w.cif.gz 8g4w.cif.gz | 614.6 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8g4w.ent.gz pdb8g4w.ent.gz | 483.7 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8g4w.json.gz 8g4w.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  8g4w_validation.pdf.gz 8g4w_validation.pdf.gz | 1.7 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  8g4w_full_validation.pdf.gz 8g4w_full_validation.pdf.gz | 1.8 MB | 表示 | |
| XML形式データ |  8g4w_validation.xml.gz 8g4w_validation.xml.gz | 103.3 KB | 表示 | |
| CIF形式データ |  8g4w_validation.cif.gz 8g4w_validation.cif.gz | 157.6 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/g4/8g4w https://data.pdbj.org/pub/pdb/validation_reports/g4/8g4w ftp://data.pdbj.org/pub/pdb/validation_reports/g4/8g4w ftp://data.pdbj.org/pub/pdb/validation_reports/g4/8g4w | HTTPS FTP |
-関連構造データ
| 関連構造データ |  29732MC  8f3cC  8g00C  8g1sC  8g2wC  8g7eC  8g8zC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-DNA鎖 , 2種, 2分子 AB
| #1: DNA鎖 | 分子量: 12063.754 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   |
|---|---|
| #2: DNA鎖 | 分子量: 9486.079 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   |
-DNA-directed RNA polymerase subunit ... , 4種, 5分子 GHKIJ
| #3: タンパク質 | 分子量: 25971.531 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   #4: タンパク質 | | 分子量: 8963.044 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   #6: タンパク質 | | 分子量: 150560.562 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   #7: タンパク質 | | 分子量: 150436.344 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   |
|---|
-RNA鎖 , 1種, 1分子 R
| #5: RNA鎖 | 分子量: 15059.079 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   |
|---|
-非ポリマー , 2種, 2分子 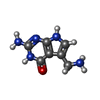


| #8: 化合物 | ChemComp-PRF / |
|---|---|
| #9: 化合物 | ChemComp-MG / |
-詳細
| 研究の焦点であるリガンドがあるか | Y |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Cryo-EM consensus structure of Escherichia coli que-PEC (paused elongation complex) RNA Polymerase plus preQ1 ligand タイプ: COMPLEX / Entity ID: #1-#7 / 由来: RECOMBINANT | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 値: 0.420 MDa / 実験値: NO | ||||||||||||||||||||
| 由来(天然) | 生物種:  | ||||||||||||||||||||
| 由来(組換発現) | 生物種:  | ||||||||||||||||||||
| 緩衝液 | pH: 7.5 | ||||||||||||||||||||
| 緩衝液成分 |
| ||||||||||||||||||||
| 試料 | 濃度: 5 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES | ||||||||||||||||||||
| 試料支持 | グリッドの材料: GOLD / グリッドのサイズ: 400 divisions/in. / グリッドのタイプ: C-flat-1.2/1.3 | ||||||||||||||||||||
| 急速凍結 | 凍結剤: ETHANE 詳細: VITRIFICATION WAS CARRIED OUT IN A CHAMBER WITH THE TEMPERATURE SET TO 4 DEGREES CELSIUS. |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 3500 nm / 最小 デフォーカス(公称値): 500 nm / Cs: 2.7 mm / アライメント法: COMA FREE |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 電子線照射量: 62 e/Å2 フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) |
| 画像スキャン | 横: 1 / 縦: 1 / 動画フレーム数/画像: 40 |
- 解析
解析
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 粒子像の選択 | 選択した粒子像数: 122526 | ||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.8 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 51824 / 対称性のタイプ: POINT | ||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: FLEXIBLE FIT / 空間: REAL / Target criteria: Cross-correlation coefficient | ||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 6ASX Accession code: 6ASX / Source name: PDB / タイプ: experimental model | ||||||||||||||||||||||||
| 精密化 | 最高解像度: 3.8 Å | ||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー







 PDBj
PDBj


































































