+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7ryr | ||||||
|---|---|---|---|---|---|---|---|
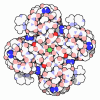
| タイトル | SthK R120A Open State 3 | ||||||
 要素 要素 | SthK | ||||||
 キーワード キーワード | TRANSPORT PROTEIN / Cyclic nucleotide-gated ion channel | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報intracellular cyclic nucleotide activated cation channel complex / intracellularly cGMP-activated cation channel activity / intracellularly cAMP-activated cation channel activity / cGMP binding / protein-containing complex binding / plasma membrane 類似検索 - 分子機能 | ||||||
| 生物種 |   Spirochaeta thermophila (バクテリア) Spirochaeta thermophila (バクテリア) | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.6 Å | ||||||
 データ登録者 データ登録者 | Gao, X. / Nimigean, C. / Schmidpeter, P. | ||||||
| 資金援助 |  米国, 1件 米国, 1件
| ||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2022 ジャーナル: Nat Commun / 年: 2022タイトル: Gating intermediates reveal inhibitory role of the voltage sensor in a cyclic nucleotide-modulated ion channel. 著者: Xiaolong Gao / Philipp A M Schmidpeter / Vladimir Berka / Ryan J Durham / Chen Fan / Vasanthi Jayaraman / Crina M Nimigean /   要旨: Understanding how ion channels gate is important for elucidating their physiological roles and targeting them in pathophysiological states. Here, we used SthK, a cyclic nucleotide-modulated channel ...Understanding how ion channels gate is important for elucidating their physiological roles and targeting them in pathophysiological states. Here, we used SthK, a cyclic nucleotide-modulated channel from Spirochaeta thermophila, to define a ligand-gating trajectory that includes multiple on-pathway intermediates. cAMP is a poor partial agonist for SthK and depolarization increases SthK activity. Tuning the energy landscape by gain-of-function mutations in the voltage sensor domain (VSD) allowed us to capture multiple intermediates along the ligand-activation pathway, highlighting the allosteric linkage between VSD, cyclic nucleotide-binding (CNBD) and pore domains. Small, lateral displacements of the VSD S4 segment were necessary to open the intracellular gate, pointing to an inhibitory VSD at rest. We propose that in wild-type SthK, depolarization leads to such VSD displacements resulting in release of inhibition. In summary, we report conformational transitions along the activation pathway that reveal allosteric couplings between key sites integrating to open the intracellular gate. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7ryr.cif.gz 7ryr.cif.gz | 349.5 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7ryr.ent.gz pdb7ryr.ent.gz | 276.5 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7ryr.json.gz 7ryr.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  7ryr_validation.pdf.gz 7ryr_validation.pdf.gz | 1.5 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  7ryr_full_validation.pdf.gz 7ryr_full_validation.pdf.gz | 1.5 MB | 表示 | |
| XML形式データ |  7ryr_validation.xml.gz 7ryr_validation.xml.gz | 53.5 KB | 表示 | |
| CIF形式データ |  7ryr_validation.cif.gz 7ryr_validation.cif.gz | 71.5 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/ry/7ryr https://data.pdbj.org/pub/pdb/validation_reports/ry/7ryr ftp://data.pdbj.org/pub/pdb/validation_reports/ry/7ryr ftp://data.pdbj.org/pub/pdb/validation_reports/ry/7ryr | HTTPS FTP |
-関連構造データ
| 関連構造データ |  24746MC  7rshC  7rtfC  7rtjC  7ru0C  7rysC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 51032.461 Da / 分子数: 4 / 変異: R120A / 由来タイプ: 組換発現 由来: (組換発現)   Spirochaeta thermophila (バクテリア) Spirochaeta thermophila (バクテリア)遺伝子: Spith_0644 / 発現宿主:  #2: 化合物 | ChemComp-CMP / #3: 化合物 | ChemComp-PGW / ( 研究の焦点であるリガンドがあるか | N | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: SthK / タイプ: COMPLEX / 詳細: R120A mutant of wild type SthK / Entity ID: #1 / 由来: RECOMBINANT | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 実験値: NO | |||||||||||||||
| 由来(天然) | 生物種:   Spirochaeta thermophila (バクテリア) Spirochaeta thermophila (バクテリア) | |||||||||||||||
| 由来(組換発現) | 生物種:  | |||||||||||||||
| 緩衝液 | pH: 7 | |||||||||||||||
| 緩衝液成分 |
| |||||||||||||||
| 試料 | 濃度: 7.5 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES / 詳細: Protein in nanodisc of DOPC/POPG/Cardiolipin | |||||||||||||||
| 試料支持 | グリッドの材料: GOLD / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil R1.2/1.3 | |||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 295 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 81000 X / 最大 デフォーカス(公称値): 2000 nm / 最小 デフォーカス(公称値): 1500 nm / Cs: 2.7 mm |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 電子線照射量: 1.459 e/Å2 / フィルム・検出器のモデル: GATAN K3 (6k x 4k) |
- 解析
解析
| ソフトウェア | 名称: PHENIX / バージョン: 1.19.2_4158: / 分類: 精密化 | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 3004702 | ||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C4 (4回回転対称) | ||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.6 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 46629 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | 空間: REAL | ||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 7RTJ Accession code: 7RTJ / Source name: PDB / タイプ: experimental model | ||||||||||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー








 PDBj
PDBj