+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 3j67 | ||||||
|---|---|---|---|---|---|---|---|
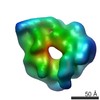
| タイトル | Structural mechanism of the dynein powerstroke (post-powerstroke state) | ||||||
 要素 要素 | Dynein motor domain | ||||||
 キーワード キーワード | MOTOR PROTEIN | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報karyogamy / astral microtubule / establishment of mitotic spindle localization / nuclear migration along microtubule / minus-end-directed microtubule motor activity / cytoplasmic dynein complex / dynein light intermediate chain binding / nuclear migration / spindle pole body / dynein intermediate chain binding ...karyogamy / astral microtubule / establishment of mitotic spindle localization / nuclear migration along microtubule / minus-end-directed microtubule motor activity / cytoplasmic dynein complex / dynein light intermediate chain binding / nuclear migration / spindle pole body / dynein intermediate chain binding / cytoplasmic microtubule / establishment of mitotic spindle orientation / mitotic sister chromatid segregation / cytoplasmic microtubule organization / Neutrophil degranulation / mitotic spindle organization / cell cortex / ATP hydrolysis activity / ATP binding / cytoplasm 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 | 電子顕微鏡法 / 電子線トモグラフィー法 / クライオ電子顕微鏡法 / 解像度: 34 Å | ||||||
 データ登録者 データ登録者 | Lin, J. / Okada, K. / Raytchev, M. / Smith, M.C. / Nicastro, D. | ||||||
 引用 引用 |  ジャーナル: Nat Cell Biol / 年: 2014 ジャーナル: Nat Cell Biol / 年: 2014タイトル: Structural mechanism of the dynein power stroke. 著者: Jianfeng Lin / Kyoko Okada / Milen Raytchev / Maria C Smith / Daniela Nicastro /  要旨: Dyneins are large microtubule motor proteins required for mitosis, intracellular transport and ciliary and flagellar motility. They generate force through a power-stroke mechanism, which is an ATP- ...Dyneins are large microtubule motor proteins required for mitosis, intracellular transport and ciliary and flagellar motility. They generate force through a power-stroke mechanism, which is an ATP-consuming cycle of pre- and post-power-stroke conformational changes that cause relative motion between different dynein domains. However, key structural details of dynein's force generation remain elusive. Here, using cryo-electron tomography of intact, active (that is, beating), rapidly frozen sea urchin sperm flagella, we determined the in situ three-dimensional structures of all domains of both pre- and post-power-stroke dynein, including the previously unresolved linker and stalk of pre-power-stroke dynein. Our results reveal that the rotation of the head relative to the linker is the key action in dynein movement, and that there are at least two distinct pre-power-stroke conformations: pre-I (microtubule-detached) and pre-II (microtubule-bound). We provide three-dimensional reconstructions of native dyneins in three conformational states, in situ, allowing us to propose a molecular model of the structural cycle underlying dynein movement. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  3j67.cif.gz 3j67.cif.gz | 466.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb3j67.ent.gz pdb3j67.ent.gz | 370.6 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  3j67.json.gz 3j67.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  3j67_validation.pdf.gz 3j67_validation.pdf.gz | 654.6 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  3j67_full_validation.pdf.gz 3j67_full_validation.pdf.gz | 722.1 KB | 表示 | |
| XML形式データ |  3j67_validation.xml.gz 3j67_validation.xml.gz | 64.6 KB | 表示 | |
| CIF形式データ |  3j67_validation.cif.gz 3j67_validation.cif.gz | 99.2 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/j6/3j67 https://data.pdbj.org/pub/pdb/validation_reports/j6/3j67 ftp://data.pdbj.org/pub/pdb/validation_reports/j6/3j67 ftp://data.pdbj.org/pub/pdb/validation_reports/j6/3j67 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 262122.234 Da / 分子数: 1 / 断片: SEE REMARK 999 / 由来タイプ: 天然 由来: (天然)  参照: UniProt: P36022*PLUS |
|---|---|
| 配列の詳細 | THE IMAGED DYNEIN WAS FROM STRONGYLOCENTROTUS PURPURATUS, BUT THE MODELED COORDINATES ARE DERIVED ...THE IMAGED DYNEIN WAS FROM STRONGYLOC |
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 電子線トモグラフィー法 |
- 試料調製
試料調製
| 構成要素 | 名称: inactive sea urchin sperm flagella / タイプ: COMPLEX |
|---|---|
| 緩衝液 | pH: 8 詳細: 360 mM NaCl, 50 mM MgCl2, 10 mM CaCl2, 10 mM KCl, 30 mM HEPES, pH 8.0, 2 mM erythro-9-[3-(2-hydroxynonyl)]-adenine |
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | 詳細: Quantifoil holey carbon grids Cu 200 mesh R2/2 |
| 急速凍結 | 装置: HOMEMADE PLUNGER / 凍結剤: ETHANE 詳細: Blot for 1.5-2.5 seconds before plunging in liquid ethane. 手法: Blot for 1.5-2.5 seconds before plunging. |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Tecnai F30 / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TECNAI F30 / 日付: 2012年4月28日 |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 13500 X / 最大 デフォーカス(公称値): 8000 nm / 最小 デフォーカス(公称値): 6000 nm |
| 試料ホルダ | 試料ホルダーモデル: GATAN LIQUID NITROGEN / 資料ホルダタイプ: GATAN LIQUID NITROGEN / 温度: 80 K / 傾斜角・最大: 65 ° / 傾斜角・最小: -65 ° |
| 撮影 | 電子線照射量: 100 e/Å2 フィルム・検出器のモデル: GENERIC GATAN (2k x 2k) |
| 電子光学装置 | エネルギーフィルター名称: GIF / エネルギーフィルター 上限: 20 eV / エネルギーフィルター 下限: 0 eV |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 相対比: 1 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||
| 3次元再構成 | 手法: fiducial alignment and weighted back-projection / 解像度: 34 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ピクセルサイズ(公称値): 9.856 Å / ピクセルサイズ(実測値): 9.856 Å 詳細: Final maps were calculated by averaging 1100 particles from 9 tomograms. 1100 axonemal repeats (96 nm long) from 9 tomograms (reconstructed using fiducial alignment and weighted ...詳細: Final maps were calculated by averaging 1100 particles from 9 tomograms. 1100 axonemal repeats (96 nm long) from 9 tomograms (reconstructed using fiducial alignment and weighted backprojection, IMOD software, Kremer et al. 1996) were aligned and averaged using the PEET software (bio3d.colorado.edu, Nicastro et al. 2006). 対称性のタイプ: POINT | ||||||||||||
| 原子モデル構築 | プロトコル: RIGID BODY FIT / Target criteria: Cross-correlation coefficient 詳細: REFINEMENT PROTOCOL--rigid body DETAILS--Initial local fitting was done using Chimera and then manual adjustment was performed. | ||||||||||||
| 原子モデル構築 | PDB-ID: 4AKI PDB chain-ID: A / Accession code: 4AKI / Source name: PDB / タイプ: experimental model | ||||||||||||
| 精密化ステップ | サイクル: LAST
|
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj










