+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Selenocysteine synthase- SelA | ||||||||||||||||||
 マップデータ マップデータ | SelA sharpened map (B-factor = 92.5 A^2) | ||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||
 キーワード キーワード | Selenocysteine / tRNASec / Sec-synthase / RNA BINDING PROTEIN | ||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報L-seryl-tRNASec selenium transferase / L-seryl-tRNA(Sec) selenium transferase activity / selenocysteine biosynthetic process / selenocysteine incorporation / pyridoxal phosphate binding / identical protein binding / cytosol 類似検索 - 分子機能 | ||||||||||||||||||
| 生物種 |  | ||||||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.69 Å | ||||||||||||||||||
 データ登録者 データ登録者 | Balasco Serrao VH / Minari K / Pereira HM / Thiemann OH | ||||||||||||||||||
| 資金援助 |  ブラジル, ブラジル,  米国, 5件 米国, 5件
| ||||||||||||||||||
 引用 引用 |  ジャーナル: Curr Res Struct Biol / 年: 2024 ジャーナル: Curr Res Struct Biol / 年: 2024タイトル: Bacterial selenocysteine synthase structure revealed by single-particle cryoEM. 著者: Vitor Hugo Balasco Serrão / Karine Minari / Humberto D'Muniz Pereira / Otavio Henrique Thiemann /   要旨: The 21st amino acid, selenocysteine (Sec), is synthesized on its dedicated transfer RNA (tRNA). In bacteria, Sec is synthesized from Ser-tRNA by Selenocysteine Synthase (SelA), which is a pivotal ...The 21st amino acid, selenocysteine (Sec), is synthesized on its dedicated transfer RNA (tRNA). In bacteria, Sec is synthesized from Ser-tRNA by Selenocysteine Synthase (SelA), which is a pivotal enzyme in the biosynthesis of Sec. The structural characterization of bacterial SelA is of paramount importance to decipher its catalytic mechanism and its role in the regulation of the Sec-synthesis pathway. Here, we present a comprehensive single-particle cryo-electron microscopy (SPA cryoEM) structure of the bacterial SelA with an overall resolution of 2.69 Å. Using recombinant SelA, we purified and prepared samples for single-particle cryoEM. The structural insights from SelA, combined with previous and knowledge, underscore the indispensable role of decamerization in SelA's function. Moreover, our structural analysis corroborates previous results that show that SelA adopts a pentamer of dimers configuration, and the active site architecture, substrate binding pocket, and key K295 catalytic residue are identified and described in detail. The differences in protein architecture and substrate coordination between the bacterial enzyme and its counterparts offer compelling structural evidence supporting the independent molecular evolution of the bacterial and archaea/eukarya Ser-Sec biosynthesis present in the natural world. | ||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_42845.map.gz emd_42845.map.gz | 398.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-42845-v30.xml emd-42845-v30.xml emd-42845.xml emd-42845.xml | 19.2 KB 19.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
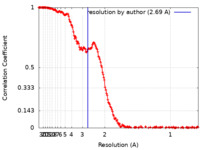
| FSC (解像度算出) |  emd_42845_fsc.xml emd_42845_fsc.xml | 21.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_42845.png emd_42845.png | 54.5 KB | ||
| Filedesc metadata |  emd-42845.cif.gz emd-42845.cif.gz | 6.6 KB | ||
| その他 |  emd_42845_half_map_1.map.gz emd_42845_half_map_1.map.gz emd_42845_half_map_2.map.gz emd_42845_half_map_2.map.gz | 391.8 MB 391.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-42845 http://ftp.pdbj.org/pub/emdb/structures/EMD-42845 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-42845 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-42845 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_42845_validation.pdf.gz emd_42845_validation.pdf.gz | 1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_42845_full_validation.pdf.gz emd_42845_full_validation.pdf.gz | 1 MB | 表示 | |
| XML形式データ |  emd_42845_validation.xml.gz emd_42845_validation.xml.gz | 25.3 KB | 表示 | |
| CIF形式データ |  emd_42845_validation.cif.gz emd_42845_validation.cif.gz | 32.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42845 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42845 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42845 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42845 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8uzwMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_42845.map.gz / 形式: CCP4 / 大きさ: 421.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_42845.map.gz / 形式: CCP4 / 大きさ: 421.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | SelA sharpened map (B-factor = 92.5 A^2) | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.826 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map B
| ファイル | emd_42845_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B | ||||||||||||
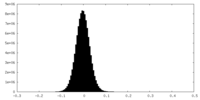
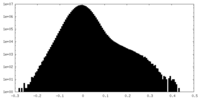
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map A
| ファイル | emd_42845_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A | ||||||||||||
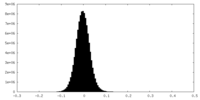
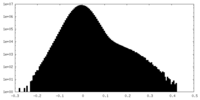
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Bacterial Selenocysteine Synthase
| 全体 | 名称: Bacterial Selenocysteine Synthase |
|---|---|
| 要素 |
|
-超分子 #1: Bacterial Selenocysteine Synthase
| 超分子 | 名称: Bacterial Selenocysteine Synthase / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: Heterologously expressed E. coli homodecameric Selenocysteine Synthase |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 510 KDa |
-分子 #1: L-seryl-tRNA(Sec) selenium transferase
| 分子 | 名称: L-seryl-tRNA(Sec) selenium transferase / タイプ: protein_or_peptide / ID: 1 / コピー数: 10 / 光学異性体: LEVO / EC番号: L-seryl-tRNASec selenium transferase |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 50.895172 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MTTETRSLYS QLPAIDRLLR DSSFLSLRDT YGHTRVVELL RQMLDEAREV IRGSQTLPAW CENWAQEVDA RLTKEAQSAL RPVINLTGT VLHTNLGRAL QAEAAVEAVA QAMRSPVTLE YDLDDAGRGH RDRALAQLLC RITGAEDACI VNNNAAAVLL M LAATASGK ...文字列: MTTETRSLYS QLPAIDRLLR DSSFLSLRDT YGHTRVVELL RQMLDEAREV IRGSQTLPAW CENWAQEVDA RLTKEAQSAL RPVINLTGT VLHTNLGRAL QAEAAVEAVA QAMRSPVTLE YDLDDAGRGH RDRALAQLLC RITGAEDACI VNNNAAAVLL M LAATASGK EVVVSRGELV EIGGAFRIPD VMRQAGCTLH EVGTTNRTHA NDYRQAVNEN TALLMKVHTS NYSIQGFTKA ID EAELVAL GKELDVPVVT DLGSGSLVDL SQYGLPKEPM PQELIAAGVS LVSFSGD(LLP)LL GGPQAGIIVG KKEMIARLQ SHPLKRALRA DKMTLAALEA TLRLYLHPEA LSEKLPTLRL LTRSAEVIQI QAQRLQAPLA AHYGAEFAVQ VMPCLSQIGS GSLPVDRLP SAALTFTPHD GRGSHLESLA ARWRELPVPV IGRIYDGRLW LDLRCLEDEQ RFLEMLLK UniProtKB: L-seryl-tRNA(Sec) selenium transferase |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3.9 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
詳細: 20 mM potassium phosphate pH 7.5, 100 mM sodium chloride, 2 mM 2-mercaptoethanol, and 10 uM pyridoxal 5-phosphate. | |||||||||||||||
| グリッド | モデル: Quantifoil / 材質: COPPER / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 支持フィルム - Film thickness: 20 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 20 sec. / 前処理 - 気圧: 0.00035999999999999997 kPa | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV 詳細: The sample was blotted for 2.5 seconds using a force of -10 and then swiftly plunged frozen into liquid ethane using the Vitrobot Mark IV - Thermo Fisher Scientific.. | |||||||||||||||
| 詳細 | Monodisperse sample after size-exclusion chromatography |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 撮影したグリッド数: 1 / 実像数: 4592 / 平均電子線量: 45.4 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD 最大 デフォーカス(公称値): 2.8000000000000003 µm 最小 デフォーカス(公称値): 0.6 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 温度因子: 95.2 |
|---|---|
| 得られたモデル |  PDB-8uzw: |
 ムービー
ムービー コントローラー
コントローラー




 Z
Z Y
Y X
X