+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Firmicutes Rubisco | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Carboxylase / Oxygenase / LYASE | |||||||||
| 生物種 |  Bacillota (バクテリア) Bacillota (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.21 Å | |||||||||
 データ登録者 データ登録者 | Kaeser BP / Liu AK / Shih PM | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Curr Biol / 年: 2023 ジャーナル: Curr Biol / 年: 2023タイトル: Deep-branching evolutionary intermediates reveal structural origins of form I rubisco. 著者: Albert K Liu / Benjamin Kaeser / LinXing Chen / Jacob West-Roberts / Leah J Taylor-Kearney / Adi Lavy / Damian Günzing / Wen-Jun Li / Michal Hammel / Eva Nogales / Jillian F Banfield / Patrick M Shih /    要旨: The enzyme rubisco (ribulose-1,5-bisphosphate carboxylase/oxygenase) catalyzes the majority of biological carbon fixation on Earth. Although the vast majority of rubiscos across the tree of life ...The enzyme rubisco (ribulose-1,5-bisphosphate carboxylase/oxygenase) catalyzes the majority of biological carbon fixation on Earth. Although the vast majority of rubiscos across the tree of life assemble as homo-oligomers, the globally predominant form I enzyme-found in plants, algae, and cyanobacteria-forms a unique hetero-oligomeric complex. The recent discovery of a homo-oligomeric sister group to form I rubisco (named form I') has filled a key gap in our understanding of the enigmatic origins of the form I clade. However, to elucidate the series of molecular events leading to the evolution of form I rubisco, we must examine more distantly related sibling clades to contextualize the molecular features distinguishing form I and form I' rubiscos. Here, we present a comparative structural study retracing the evolutionary history of rubisco that reveals a complex structural trajectory leading to the ultimate hetero-oligomerization of the form I clade. We structurally characterize the oligomeric states of deep-branching form Iα and I'' rubiscos recently discovered from metagenomes, which represent key evolutionary intermediates preceding the form I clade. We further solve the structure of form I'' rubisco, revealing the molecular determinants that likely primed the enzyme core for the transition from a homo-oligomer to a hetero-oligomer. Our findings yield new insight into the evolutionary trajectory underpinning the adoption and entrenchment of the prevalent assembly of form I rubisco, providing additional context when viewing the enzyme family through the broader lens of protein evolution. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_41946.map.gz emd_41946.map.gz | 97.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-41946-v30.xml emd-41946-v30.xml emd-41946.xml emd-41946.xml | 19.2 KB 19.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
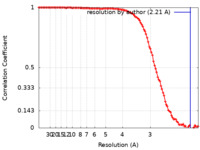
| FSC (解像度算出) |  emd_41946_fsc.xml emd_41946_fsc.xml | 13.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_41946.png emd_41946.png | 39.6 KB | ||
| Filedesc metadata |  emd-41946.cif.gz emd-41946.cif.gz | 6.4 KB | ||
| その他 |  emd_41946_half_map_1.map.gz emd_41946_half_map_1.map.gz emd_41946_half_map_2.map.gz emd_41946_half_map_2.map.gz | 95.3 MB 95.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-41946 http://ftp.pdbj.org/pub/emdb/structures/EMD-41946 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41946 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41946 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_41946.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_41946.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.05 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_41946_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
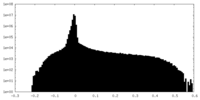
| 投影像・断面図 |
| ||||||||||||
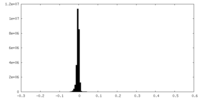
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_41946_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
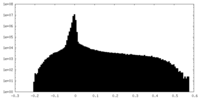
| 投影像・断面図 |
| ||||||||||||
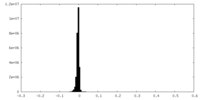
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : RUBISCO octamer
| 全体 | 名称: RUBISCO octamer |
|---|---|
| 要素 |
|
-超分子 #1: RUBISCO octamer
| 超分子 | 名称: RUBISCO octamer / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Bacillota (バクテリア) Bacillota (バクテリア) |
-分子 #1: Rubisco
| 分子 | 名称: Rubisco / タイプ: protein_or_peptide / ID: 1 / コピー数: 8 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Bacillota (バクテリア) Bacillota (バクテリア) |
| 分子量 | 理論値: 50.978855 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MARQQFVAGV QPYRKTYYEP GYEPKETDLL CAFRIEPSPG IPLEEAAAAV AAESSTGTWT EVWSQEMTDL HRYKGRCYAI DGNTAYIAY PLDLFEEGSI VNVMSSIVGN VFGFKAVRAL RLLDMRIPTA YLKTFPGPPT GIAQERDRLK VYHRPLLGGT I KPKLGLGP ...文字列: MARQQFVAGV QPYRKTYYEP GYEPKETDLL CAFRIEPSPG IPLEEAAAAV AAESSTGTWT EVWSQEMTDL HRYKGRCYAI DGNTAYIAY PLDLFEEGSI VNVMSSIVGN VFGFKAVRAL RLLDMRIPTA YLKTFPGPPT GIAQERDRLK VYHRPLLGGT I KPKLGLGP KEFARVVYEC LVGGLDTT(KCX)D DENLNSQPFC RWRDRYLYVM DAVHRAEEET GEAKGHWLNV TAGDTEEM L RRAEFAKEVG SRYIMVDFLT AGFSAYATLR RRAEELGLMI HCHRAMHAVF TRPKDHGIHF RVVAKWLRMA GGDHVHTGT VVGKLEGARE EVRGIADLLR EEFVPANPQR GLLFDQPWAG LKPLFPVASG GIHVWHVPDL VSIYGNDAFF LFGGGTHGHP RGSRAGARA NRAAVEAVAA AYREGRDILA EGRQILQDAA RTCPELREAM ELWEGVTFGE E |
-分子 #2: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 2 / コピー数: 8 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-分子 #3: 2-CARBOXYARABINITOL-1,5-DIPHOSPHATE
| 分子 | 名称: 2-CARBOXYARABINITOL-1,5-DIPHOSPHATE / タイプ: ligand / ID: 3 / コピー数: 8 / 式: CAP |
|---|---|
| 分子量 | 理論値: 356.115 Da |
| Chemical component information |  ChemComp-CAP: |
-分子 #4: water
| 分子 | 名称: water / タイプ: ligand / ID: 4 / コピー数: 981 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| 凍結 | 凍結剤: ETHANE-PROPANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 81000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)