+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the human cholesterol transporter ABCG1 in complex with cholesterol | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Human ABCG1 / cholsterol transporter / ATP-bound / cholesterol / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報ABC-type sterol transporter activity / glycoprotein transport / cellular response to high density lipoprotein particle stimulus / intracellular cholesterol transport / toxin transmembrane transporter activity / ABC transporters in lipid homeostasis / floppase activity / positive regulation of cholesterol biosynthetic process / phosphatidylcholine floppase activity / phospholipid homeostasis ...ABC-type sterol transporter activity / glycoprotein transport / cellular response to high density lipoprotein particle stimulus / intracellular cholesterol transport / toxin transmembrane transporter activity / ABC transporters in lipid homeostasis / floppase activity / positive regulation of cholesterol biosynthetic process / phosphatidylcholine floppase activity / phospholipid homeostasis / high-density lipoprotein particle remodeling / phospholipid efflux / reverse cholesterol transport / cholesterol transfer activity / トランスロカーゼ; 他の化合物の輸送を触媒; ヌクレオシド三リン酸の加水分解に伴う / low-density lipoprotein particle remodeling / HDL remodeling / cholesterol efflux / regulation of cholesterol metabolic process / positive regulation of amyloid-beta formation / response to lipid / cholesterol binding / negative regulation of cholesterol storage / amyloid precursor protein catabolic process / negative regulation of macrophage derived foam cell differentiation / positive regulation of cholesterol efflux / NR1H3 & NR1H2 regulate gene expression linked to cholesterol transport and efflux / cholesterol metabolic process / : / cholesterol homeostasis / positive regulation of protein secretion / recycling endosome / phospholipid binding / transmembrane transport / ADP binding / endosome / protein heterodimerization activity / external side of plasma membrane / Golgi membrane / endoplasmic reticulum membrane / Golgi apparatus / protein homodimerization activity / ATP hydrolysis activity / mitochondrion / ATP binding / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.26 Å | |||||||||
 データ登録者 データ登録者 | Xu D / Li YY / Yang FR / Sun CR / Pan JH / Wang L / Chen ZP / Fang SC / Yao XB / Hou WT ...Xu D / Li YY / Yang FR / Sun CR / Pan JH / Wang L / Chen ZP / Fang SC / Yao XB / Hou WT / Zhou CZ / Chen Y | |||||||||
| 資金援助 |  中国, 1件 中国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Cell Rep / 年: 2022 ジャーナル: Cell Rep / 年: 2022タイトル: Structure and transport mechanism of the human cholesterol transporter ABCG1. 著者: Da Xu / Yanyan Li / Fengrui Yang / Cai-Rong Sun / Jinheng Pan / Liang Wang / Zhi-Peng Chen / Shu-Cheng Fang / Xuebiao Yao / Wen-Tao Hou / Cong-Zhao Zhou / Yuxing Chen /  要旨: The reverse cholesterol transport pathway is responsible for the maintenance of human cholesterol homeostasis, an imbalance of which usually leads to atherosclerosis. As a key component of this ...The reverse cholesterol transport pathway is responsible for the maintenance of human cholesterol homeostasis, an imbalance of which usually leads to atherosclerosis. As a key component of this pathway, the ATP-binding cassette transporter ABCG1 forwards cellular cholesterol to the extracellular acceptor nascent high-density lipoprotein (HDL). Here, we report a 3.26-Å cryo-electron microscopy structure of cholesterol-bound ABCG1 in an inward-facing conformation, which represents a turnover condition upon ATP binding. Structural analyses combined with functional assays reveals that a cluster of conserved hydrophobic residues, in addition to two sphingomyelins, constitute a well-defined cholesterol-binding cavity. The exit of this cavity is closed by three pairs of conserved Phe residues, which constitute a hydrophobic path for the release of cholesterol in an acceptor concentration-dependent manner. Overall, we propose an ABCG1-driven cholesterol transport cycle initiated by sphingomyelin-assisted cholesterol recruitment and accomplished by the release of cholesterol to HDL. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_31547.map.gz emd_31547.map.gz | 49.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-31547-v30.xml emd-31547-v30.xml emd-31547.xml emd-31547.xml | 12.4 KB 12.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_31547.png emd_31547.png | 34.1 KB | ||
| Filedesc metadata |  emd-31547.cif.gz emd-31547.cif.gz | 5.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-31547 http://ftp.pdbj.org/pub/emdb/structures/EMD-31547 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-31547 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-31547 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_31547_validation.pdf.gz emd_31547_validation.pdf.gz | 514 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_31547_full_validation.pdf.gz emd_31547_full_validation.pdf.gz | 513.6 KB | 表示 | |
| XML形式データ |  emd_31547_validation.xml.gz emd_31547_validation.xml.gz | 6.1 KB | 表示 | |
| CIF形式データ |  emd_31547_validation.cif.gz emd_31547_validation.cif.gz | 6.9 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-31547 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-31547 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-31547 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-31547 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7fdvMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_31547.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_31547.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.01 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : The complex of human ABCG1 with cholesterol and ATP
| 全体 | 名称: The complex of human ABCG1 with cholesterol and ATP |
|---|---|
| 要素 |
|
-超分子 #1: The complex of human ABCG1 with cholesterol and ATP
| 超分子 | 名称: The complex of human ABCG1 with cholesterol and ATP / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 152 KDa |
-分子 #1: ATP-binding cassette sub-family G member 1
| 分子 | 名称: ATP-binding cassette sub-family G member 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO EC番号: トランスロカーゼ; 他の化合物の輸送を触媒; ヌクレオシド三リン酸の加水分解に伴う |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 75.670844 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MACLMAAFSV GTAMNASSYS AEMTEPKSVC VSVDEVVSSN MEATETDLLN GHLKKVDNNL TEAQRFSSLP RRAAVNIEFR DLSYSVPEG PWWRKKGYKT LLKGISGKFN SGELVAIMGP SGAGKSTLMN ILAGYRETGM KGAVLINGLP RDLRCFRKVS C YIMQDDML ...文字列: MACLMAAFSV GTAMNASSYS AEMTEPKSVC VSVDEVVSSN MEATETDLLN GHLKKVDNNL TEAQRFSSLP RRAAVNIEFR DLSYSVPEG PWWRKKGYKT LLKGISGKFN SGELVAIMGP SGAGKSTLMN ILAGYRETGM KGAVLINGLP RDLRCFRKVS C YIMQDDML LPHLTVQEAM MVSAHLKLQE KDEGRREMVK EILTALGLLS CANTRTGSLS GGQRKRLAIA LELVNNPPVM FF DQPTSGL DSASCFQVVS LMKGLAQGGR SIICTIHQPS AKLFELFDQL YVLSQGQCVY RGKVCNLVPY LRDLGLNCPT YHN PADFVM EVASGEYGDQ NSRLVRAVRE GMCDSDHKRD LGGDAEVNPF LWHRPSEEVK QTKRLKGLRK DSSSMEGCHS FSAS CLTQF CILFKRTFLS IMRDSVLTHL RITSHIGIGL LIGLLYLGIG NEAKKVLSNS GFLFFSMLFL MFAALMPTVL TFPLE MGVF LREHLNYWYS LKAYYLAKTM ADVPFQIMFP VAYCSIVYWM TSQPSDAVRF VLFAALGTMT SLVAQSLGLL IGAAST SLQ VATFVGPVTA IPVLLFSGFF VSFDTIPTYL QWMSYISYVR YGFEGVILSI YGLDREDLHC DIDETCHFQK SEAILRE LD VENAKLYLDF IVLGIFFISL RLIAYFVLRY KIRAER UniProtKB: ATP-binding cassette sub-family G member 1 |
-分子 #2: ADENOSINE-5'-TRIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-TRIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 2 / 式: ATP |
|---|---|
| 分子量 | 理論値: 507.181 Da |
| Chemical component information |  ChemComp-ATP: |
-分子 #3: [(E,2S,3R)-2-(hexadecanoylamino)-3-oxidanyl-octadec-4-enyl] 2-(tr...
| 分子 | 名称: [(E,2S,3R)-2-(hexadecanoylamino)-3-oxidanyl-octadec-4-enyl] 2-(trimethylazaniumyl)ethyl phosphate タイプ: ligand / ID: 3 / コピー数: 2 / 式: HWP |
|---|---|
| 分子量 | 理論値: 703.028 Da |
| Chemical component information | 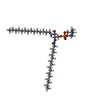 ChemComp-HWP: |
-分子 #4: CHOLESTEROL
| 分子 | 名称: CHOLESTEROL / タイプ: ligand / ID: 4 / コピー数: 2 / 式: CLR |
|---|---|
| 分子量 | 理論値: 386.654 Da |
| Chemical component information |  ChemComp-CLR: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 時間: 10 sec. / 前処理 - 雰囲気: OTHER |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 281 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 57.6 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.2 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: INSILICO MODEL |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 3.26 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 151593 |
| 初期 角度割当 | タイプ: PROJECTION MATCHING |
| 最終 角度割当 | タイプ: PROJECTION MATCHING |
-原子モデル構築 1
| 精密化 | プロトコル: AB INITIO MODEL / 温度因子: 142 |
|---|---|
| 得られたモデル |  PDB-7fdv: |
 ムービー
ムービー コントローラー
コントローラー












