+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of Type II Prion filaments from Gerstmann-Straussler-Scheinker disease | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Prion / PrP / GSS / filament / fibril / human brain derived / neurodegenerative / PROTEIN FIBRIL | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報positive regulation of glutamate receptor signaling pathway / negative regulation of amyloid precursor protein catabolic process / lamin binding / regulation of glutamate receptor signaling pathway / regulation of calcium ion import across plasma membrane / aspartic-type endopeptidase inhibitor activity / glycosaminoglycan binding / ATP-dependent protein binding / NCAM1 interactions / negative regulation of interleukin-17 production ...positive regulation of glutamate receptor signaling pathway / negative regulation of amyloid precursor protein catabolic process / lamin binding / regulation of glutamate receptor signaling pathway / regulation of calcium ion import across plasma membrane / aspartic-type endopeptidase inhibitor activity / glycosaminoglycan binding / ATP-dependent protein binding / NCAM1 interactions / negative regulation of interleukin-17 production / regulation of potassium ion transmembrane transport / type 5 metabotropic glutamate receptor binding / negative regulation of dendritic spine maintenance / cupric ion binding / negative regulation of protein processing / dendritic spine maintenance / negative regulation of calcineurin-NFAT signaling cascade / negative regulation of T cell receptor signaling pathway / Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / negative regulation of interleukin-2 production / extrinsic component of membrane / negative regulation of amyloid-beta formation / negative regulation of activated T cell proliferation / cuprous ion binding / response to amyloid-beta / negative regulation of type II interferon production / negative regulation of long-term synaptic potentiation / intracellular copper ion homeostasis / positive regulation of protein targeting to membrane / long-term memory / response to cadmium ion / regulation of peptidyl-tyrosine phosphorylation / inclusion body / cellular response to copper ion / neuron projection maintenance / positive regulation of calcium-mediated signaling / tubulin binding / negative regulation of protein phosphorylation / molecular function activator activity / positive regulation of protein localization to plasma membrane / molecular condensate scaffold activity / protein destabilization / protein homooligomerization / negative regulation of DNA-binding transcription factor activity / terminal bouton / positive regulation of peptidyl-tyrosine phosphorylation / cellular response to amyloid-beta / positive regulation of neuron apoptotic process / cellular response to xenobiotic stimulus / signaling receptor activity / protein-folding chaperone binding / amyloid-beta binding / microtubule binding / protease binding / nuclear membrane / transmembrane transporter binding / response to oxidative stress / postsynapse / molecular adaptor activity / postsynaptic density / learning or memory / regulation of cell cycle / membrane raft / copper ion binding / external side of plasma membrane / intracellular membrane-bounded organelle / dendrite / protein-containing complex binding / negative regulation of apoptotic process / Golgi apparatus / cell surface / endoplasmic reticulum / extracellular exosome / identical protein binding / plasma membrane / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 3.13 Å | |||||||||
 データ登録者 データ登録者 | Ozcan KO / Hoq MR / Bharath SR / Jiang W | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Acta Neuropathol / 年: 2022 ジャーナル: Acta Neuropathol / 年: 2022タイトル: Cryo-EM structures of prion protein filaments from Gerstmann-Sträussler-Scheinker disease. 著者: Grace I Hallinan / Kadir A Ozcan / Md Rejaul Hoq / Laura Cracco / Frank S Vago / Sakshibeedu R Bharath / Daoyi Li / Max Jacobsen / Emma H Doud / Amber L Mosley / Anllely Fernandez / Holly J ...著者: Grace I Hallinan / Kadir A Ozcan / Md Rejaul Hoq / Laura Cracco / Frank S Vago / Sakshibeedu R Bharath / Daoyi Li / Max Jacobsen / Emma H Doud / Amber L Mosley / Anllely Fernandez / Holly J Garringer / Wen Jiang / Bernardino Ghetti / Ruben Vidal /  要旨: Prion protein (PrP) aggregation and formation of PrP amyloid (APrP) are central events in the pathogenesis of prion diseases. In the dominantly inherited prion protein amyloidosis known as Gerstmann- ...Prion protein (PrP) aggregation and formation of PrP amyloid (APrP) are central events in the pathogenesis of prion diseases. In the dominantly inherited prion protein amyloidosis known as Gerstmann-Sträussler-Scheinker (GSS) disease, plaques made of PrP amyloid are present throughout the brain. The c.593t > c mutation in the prion protein gene (PRNP) results in a phenylalanine to serine amino acid substitution at PrP residue 198 (F198S) and causes the most severe amyloidosis among GSS variants. It has been shown that neurodegeneration in this disease is associated with the presence of extracellular APrP plaques and neuronal intracytoplasmic Tau inclusions, that have been shown to contain paired helical filaments identical to those found in Alzheimer disease. Using cryogenic electron microscopy (cryo-EM), we determined for the first time the structures of filaments of human APrP, isolated post-mortem from the brain of two symptomatic PRNP F198S mutation carriers. We report that in GSS (F198S) APrP filaments are composed of dimeric, trimeric and tetrameric left-handed protofilaments with their protomers sharing a common protein fold. The protomers in the cross-β spines consist of 62 amino acids and span from glycine 80 to phenylalanine 141, adopting a previously unseen spiral fold with a thicker outer layer and a thinner inner layer. Each protomer comprises nine short β-strands, with the β1 and β8 strands, as well as the β4 and β9 strands, forming a steric zipper. The data obtained by cryo-EM provide insights into the structural complexity of the PrP filament in a dominantly inherited human PrP amyloidosis. The novel findings highlight the urgency of extending our knowledge of the filaments' structures that may underlie distinct clinical and pathologic phenotypes of human neurodegenerative diseases. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_26613.map.gz emd_26613.map.gz | 103.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-26613-v30.xml emd-26613-v30.xml emd-26613.xml emd-26613.xml | 18.7 KB 18.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_26613.png emd_26613.png | 71.2 KB | ||
| Filedesc metadata |  emd-26613.cif.gz emd-26613.cif.gz | 5.6 KB | ||
| その他 |  emd_26613_additional_1.map.gz emd_26613_additional_1.map.gz emd_26613_half_map_1.map.gz emd_26613_half_map_1.map.gz emd_26613_half_map_2.map.gz emd_26613_half_map_2.map.gz | 47.7 MB 41.8 MB 41.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-26613 http://ftp.pdbj.org/pub/emdb/structures/EMD-26613 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-26613 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-26613 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_26613_validation.pdf.gz emd_26613_validation.pdf.gz | 841 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_26613_full_validation.pdf.gz emd_26613_full_validation.pdf.gz | 840.6 KB | 表示 | |
| XML形式データ |  emd_26613_validation.xml.gz emd_26613_validation.xml.gz | 14.4 KB | 表示 | |
| CIF形式データ |  emd_26613_validation.cif.gz emd_26613_validation.cif.gz | 16.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26613 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26613 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26613 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26613 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7un5MC  7umqC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_26613.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_26613.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
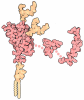
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.078 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: #1
| ファイル | emd_26613_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_26613_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_26613_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Type II Prion protein filament from Gerstmann-Straussler-Scheinke...
| 全体 | 名称: Type II Prion protein filament from Gerstmann-Straussler-Scheinker disease |
|---|---|
| 要素 |
|
-超分子 #1: Type II Prion protein filament from Gerstmann-Straussler-Scheinke...
| 超分子 | 名称: Type II Prion protein filament from Gerstmann-Straussler-Scheinker disease タイプ: tissue / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Brain / 組織: Cerebellum Homo sapiens (ヒト) / 器官: Brain / 組織: Cerebellum |
-分子 #1: Major prion protein
| 分子 | 名称: Major prion protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 10 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Brain / 組織: Cerebellum Homo sapiens (ヒト) / 器官: Brain / 組織: Cerebellum |
| 分子量 | 理論値: 6.219043 KDa |
| 配列 | 文字列: GWGQPHGGGW GQGGGTHSQW NKPSKPKTNM KHMAGAAAAG AVVGGLGGYV LGSAMSRPII HF UniProtKB: Major prion protein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 8 構成要素:
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: GRAPHENE OXIDE / 支持フィルム - トポロジー: CONTINUOUS / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 10 sec. / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.002 kPa 詳細: Glow discharged using PELCO easiGlow at 15 mA for 10 seconds. | ||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 293 K / 装置: GATAN CRYOPLUNGE 3 / 詳細: Plunge frozen in a BSL-2 hood. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 撮影したグリッド数: 1 / 実像数: 8600 / 平均電子線量: 56.5 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.4 µm / 倍率(公称値): 81000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 想定した対称性 - らせんパラメータ - Δz: 4.83 Å 想定した対称性 - らせんパラメータ - ΔΦ: -0.94 ° 想定した対称性 - らせんパラメータ - 軸対称性: C1 (非対称) 解像度のタイプ: BY AUTHOR / 解像度: 3.13 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: RELION (ver. 3.1) / 使用した粒子像数: 19341 |
|---|---|
| 初期モデル | モデルのタイプ: NONE |
| 最終 角度割当 | タイプ: NOT APPLICABLE |
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-7un5: |
 ムービー
ムービー コントローラー
コントローラー







 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)












































