[日本語] English
 万見
万見- EMDB-23626: cryo-EM Structure of Nucleosome containing mouse histone variant H2A.Z -
+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-23626 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | cryo-EM Structure of Nucleosome containing mouse histone variant H2A.Z | |||||||||
 マップデータ マップデータ | cryo-EM map of nucleosome containing histone variant H2A.Z | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | chromatin / nucleosome / histone variant / epigenetics / transcription / DNA BINDING PROTEIN / DNA BINDING PROTEIN-DNA complex | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報RNA polymerase II core promoter sequence-specific DNA binding / heterochromatin / heterochromatin organization / nucleosomal DNA binding / cellular response to estradiol stimulus / euchromatin / cellular response to insulin stimulus / structural constituent of chromatin / nucleosome / nucleosome assembly ...RNA polymerase II core promoter sequence-specific DNA binding / heterochromatin / heterochromatin organization / nucleosomal DNA binding / cellular response to estradiol stimulus / euchromatin / cellular response to insulin stimulus / structural constituent of chromatin / nucleosome / nucleosome assembly / chromatin organization / protein heterodimerization activity / RNA polymerase II cis-regulatory region sequence-specific DNA binding / positive regulation of transcription by RNA polymerase II / DNA binding / nucleus 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
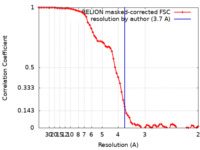
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.7 Å | |||||||||
 データ登録者 データ登録者 | Tan D / Lewis T | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nucleic Acids Res / 年: 2021 ジャーナル: Nucleic Acids Res / 年: 2021タイトル: Structural basis of chromatin regulation by histone variant H2A.Z. 著者: Tyler S Lewis / Vladyslava Sokolova / Harry Jung / Honkit Ng / Dongyan Tan /  要旨: The importance of histone variant H2A.Z in transcription regulation has been well established, yet its mechanism-of-action remains enigmatic. Conflicting evidence exists in support of both an ...The importance of histone variant H2A.Z in transcription regulation has been well established, yet its mechanism-of-action remains enigmatic. Conflicting evidence exists in support of both an activating and a repressive role of H2A.Z in transcription. Here we report cryo-electron microscopy (cryo-EM) structures of nucleosomes and chromatin fibers containing H2A.Z and those containing canonical H2A. The structures show that H2A.Z incorporation results in substantial structural changes in both nucleosome and chromatin fiber. While H2A.Z increases the mobility of DNA terminus in nucleosomes, it simultaneously enables nucleosome arrays to form a more regular and condensed chromatin fiber. We also demonstrated that H2A.Z's ability to enhance nucleosomal DNA mobility is largely attributed to its characteristic shorter C-terminus. Our study provides the structural basis for H2A.Z-mediated chromatin regulation, showing that the increase flexibility of the DNA termini in H2A.Z nucleosomes is central to its dual-functions in chromatin regulation and in transcription. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_23626.map.gz emd_23626.map.gz | 26.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-23626-v30.xml emd-23626-v30.xml emd-23626.xml emd-23626.xml | 26.7 KB 26.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_23626_fsc.xml emd_23626_fsc.xml | 6.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_23626.png emd_23626.png | 199.4 KB | ||
| Filedesc metadata |  emd-23626.cif.gz emd-23626.cif.gz | 6.8 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-23626 http://ftp.pdbj.org/pub/emdb/structures/EMD-23626 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-23626 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-23626 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_23626_validation.pdf.gz emd_23626_validation.pdf.gz | 406 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_23626_full_validation.pdf.gz emd_23626_full_validation.pdf.gz | 405.6 KB | 表示 | |
| XML形式データ |  emd_23626_validation.xml.gz emd_23626_validation.xml.gz | 9.2 KB | 表示 | |
| CIF形式データ |  emd_23626_validation.cif.gz emd_23626_validation.cif.gz | 11.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23626 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23626 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23626 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-23626 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_23626.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_23626.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | cryo-EM map of nucleosome containing histone variant H2A.Z | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.1 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : Nucleosome core particle containing variant H2A.Z and canonical c...
+超分子 #1: Nucleosome core particle containing variant H2A.Z and canonical c...
+超分子 #2: Histone H3
+超分子 #3: Histone H4
+超分子 #4: Histone variant H2A.Z
+超分子 #5: Histone H2B
+超分子 #6: DNA (136-MER)
+超分子 #7: DNA (136-MER)
+分子 #1: DNA (136-MER)
+分子 #2: DNA (136-MER)
+分子 #3: Histone H3
+分子 #4: Histone H4
+分子 #5: Histone H2A.Z
+分子 #6: Histone H2B 1.1
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| |||||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 30 sec. / 前処理 - 雰囲気: AIR | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV / 詳細: blot for 4.5 seconds before plunging. | |||||||||||||||
| 詳細 | This sample was mono-disperse. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 3 / 実像数: 1950 / 平均露光時間: 60.0 sec. / 平均電子線量: 33.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 倍率(補正後): 123811 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 92000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル |
| ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT / 当てはまり具合の基準: rmsd | ||||||||||||||||||||||
| 得られたモデル |  PDB-7m1x: |
 ムービー
ムービー コントローラー
コントローラー