+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of the human Commander complex COMMD ring | |||||||||||||||
 マップデータ マップデータ | ||||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | COMMD fold / calponin homology fold / pseudo-C5 symmetry / UNKNOWN FUNCTION | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報negative regulation of sodium ion transmembrane transport / plasma membrane to endosome transport / cytoplasmic sequestering of NF-kappaB / regulation of proteasomal ubiquitin-dependent protein catabolic process / negative regulation of protein localization to cell surface / copper ion homeostasis / Golgi to plasma membrane transport / phosphatidic acid binding / positive regulation of ubiquitin-dependent protein catabolic process / phosphatidylinositol-3,4-bisphosphate binding ...negative regulation of sodium ion transmembrane transport / plasma membrane to endosome transport / cytoplasmic sequestering of NF-kappaB / regulation of proteasomal ubiquitin-dependent protein catabolic process / negative regulation of protein localization to cell surface / copper ion homeostasis / Golgi to plasma membrane transport / phosphatidic acid binding / positive regulation of ubiquitin-dependent protein catabolic process / phosphatidylinositol-3,4-bisphosphate binding / endocytic recycling / sodium channel inhibitor activity / phosphatidylinositol-3,5-bisphosphate binding / Cul2-RING ubiquitin ligase complex / sodium ion transport / negative regulation of NF-kappaB transcription factor activity / phosphatidylinositol-3,4,5-trisphosphate binding / cullin family protein binding / NF-kappaB binding / intracellular copper ion homeostasis / negative regulation of canonical NF-kappaB signal transduction / tumor necrosis factor-mediated signaling pathway / phosphatidylinositol-4,5-bisphosphate binding / positive regulation of protein ubiquitination / cholesterol homeostasis / nucleotide-excision repair / recycling endosome / protein transport / Neddylation / cytoplasmic vesicle / secretory granule lumen / positive regulation of canonical NF-kappaB signal transduction / ficolin-1-rich granule lumen / early endosome / endosome membrane / endosome / copper ion binding / intracellular membrane-bounded organelle / negative regulation of DNA-templated transcription / centrosome / Neutrophil degranulation / Golgi apparatus / protein homodimerization activity / extracellular region / nucleoplasm / identical protein binding / nucleus / plasma membrane / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||||||||
 データ登録者 データ登録者 | Kumpula EP / Laulumaa S / Huiskonen JT | |||||||||||||||
| 資金援助 |  フィンランド, 4件 フィンランド, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2024 ジャーナル: Nat Struct Mol Biol / 年: 2024タイトル: Structure and interactions of the endogenous human Commander complex. 著者: Saara Laulumaa / Esa-Pekka Kumpula / Juha T Huiskonen / Markku Varjosalo /  要旨: The Commander complex, a 16-protein assembly, plays multiple roles in cell homeostasis, cell cycle and immune response. It consists of copper-metabolism Murr1 domain proteins (COMMD1-10), coiled-coil ...The Commander complex, a 16-protein assembly, plays multiple roles in cell homeostasis, cell cycle and immune response. It consists of copper-metabolism Murr1 domain proteins (COMMD1-10), coiled-coil domain-containing proteins (CCDC22 and CCDC93), DENND10 and the Retriever subcomplex (VPS26C, VPS29 and VPS35L), all expressed ubiquitously in the body and linked to various diseases. Here, we report the structure and key interactions of the endogenous human Commander complex by cryogenic-electron microscopy and mass spectrometry-based proteomics. The complex consists of a stable core of COMMD1-10 and an effector containing DENND10 and Retriever, scaffolded together by CCDC22 and CCDC93. We establish the composition of Commander and reveal major interaction interfaces. These findings clarify its roles in intracellular transport, and uncover a strong association with cilium assembly, and centrosome and centriole functions. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_17340.map.gz emd_17340.map.gz | 633.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-17340-v30.xml emd-17340-v30.xml emd-17340.xml emd-17340.xml | 29.4 KB 29.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_17340_fsc.xml emd_17340_fsc.xml | 18.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_17340.png emd_17340.png | 154.4 KB | ||
| マスクデータ |  emd_17340_msk_1.map emd_17340_msk_1.map | 669.9 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-17340.cif.gz emd-17340.cif.gz | 8.3 KB | ||
| その他 |  emd_17340_half_map_1.map.gz emd_17340_half_map_1.map.gz emd_17340_half_map_2.map.gz emd_17340_half_map_2.map.gz | 620.7 MB 620.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-17340 http://ftp.pdbj.org/pub/emdb/structures/EMD-17340 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17340 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17340 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_17340_validation.pdf.gz emd_17340_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_17340_full_validation.pdf.gz emd_17340_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_17340_validation.xml.gz emd_17340_validation.xml.gz | 28.3 KB | 表示 | |
| CIF形式データ |  emd_17340_validation.cif.gz emd_17340_validation.cif.gz | 37.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17340 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17340 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17340 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17340 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8p0wMC  8p0vC  8p0xC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_17340.map.gz / 形式: CCP4 / 大きさ: 669.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_17340.map.gz / 形式: CCP4 / 大きさ: 669.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.8464 Å | ||||||||||||||||||||
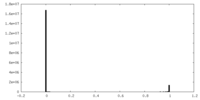
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_17340_msk_1.map emd_17340_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
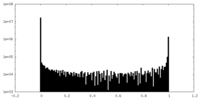
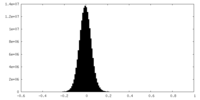
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_17340_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
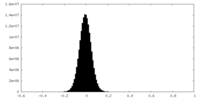
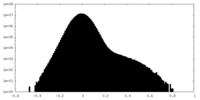
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_17340_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
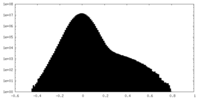
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : Human Commander Complex
+超分子 #1: Human Commander Complex
+分子 #1: COMM domain-containing protein 1
+分子 #2: COMM domain-containing protein 2
+分子 #3: COMM domain-containing protein 3
+分子 #4: COMM domain-containing protein 4
+分子 #5: COMM domain-containing protein 5
+分子 #6: COMM domain-containing protein 6
+分子 #7: COMM domain-containing protein 7
+分子 #8: COMM domain-containing protein 8
+分子 #9: COMM domain-containing protein 9
+分子 #10: COMM domain-containing protein 10
+分子 #11: Coiled-coil domain-containing protein 93
+分子 #12: Coiled-coil domain-containing protein 22
+分子 #13: water
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.1 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 支持フィルム - Film thickness: 2 / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 時間: 50 sec. / 前処理 - 気圧: 0.107 kPa |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 279 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 撮影したグリッド数: 2 / 実像数: 55769 / 平均電子線量: 59.0 e/Å2 詳細: Two datasets were collected from identical grids prepared in the same session. Dataset 1: 20675 movies 50 frames / movie 59 e-/A2 total dose Dataset 2: 35084 movies 45 frames / movie 56 e-/A2 total dose |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.6 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 105000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | Chain - Source name: AlphaFold / Chain - Initial model type: in silico model |
|---|---|
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT |
| 得られたモデル |  PDB-8p0w: |
 ムービー
ムービー コントローラー
コントローラー







 Z
Z Y
Y X
X