+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Complex C1 symmetry | |||||||||
 マップデータ マップデータ | Complex C1 symmetry | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | PROTEIN / STRUCTURAL PROTEIN / S-layer / deinococcus radiodurans / DR_2577 / S-layer Deinoxanthin Binding Complex | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報porin activity / pore complex / monoatomic ion transport / cell outer membrane / lipid binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Deinococcus radiodurans R1 (放射線耐性) Deinococcus radiodurans R1 (放射線耐性) | |||||||||
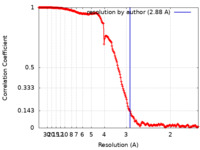
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.88 Å | |||||||||
 データ登録者 データ登録者 | Iesu L / de Sanctis D | |||||||||
| 資金援助 |  ポーランド, 2件 ポーランド, 2件
| |||||||||
 引用 引用 |  ジャーナル: J Biol Chem / 年: 2022 ジャーナル: J Biol Chem / 年: 2022タイトル: The cryo-EM structure of the S-layer deinoxanthin-binding complex of Deinococcus radiodurans informs properties of its environmental interactions. 著者: Domenica Farci / Patrycja Haniewicz / Daniele de Sanctis / Luca Iesu / Sami Kereïche / Mathias Winterhalter / Dario Piano /       要旨: The radiation-resistant bacterium Deinococcus radiodurans is known as the world's toughest bacterium. The S-layer of D. radiodurans, consisting of several proteins on the surface of the cellular ...The radiation-resistant bacterium Deinococcus radiodurans is known as the world's toughest bacterium. The S-layer of D. radiodurans, consisting of several proteins on the surface of the cellular envelope and intimately associated with the outer membrane, has therefore been useful as a model for structural and functional studies. Its main proteinaceous unit, the S-layer deinoxanthin-binding complex (SDBC), is a hetero-oligomeric assembly known to contribute to the resistance against environmental stress and have porin functional features; however, its precise structure is unknown. Here, we resolved the structure of the SDBC at ∼2.5 Å resolution by cryo-EM and assigned the sequence of its main subunit, the protein DR_2577. This structure is characterized by a pore region, a massive β-barrel organization, a stalk region consisting of a trimeric coiled coil, and a collar region at the base of the stalk. We show that each monomer binds three Cu ions and one Fe ion and retains one deinoxanthin molecule and two phosphoglycolipids, all exclusive to D. radiodurans. Finally, electrophysiological characterization of the SDBC shows that it exhibits transport properties with several amino acids. Taken together, these results highlight the SDBC as a robust structure displaying both protection and sieving functions that facilitates exchanges with the environment. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_14714.map.gz emd_14714.map.gz | 530.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-14714-v30.xml emd-14714-v30.xml emd-14714.xml emd-14714.xml | 15.2 KB 15.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_14714_fsc.xml emd_14714_fsc.xml | 18.3 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_14714.png emd_14714.png | 39 KB | ||
| Filedesc metadata |  emd-14714.cif.gz emd-14714.cif.gz | 5.7 KB | ||
| その他 |  emd_14714_half_map_1.map.gz emd_14714_half_map_1.map.gz emd_14714_half_map_2.map.gz emd_14714_half_map_2.map.gz | 521.6 MB 521.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-14714 http://ftp.pdbj.org/pub/emdb/structures/EMD-14714 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14714 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14714 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_14714_validation.pdf.gz emd_14714_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_14714_full_validation.pdf.gz emd_14714_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_14714_validation.xml.gz emd_14714_validation.xml.gz | 27.3 KB | 表示 | |
| CIF形式データ |  emd_14714_validation.cif.gz emd_14714_validation.cif.gz | 35.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14714 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14714 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14714 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14714 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7zgxMC  7zgyC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_14714.map.gz / 形式: CCP4 / 大きさ: 561.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_14714.map.gz / 形式: CCP4 / 大きさ: 561.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Complex C1 symmetry | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.818 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map A Complex C1 symmetry
| ファイル | emd_14714_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A Complex C1 symmetry | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map B Complex C1 symmetry
| ファイル | emd_14714_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B Complex C1 symmetry | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Complex C1 symmetry
| 全体 | 名称: Complex C1 symmetry |
|---|---|
| 要素 |
|
-超分子 #1: Complex C1 symmetry
| 超分子 | 名称: Complex C1 symmetry / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Deinococcus radiodurans R1 (放射線耐性) Deinococcus radiodurans R1 (放射線耐性) |
| 分子量 | 理論値: 800 KDa |
-分子 #1: S-layer protein SlpA
| 分子 | 名称: S-layer protein SlpA / タイプ: protein_or_peptide / ID: 1 / コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Deinococcus radiodurans R1 (放射線耐性) Deinococcus radiodurans R1 (放射線耐性)株: ATCC 13939 / DSM 20539 / JCM 16871 / LMG 4051 / NBRC 15346 / NCIMB 9279 / R1 / VKM B-1422 |
| 分子量 | 理論値: 123.835367 KDa |
| 配列 | 文字列: MKKSLIALTT ALSFGLAAAQ TAAPVSAPQV PALTDVPAGH WAKDAIDRLV SRGVILGYPD GTFRGTQNLT RYEAAIIIAR LLDQMRDGE TPAGMTAEDM TALQNAIQEL AADLAALGVR VSDLEANAVS KDDFARLEAR IEEVAAAGGE QGATEALQGQ I DDLTARVD ...文字列: MKKSLIALTT ALSFGLAAAQ TAAPVSAPQV PALTDVPAGH WAKDAIDRLV SRGVILGYPD GTFRGTQNLT RYEAAIIIAR LLDQMRDGE TPAGMTAEDM TALQNAIQEL AADLAALGVR VSDLEANAVS KDDFARLEAR IEEVAAAGGE QGATEALQGQ I DDLTARVD EYDALRADVD DNASSIAALN DLTVLLNQDI LDLQDRVSAV EAAQADFVQR SDFDALGGRV TTVETRVETV NN SLTGRIA ALERNAFSVK PSLTIGYSVS RTSRNFDVDR LFPLNADGTV ANNAFTSGGI DTDTGAQRRD FGDFGNASDP VVA GAAGLY GFADGVSYTV YFTDGSTATF DGLNPADYKV PTGKVIDTTK GRNGFGFNNL ARYKEGSTDI GISLGFDTSG QFSQ VTSGT GGSLFSTAGR LQVNQIDLNF GLVTGLPSDA YVDTNGNGKK DDGEATGRGT YLGSGGTAAI LRDPAGNVYR PVFFR FKNA TTQFSVGNNP VIVTLGQQQK FYFSDYVFDN NYDGRGDGFT VTVDGSNVPV IGAWKPQIKG VYGSRSGLDG TAEAGY GVY YRGVRAQITP VGTLTAGIHY AQEGRDMFGA AQNTTSTPSD VTTYGADLHG KAFGVELHSE YATSRVRPNT ANAAVQT SN AFYARVATRK DNLAFDLNTP AAKFGNDTFG VSLYDLNYRK IDAGYNNVAG ISEYGYGSYS RTSAQNIAYN PDTGVTAP F ANLDRQAYTD ANNDGTSDRN ADGTVVATNT KIGQMGFGVK AAANLGPVAI GGYYDTSTGA NGDNANRMTE AGGSAKVAY SIFSLRGTYN TLDSNRPQIY RDAAGTQIIG DAKVRRYAVQ ADVTPGLGLF VGAYYRDVNV NGVRSTTDRG LLGRGYLASS FEPGVGNNA YRTGLRCADN NFGTGTRDID GVGGVLNPAV NLDQSRTATC FTSYGVEAGH AGDNANALVK DLFFRVGYSR V YVPTTATA TTGDFSGSVT YGDARYDRKV GVANVRLAGS FSTTNTQLDS RPAGTRGAVG LIVRTDPLEN VPFRPQFNGQ VG YYTADNR VAAGNYNANA TKYGAGVVLN DFLLPQTKIG VRYDGYMAQN RQYTPFDGDG TQGYFSDANN NRRTNLNGVY VEG AYQDLI FSYGTYTLSQ KDLNGVEYGS GINNGQPARG QTFKISYKVN F UniProtKB: Outer membrane protein SlpA |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 平均電子線量: 1.3 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.0 µm / 最小 デフォーカス(公称値): 0.5 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー





 Z
Z Y
Y X
X