+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-13587 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Photorhabdus laumondii T6SS-associated Rhs protein carrying the Tre23 toxin domain | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | RHS / TVISS / T6SS / TOXIN | |||||||||
| 機能・相同性 | RHS repeat / RHS Repeat / PAAR motif / PAAR motif / YD repeat / Rhs repeat-associated core / membrane => GO:0016020 / Uncharacterized protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Photorhabdus laumondii (バクテリア) / Photorhabdus laumondii (バクテリア) /  Photorhabdus laumondii subsp. laumondii TTO1 (バクテリア) Photorhabdus laumondii subsp. laumondii TTO1 (バクテリア) | |||||||||
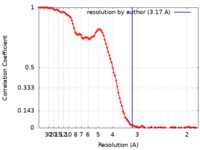
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.17 Å | |||||||||
 データ登録者 データ登録者 | Jurenas D / Talachia Rosa L | |||||||||
| 資金援助 |  フランス, 1件 フランス, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2021 ジャーナル: Nat Commun / 年: 2021タイトル: Mounting, structure and autocleavage of a type VI secretion-associated Rhs polymorphic toxin. 著者: Dukas Jurėnas / Leonardo Talachia Rosa / Martial Rey / Julia Chamot-Rooke / Rémi Fronzes / Eric Cascales /  要旨: Bacteria have evolved toxins to outcompete other bacteria or to hijack host cell pathways. One broad family of bacterial polymorphic toxins gathers multidomain proteins with a modular organization, ...Bacteria have evolved toxins to outcompete other bacteria or to hijack host cell pathways. One broad family of bacterial polymorphic toxins gathers multidomain proteins with a modular organization, comprising a C-terminal toxin domain fused to a N-terminal domain that adapts to the delivery apparatus. Polymorphic toxins include bacteriocins, contact-dependent growth inhibition systems, and specialized Hcp, VgrG, PAAR or Rhs Type VI secretion (T6SS) components. We recently described and characterized Tre23, a toxin domain fused to a T6SS-associated Rhs protein in Photorhabdus laumondii, Rhs1. Here, we show that Rhs1 forms a complex with the T6SS spike protein VgrG and the EagR chaperone. Using truncation derivatives and cross-linking mass spectrometry, we demonstrate that VgrG-EagR-Rhs1 complex formation requires the VgrG C-terminal β-helix and the Rhs1 N-terminal region. We then report the cryo-electron-microscopy structure of the Rhs1-EagR complex, demonstrating that the Rhs1 central region forms a β-barrel cage-like structure that encapsulates the C-terminal toxin domain, and provide evidence for processing of the Rhs1 protein through aspartyl autoproteolysis. We propose a model for Rhs1 loading on the T6SS, transport and delivery into the target cell. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_13587.map.gz emd_13587.map.gz | 65.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-13587-v30.xml emd-13587-v30.xml emd-13587.xml emd-13587.xml | 17.8 KB 17.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_13587_fsc.xml emd_13587_fsc.xml | 12.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_13587.png emd_13587.png | 49.6 KB | ||
| マスクデータ |  emd_13587_msk_1.map emd_13587_msk_1.map | 83.7 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-13587.cif.gz emd-13587.cif.gz | 6.6 KB | ||
| その他 |  emd_13587_half_map_1.map.gz emd_13587_half_map_1.map.gz emd_13587_half_map_2.map.gz emd_13587_half_map_2.map.gz | 65.5 MB 65.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-13587 http://ftp.pdbj.org/pub/emdb/structures/EMD-13587 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13587 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13587 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_13587_validation.pdf.gz emd_13587_validation.pdf.gz | 946.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_13587_full_validation.pdf.gz emd_13587_full_validation.pdf.gz | 946.6 KB | 表示 | |
| XML形式データ |  emd_13587_validation.xml.gz emd_13587_validation.xml.gz | 16.9 KB | 表示 | |
| CIF形式データ |  emd_13587_validation.cif.gz emd_13587_validation.cif.gz | 22.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13587 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13587 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13587 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13587 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_13587.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_13587.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.93 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_13587_msk_1.map emd_13587_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
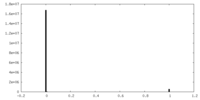
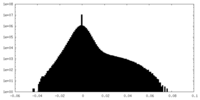
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_13587_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
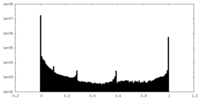
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_13587_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
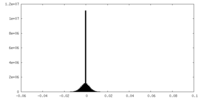
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Tre23
| 全体 | 名称: Tre23 |
|---|---|
| 要素 |
|
-超分子 #1: Tre23
| 超分子 | 名称: Tre23 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Photorhabdus laumondii (バクテリア) Photorhabdus laumondii (バクテリア) |
-分子 #1: Tre23
| 分子 | 名称: Tre23 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Photorhabdus laumondii subsp. laumondii TTO1 (バクテリア) Photorhabdus laumondii subsp. laumondii TTO1 (バクテリア) |
| 分子量 | 理論値: 165.588828 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSLGDEIVTR IARVGARHAV HVSPPQGSPG PAAAREGDPI KHASFLGALA GAITGALIGA AVFAAASALV GLTILTGGLA TVAVIALGT AATFALGDVI SAASSAVTNM VDSIGPPSGT LTSGSPNVFI EGQPAARATT DIAVCSKHPA PPLIAQGSET V LINGSPAA ...文字列: MSLGDEIVTR IARVGARHAV HVSPPQGSPG PAAAREGDPI KHASFLGALA GAITGALIGA AVFAAASALV GLTILTGGLA TVAVIALGT AATFALGDVI SAASSAVTNM VDSIGPPSGT LTSGSPNVFI EGQPAARATT DIAVCSKHPA PPLIAQGSET V LINGSPAA RVDDKLACGA TIKSGAKTVF IGSGQGTYLA VADEFSAWER AILIAVEFLV PPSRGALKGL GKLFTKPGQG IQ GVLKGAK AGAKKAKALL SNRISCAKKA FRETEGAKRY REATKKFFTG DPIDVTTGQL FDQRTDITLG QTLPLVFLRS WVP EEQGLL GPGWTDSFSE CALATGDRVE IRTTEGASLY FALPAAYTHS VNPDHPDFTL SRGEQGYILR HRDSPVSKYF TLPH PSSAS KEAPRRWLLT EHRDVYDNRL RFIYNKHCQL TQVLHSDGPE LTLLYNLRGQ LTEIRRTDER LQEVMARYHY HDNGR LAEA DSTQNFHLYY EYNAQGLISR WSDGDQTWVD YRYDKQGRCT DSVGAGGFYP VHLDYAPGIT RSTTPQGHTT TGHYND QQL ITEIHTPCGG VTRYEYDRWG NLVRQILPEG ETLTLTYLAD TGRVTSLTEA TGAVWQYSYE ADSLQLTGMT DPLQRTW LP QYDEQGQPAG FIAPDGRKTT LTRNAFGLVT SETDPDGNSR TQEYDKHQRL VRVLDEENRT VSLGYDSQDR LRSLTAAG A LWRWRYDRHH RVAVSDRPDN QLEHFTHDRH GNLTCWTDAR GVKWQVEYGP FDLPVARRDG EGHRWQYRYD ADTLQLTQV INPQGETYSY TLDADGRVIT EQDYAGTQWH YRYDRSGNCI EKRDGEENVT RYDYDAARRL TTLHTPEGPT RYHYDSVGRL LTVDSPDST LHFEYDGQDR IVREIQPHGE IQRHYPDNRT AERQLLTGET APVTGPARFS GQTHPGRWQS RREVNRVGEL I TLTLAGQA PLTIERDDAG RDTGRYVDGG FILRQQYSLM GQLTAQRAGR NPYFFRPAEP DEIEGPAYAG VARRYEYDTA LN LTAASDD GQQVNYLLNG NGQVISVGEG RTLREHYQYD ETGYPSRRFD GVQEIMGETL YQEGHRLNWV GSHRFVYDRA GRM QEKQFL AEGCRLALTK YRWNSQNQLT GLITPDGIPW EYRYDAFGRR TEKRCIQSGK LTTYLWDGNV PAEIREYQHG RLKM IRHLV FDGWELVAQQ TQAFTLNLDN RVELMAGEVQ TQYAVSAPTG EPLALFDPAG KRVWRRPKQS LYGLRLGGYG ENPQL DPGL RFAGQLFDEE SGLFYNRFRY YLPEATCYLS PDPTGLWGGE NTYRYVQNPT KFINPLGLAG ENVFIHATNK AGFDGI MKS GVLHPNVSGK VAITDVLMSP KDVMRDLLIN NPNHIGRGDY AIIFKIDPGE RGNIRSPSRL EYTHEGKLKL NNILYAG KN PYAILEHLDY DTRLKLTDNQ VKIRKCGGKV DDYKDDDDK UniProtKB: Uncharacterized protein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 8.5 詳細: 50 mM Tris-HCl pH8.5, 250 mM NaCl, 1 mM TCEP, cOmpleteTM protease inhibitor cocktail (Sigma-Aldrich) |
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 35 sec. / 前処理 - 気圧: 25.0 kPa / 詳細: 2 mAu current |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK III |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - 画像ごとのフレーム数: 1-37 / 撮影したグリッド数: 1 / 実像数: 8550 / 平均露光時間: 3.7 sec. / 平均電子線量: 49.75 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 20.0 µm / 最小 デフォーカス(公称値): 5.0 µm / 倍率(公称値): 45000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: BACKBONE TRACE / 温度因子: 75.76 |
|---|---|
| 得られたモデル |  PDB-7pq5: |
 ムービー
ムービー コントローラー
コントローラー












 Z
Z Y
Y X
X