+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-12158 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM structure of Mycobacterium tuberculosis UMP Kinase (UMPK) in complex with UDP and UTP | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | nucleotide metabolism / UMP kinase / allosteric regulation / antibacterial target / TRANSFERASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報UMP kinase / UMP kinase activity / 'de novo' CTP biosynthetic process / ATP binding / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.85 Å | |||||||||
 データ登録者 データ登録者 | Bous J / Trapani S | |||||||||
| 資金援助 | European Union,  フランス, 2件 フランス, 2件
| |||||||||
 引用 引用 |  ジャーナル: FEBS J / 年: 2022 ジャーナル: FEBS J / 年: 2022タイトル: Structural basis for the allosteric inhibition of UMP kinase from Gram-positive bacteria, a promising antibacterial target. 著者: Patrick Walter / Ariel Mechaly / Julien Bous / Ahmed Haouz / Patrick England / Joséphine Lai-Kee-Him / Aurélie Ancelin / Sylviane Hoos / Bruno Baron / Stefano Trapani / Patrick Bron / ...著者: Patrick Walter / Ariel Mechaly / Julien Bous / Ahmed Haouz / Patrick England / Joséphine Lai-Kee-Him / Aurélie Ancelin / Sylviane Hoos / Bruno Baron / Stefano Trapani / Patrick Bron / Gilles Labesse / Hélène Munier-Lehmann /  要旨: Tuberculosis claims significantly more than one million lives each year. A feasible way to face the issue of drug resistance is the development of new antibiotics. Bacterial uridine 5'-monophosphate ...Tuberculosis claims significantly more than one million lives each year. A feasible way to face the issue of drug resistance is the development of new antibiotics. Bacterial uridine 5'-monophosphate (UMP) kinase is a promising target for novel antibiotic discovery as it is essential for bacterial survival and has no counterpart in human cells. The UMP kinase from M. tuberculosis is also a model of particular interest for allosteric regulation with two effectors, GTP (positive) and UTP (negative). In this study, using X-ray crystallography and cryo-electron microscopy, we report for the first time a detailed description of the negative effector UTP-binding site of a typical Gram-positive behaving UMP kinase. Comparison between this snapshot of low affinity for Mg-ATP with our previous 3D-structure of the GTP-bound complex of high affinity for Mg-ATP led to a better understanding of the cooperative mechanism and the allosteric regulation of UMP kinase. Thermal shift assay and circular dichroism experiments corroborate our model of an inhibition by UTP linked to higher flexibility of the Mg-ATP-binding domain. These new structural insights provide valuable knowledge for future drug discovery strategies targeting bacterial UMP kinases. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_12158.map.gz emd_12158.map.gz | 62.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-12158-v30.xml emd-12158-v30.xml emd-12158.xml emd-12158.xml | 16.9 KB 16.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_12158_fsc.xml emd_12158_fsc.xml | 9.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_12158.png emd_12158.png | 113.4 KB | ||
| マスクデータ |  emd_12158_msk_1.map emd_12158_msk_1.map | 67 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-12158.cif.gz emd-12158.cif.gz | 6 KB | ||
| その他 |  emd_12158_half_map_1.map.gz emd_12158_half_map_1.map.gz emd_12158_half_map_2.map.gz emd_12158_half_map_2.map.gz | 51 MB 50.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-12158 http://ftp.pdbj.org/pub/emdb/structures/EMD-12158 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12158 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12158 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_12158_validation.pdf.gz emd_12158_validation.pdf.gz | 981.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_12158_full_validation.pdf.gz emd_12158_full_validation.pdf.gz | 981.4 KB | 表示 | |
| XML形式データ |  emd_12158_validation.xml.gz emd_12158_validation.xml.gz | 16.2 KB | 表示 | |
| CIF形式データ |  emd_12158_validation.cif.gz emd_12158_validation.cif.gz | 21.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12158 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12158 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12158 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12158 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_12158.map.gz / 形式: CCP4 / 大きさ: 67 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_12158.map.gz / 形式: CCP4 / 大きさ: 67 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.052 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
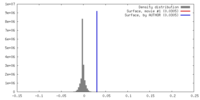
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_12158_msk_1.map emd_12158_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
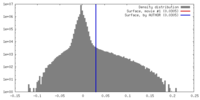
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_12158_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
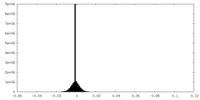
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_12158_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
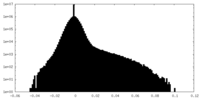
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : UMPK-UDP-UTP
| 全体 | 名称: UMPK-UDP-UTP |
|---|---|
| 要素 |
|
-超分子 #1: UMPK-UDP-UTP
| 超分子 | 名称: UMPK-UDP-UTP / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 177.558 KDa |
-分子 #1: Uridylate kinase
| 分子 | 名称: Uridylate kinase / タイプ: protein_or_peptide / ID: 1 / コピー数: 3 / 光学異性体: LEVO / EC番号: UMP kinase |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 29.625893 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGSSHHHHHH SSGLVPRGSH MTEPDVAGAP ASKPEPASTG AASAAQLSGY SRVLLKLGGE MFGGGQVGLD PDVVAQVARQ IADVVRGGV QIAVVIGGGN FFRGAQLQQL GMERTRSDYM GMLGTVMNSL ALQDFLEKEG IVTRVQTAIT MGQVAEPYLP L RAVRHLEK ...文字列: MGSSHHHHHH SSGLVPRGSH MTEPDVAGAP ASKPEPASTG AASAAQLSGY SRVLLKLGGE MFGGGQVGLD PDVVAQVARQ IADVVRGGV QIAVVIGGGN FFRGAQLQQL GMERTRSDYM GMLGTVMNSL ALQDFLEKEG IVTRVQTAIT MGQVAEPYLP L RAVRHLEK GRVVIFGAGM GLPYFSTDTT AAQRALEIGA DVVLMAKAVD GVFAEDPRVN PEAELLTAVS HREVLDRGLR VA DATAFSL CMDNGMPILV FNLLTDGNIA RAVRGEKIGT LVTT UniProtKB: Uridylate kinase |
-分子 #2: URIDINE-5'-DIPHOSPHATE
| 分子 | 名称: URIDINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 3 / 式: UDP |
|---|---|
| 分子量 | 理論値: 404.161 Da |
| Chemical component information | 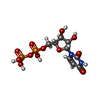 ChemComp-UDP: |
-分子 #3: URIDINE 5'-TRIPHOSPHATE
| 分子 | 名称: URIDINE 5'-TRIPHOSPHATE / タイプ: ligand / ID: 3 / コピー数: 2 / 式: UTP |
|---|---|
| 分子量 | 理論値: 484.141 Da |
| Chemical component information | 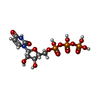 ChemComp-UTP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3 mg/mL | ||||||
|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 / 構成要素:
| ||||||
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY | ||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / 平均電子線量: 53.6 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / 温度因子: 87.61 |
|---|---|
| 得られたモデル |  PDB-7bes: |
 ムービー
ムービー コントローラー
コントローラー














 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)