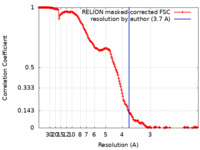
登録情報 データベース : EMDB / ID : EMD-11969タイトル A 3.7-angstrom structure of Yarrowia lipolytica complex I with an R121M mutation in NUCM. Final map globally sharpened with RELION postprocess 複合体 : Yarrowia lipolytica mitochondrial complex I (NADH:Ubiquinone oxidoreductase) with NUCM R121M mutationタンパク質・ペプチド : x 3種リガンド : x 10種 / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Yarrowia lipolytica (酵母)手法 / / 解像度 : 3.7 Å Hirst J / Grba D 資金援助 Organization Grant number 国 Medical Research Council (MRC, United Kingdom) MC_U105663141 Medical Research Council (MRC, United Kingdom) MC_UU_00015/2
ジャーナル : J Biol Chem / 年 : 2021タイトル : A conserved arginine residue is critical for stabilizing the N2 FeS cluster in mitochondrial complex I.著者 : Mikhail A Hameedi / Daniel N Grba / Katherine H Richardson / Andrew J Y Jones / Wei Song / Maxie M Roessler / John J Wright / Judy Hirst / 要旨 : Respiratory complex I (NADH:ubiquinone oxidoreductase), the first enzyme of the electron-transport chain, captures the free energy released by NADH oxidation and ubiquinone reduction to translocate ... Respiratory complex I (NADH:ubiquinone oxidoreductase), the first enzyme of the electron-transport chain, captures the free energy released by NADH oxidation and ubiquinone reduction to translocate protons across an energy-transducing membrane and drive ATP synthesis during oxidative phosphorylation. The cofactor that transfers the electrons directly to ubiquinone is an iron-sulfur cluster (N2) located in the NDUFS2/NUCM subunit. A nearby arginine residue (R121), which forms part of the second coordination sphere of the N2 cluster, is known to be posttranslationally dimethylated but its functional and structural significance are not known. Here, we show that mutations of this arginine residue (R121M/K) abolish the quinone-reductase activity, concomitant with disappearance of the N2 signature from the electron paramagnetic resonance (EPR) spectrum. Analysis of the cryo-EM structure of NDUFS2-R121M complex I at 3.7 Å resolution identified the absence of the cubane N2 cluster as the cause of the dysfunction, within an otherwise intact enzyme. The mutation further induced localized disorder in nearby elements of the quinone-binding site, consistent with the close connections between the cluster and substrate-binding regions. Our results demonstrate that R121 is required for the formation and/or stability of the N2 cluster and highlight the importance of structural analyses for mechanistic interpretation of biochemical and spectroscopic data on complex I variants. 履歴 登録 2020年11月20日 - ヘッダ(付随情報) 公開 2021年3月10日 - マップ公開 2021年3月10日 - 更新 2025年12月17日 - 現状 2025年12月17日 処理サイト : PDBe / 状態 : 公開
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
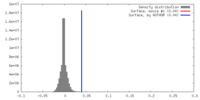
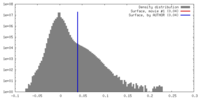
基本情報 マップデータ
マップデータ 試料
試料 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Yarrowia lipolytica (酵母)
Yarrowia lipolytica (酵母) データ登録者
データ登録者 英国, 2件
英国, 2件  引用
引用 ジャーナル: J Biol Chem / 年: 2021
ジャーナル: J Biol Chem / 年: 2021
 構造の表示
構造の表示 ムービービューア
ムービービューア SurfView
SurfView Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク emd_11969.map.gz
emd_11969.map.gz EMDBマップデータ形式
EMDBマップデータ形式 emd-11969-v30.xml
emd-11969-v30.xml emd-11969.xml
emd-11969.xml EMDBヘッダ
EMDBヘッダ emd_11969_fsc.xml
emd_11969_fsc.xml FSCデータファイル
FSCデータファイル emd_11969.png
emd_11969.png emd_11969_msk_1.map
emd_11969_msk_1.map マスクマップ
マスクマップ emd-11969.cif.gz
emd-11969.cif.gz emd_11969_half_map_1.map.gz
emd_11969_half_map_1.map.gz emd_11969_half_map_2.map.gz
emd_11969_half_map_2.map.gz http://ftp.pdbj.org/pub/emdb/structures/EMD-11969
http://ftp.pdbj.org/pub/emdb/structures/EMD-11969 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11969
ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11969 リンク
リンク EMDB (EBI/PDBe) /
EMDB (EBI/PDBe) /  EMDataResource
EMDataResource マップ
マップ ダウンロード / ファイル: emd_11969.map.gz / 形式: CCP4 / 大きさ: 347.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES)
ダウンロード / ファイル: emd_11969.map.gz / 形式: CCP4 / 大きさ: 347.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) emd_11969_msk_1.map
emd_11969_msk_1.map 試料の構成要素
試料の構成要素 解析
解析 試料調製
試料調製 電子顕微鏡法
電子顕微鏡法 FIELD EMISSION GUN
FIELD EMISSION GUN
 ムービー
ムービー コントローラー
コントローラー




























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)