+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8fxi | ||||||
|---|---|---|---|---|---|---|---|
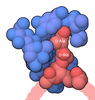
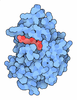
| タイトル | Cryo-EM structure of Stanieria sp. CphA2 in complex with ADPCP and 4x(beta-Asp-Arg) | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | LIGASE / cyanophycin / CphA2 / ATP-grasp | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報N-acetyl-L-aspartate-L-glutamate ligase activity / ribosomal S6-glutamic acid ligase activity / SOS response / ATP binding / metal ion binding / cytoplasm 類似検索 - 分子機能 | ||||||
| 生物種 |  Stanieria sp. NIES-3757 (バクテリア) Stanieria sp. NIES-3757 (バクテリア)synthetic construct (人工物) | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.7 Å | ||||||
 データ登録者 データ登録者 | Markus, L.M. / Sharon, I. / Strauss, M. / Schmeing, T.M. | ||||||
| 資金援助 |  カナダ, 1件 カナダ, 1件
| ||||||
 引用 引用 |  ジャーナル: Protein Sci / 年: 2023 ジャーナル: Protein Sci / 年: 2023タイトル: Structure and function of a hexameric cyanophycin synthetase 2. 著者: Linda M D Markus / Itai Sharon / Kim Munro / Marcel Grogg / Donald Hilvert / Mike Strauss / T Martin Schmeing /   要旨: Cyanophycin is a natural polymer composed of a poly-aspartate backbone with arginine attached to each of the aspartate sidechains. Produced by a wide range of bacteria, which mainly use it as a store ...Cyanophycin is a natural polymer composed of a poly-aspartate backbone with arginine attached to each of the aspartate sidechains. Produced by a wide range of bacteria, which mainly use it as a store of fixed nitrogen, it has many promising industrial applications. Cyanophycin can be synthesized from the amino acids Asp and Arg by the widespread cyanophycin synthetase 1 (CphA1), or from the dipeptide β-Asp-Arg by the cyanobacterial enzyme cyanophycin synthetase 2 (CphA2). CphA2 enzymes display a range of oligomeric states, from dimers to dodecamers. Recently, the crystal structure of a CphA2 dimer was solved but could not be obtained in complex with substrate. Here, we report cryo-EM structures of the hexameric CphA2 from Stanieria sp. at ~2.8 Å resolution, both with and without ATP analog and cyanophycin. The structures show a two-fold symmetrical, trimer-of-dimers hexameric architecture, and substrate-binding interactions that are similar to those of CphA1. Mutagenesis experiments demonstrate the importance of several conserved substrate-binding residues. We also find that a Q416A/R528G double mutation prevents hexamer formation and use this double mutant to show that hexamerization augments the rate of cyanophycin synthesis. Together, these results increase our mechanistic understanding of how an interesting green polymer is biosynthesized. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8fxi.cif.gz 8fxi.cif.gz | 722.1 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8fxi.ent.gz pdb8fxi.ent.gz | 596.7 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8fxi.json.gz 8fxi.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  8fxi_validation.pdf.gz 8fxi_validation.pdf.gz | 1.5 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  8fxi_full_validation.pdf.gz 8fxi_full_validation.pdf.gz | 1.6 MB | 表示 | |
| XML形式データ |  8fxi_validation.xml.gz 8fxi_validation.xml.gz | 120.5 KB | 表示 | |
| CIF形式データ |  8fxi_validation.cif.gz 8fxi_validation.cif.gz | 178.8 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/fx/8fxi https://data.pdbj.org/pub/pdb/validation_reports/fx/8fxi ftp://data.pdbj.org/pub/pdb/validation_reports/fx/8fxi ftp://data.pdbj.org/pub/pdb/validation_reports/fx/8fxi | HTTPS FTP |
-関連構造データ
| 関連構造データ |  29534MC  8fxhC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 72886.516 Da / 分子数: 6 / 由来タイプ: 組換発現 / 由来: (組換発現) Stanieria sp. NIES-3757 / 遺伝子: STA3757_02480 / 発現宿主:  #2: タンパク質・ペプチド | 分子量: 1103.106 Da / 分子数: 2 / 由来タイプ: 合成 / 由来: (合成) synthetic construct (人工物) #3: 化合物 | ChemComp-YHZ / | #4: 化合物 | ChemComp-MG / #5: 化合物 | ChemComp-ACP / | 研究の焦点であるリガンドがあるか | Y | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Stanieria sp. CphA2 in complex with ADPCP and 4x(beta-Asp-Arg) タイプ: COMPLEX / Entity ID: #1 / 由来: RECOMBINANT |
|---|---|
| 由来(天然) | 生物種:  Stanieria sp. (バクテリア) Stanieria sp. (バクテリア) |
| 由来(組換発現) | 生物種:  |
| 緩衝液 | pH: 7.5 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: SPOT SCAN FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: SPOT SCAN |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): -2.5 nm / 最小 デフォーカス(公称値): -1 nm |
| 撮影 | 電子線照射量: 80 e/Å2 フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) |
- 解析
解析
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION |
|---|---|
| 3次元再構成 | 解像度: 2.7 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 549663 / 対称性のタイプ: POINT |
 ムービー
ムービー コントローラー
コントローラー




 PDBj
PDBj