+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8639 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM map of Hrd1 dimer with one Hrd3 molecule | |||||||||
 マップデータ マップデータ | Hrd1 dimer with one Hrd3 binding map with low-pass filtering to 4.7A and applied -250 b-factor | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Hrd1p ubiquitin ligase ERAD-M complex / detection of unfolded protein / luminal surveillance complex / Hrd1p ubiquitin ligase complex / Hrd1p ubiquitin ligase ERAD-L complex / negative regulation of protein autoubiquitination / retrograde protein transport, ER to cytosol / ERAD pathway / endoplasmic reticulum membrane / endoplasmic reticulum 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
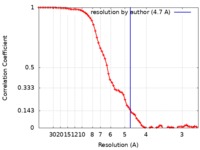
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.7 Å | |||||||||
 データ登録者 データ登録者 | Schoebel S / Mi W / Stein A / Rapoport TA / Liao M | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2017 ジャーナル: Nature / 年: 2017タイトル: Cryo-EM structure of the protein-conducting ERAD channel Hrd1 in complex with Hrd3. 著者: Stefan Schoebel / Wei Mi / Alexander Stein / Sergey Ovchinnikov / Ryan Pavlovicz / Frank DiMaio / David Baker / Melissa G Chambers / Huayou Su / Dongsheng Li / Tom A Rapoport / Maofu Liao /    要旨: Misfolded endoplasmic reticulum proteins are retro-translocated through the membrane into the cytosol, where they are poly-ubiquitinated, extracted from the membrane, and degraded by the proteasome-a ...Misfolded endoplasmic reticulum proteins are retro-translocated through the membrane into the cytosol, where they are poly-ubiquitinated, extracted from the membrane, and degraded by the proteasome-a pathway termed endoplasmic reticulum-associated protein degradation (ERAD). Proteins with misfolded domains in the endoplasmic reticulum lumen or membrane are discarded through the ERAD-L and ERAD-M pathways, respectively. In Saccharomyces cerevisiae, both pathways require the ubiquitin ligase Hrd1, a multi-spanning membrane protein with a cytosolic RING finger domain. Hrd1 is the crucial membrane component for retro-translocation, but it is unclear whether it forms a protein-conducting channel. Here we present a cryo-electron microscopy structure of S. cerevisiae Hrd1 in complex with its endoplasmic reticulum luminal binding partner, Hrd3. Hrd1 forms a dimer within the membrane with one or two Hrd3 molecules associated at its luminal side. Each Hrd1 molecule has eight transmembrane segments, five of which form an aqueous cavity extending from the cytosol almost to the endoplasmic reticulum lumen, while a segment of the neighbouring Hrd1 molecule forms a lateral seal. The aqueous cavity and lateral gate are reminiscent of features of protein-conducting conduits that facilitate polypeptide movement in the opposite direction-from the cytosol into or across membranes. Our results suggest that Hrd1 forms a retro-translocation channel for the movement of misfolded polypeptides through the endoplasmic reticulum membrane. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8639.map.gz emd_8639.map.gz | 25 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8639-v30.xml emd-8639-v30.xml emd-8639.xml emd-8639.xml | 14.6 KB 14.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_8639_fsc.xml emd_8639_fsc.xml | 8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_8639.png emd_8639.png | 96.7 KB | ||
| その他 |  emd_8639_additional.map.gz emd_8639_additional.map.gz | 20.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8639 http://ftp.pdbj.org/pub/emdb/structures/EMD-8639 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8639 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8639 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_8639_validation.pdf.gz emd_8639_validation.pdf.gz | 505.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_8639_full_validation.pdf.gz emd_8639_full_validation.pdf.gz | 504.8 KB | 表示 | |
| XML形式データ |  emd_8639_validation.xml.gz emd_8639_validation.xml.gz | 9.5 KB | 表示 | |
| CIF形式データ |  emd_8639_validation.cif.gz emd_8639_validation.cif.gz | 12.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8639 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8639 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8639 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8639 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8637C  8638C  8642C  5v6pC  5v7vC C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10099 (タイトル: Cryo-EM structure of Hrd1 and Hrd3 complex / Data size: 708.3 EMPIAR-10099 (タイトル: Cryo-EM structure of Hrd1 and Hrd3 complex / Data size: 708.3 Data #1: summed frame micrographs of Hrd1/Hrd3 complex [micrographs - single frame] Data #2: dose-weighted summed frame micrographs of Hrd1/Hrd3 complex [micrographs - single frame] Data #3: picked particles of Hrd1/Hrd3 complex [picked particles - multiframe - processed]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8639.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8639.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Hrd1 dimer with one Hrd3 binding map with low-pass filtering to 4.7A and applied -250 b-factor | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
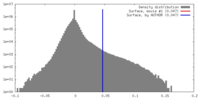
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.35 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-追加マップ: Hrd1 dimer with one Hrd3 binding map without...
| ファイル | emd_8639_additional.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Hrd1 dimer with one Hrd3 binding map without filtering or amplitude modification | ||||||||||||
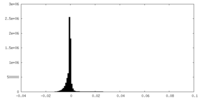
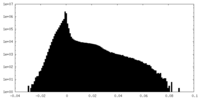
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Hrd1 dimer with one Hrd3 molecule
| 全体 | 名称: Hrd1 dimer with one Hrd3 molecule |
|---|---|
| 要素 |
|
-超分子 #1: Hrd1 dimer with one Hrd3 molecule
| 超分子 | 名称: Hrd1 dimer with one Hrd3 molecule / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #1: ERAD-associated E3 ubiquitin-protein ligase HRD1
| 分子 | 名称: ERAD-associated E3 ubiquitin-protein ligase HRD1 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MVPENRRKQL AIFVVVTYLL TFYCVYSATK TSVSFLQVTL KLNEGFNLMV LSIFILLNST LL WQLLTKL LFGELRLIEH EHIFERLPFT IINTLFMSSL FHERYFFTVA FFGLLLLYLK VFHWILKDRL EALLQSINDS TTMKTLIFSR FSFNLV LLA VVDYQIITRC ...文字列: MVPENRRKQL AIFVVVTYLL TFYCVYSATK TSVSFLQVTL KLNEGFNLMV LSIFILLNST LL WQLLTKL LFGELRLIEH EHIFERLPFT IINTLFMSSL FHERYFFTVA FFGLLLLYLK VFHWILKDRL EALLQSINDS TTMKTLIFSR FSFNLV LLA VVDYQIITRC ISSIYTNQKS DIESTSLYLI QVMEFTMLLI DLLNLFLQTC LNFWEFYRSQ QSLSNENNHI VHGDPTDENT VESDQSQPVL NDDDDDDDD DRQFTGLEGK FMYEKAIDVF TRFLKTALHL SMLIPFRMPM MLLKDVVWDI LALYQSGTSL WKIWRNNKQL DDTLVTVTVE QLQN SANDD NICIICMDEL IHSPNQQTWK NKNKKPKRLP CGHILHLSCL KNWMERSQTC PICRLPVFDE K |
-分子 #2: ERAD-associated E3 ubiquitin-protein ligase component HRD3
| 分子 | 名称: ERAD-associated E3 ubiquitin-protein ligase component HRD3 タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MITLLLYLCV ICNAIVLIRA DSIADPWPEA RHLLNTIAKS RDPMKEAAME PNADEFVGFY VPMDYSPRN EEKNYQSIWQ NEITDSQRHI YELLVQSSEQ FNNSEATYTL SQIHLWSQYN F PHNMTLAH KYLEKFNDLT HFTNHSAIFD LAVMYATGGC ASGNDQTVIP ...文字列: MITLLLYLCV ICNAIVLIRA DSIADPWPEA RHLLNTIAKS RDPMKEAAME PNADEFVGFY VPMDYSPRN EEKNYQSIWQ NEITDSQRHI YELLVQSSEQ FNNSEATYTL SQIHLWSQYN F PHNMTLAH KYLEKFNDLT HFTNHSAIFD LAVMYATGGC ASGNDQTVIP QDSAKALLYY QR AAQLGNL KAKQVLAYKY YSGFNVPRNF HKSLVLYRDI AEQLRKSYSR DEWDIVFPYW ESY NVRISD FESGLLGKGL NSVPSSTVRK RTTRPDIGSP FIAQVNGVQM TLQIEPMGRF AFNG NDGNI NGDEDDEDAS ERRIIRIYYA ALNDYKGTYS QSRNCERAKN LLELTYKEFQ PHVDN LDPL QVFYYVRCLQ LLGHMYFTGE GSSKPNIHMA EEILTTSLEI SRRAQGPIGR ACIDLG LIN QYITNNISQA ISYYMKAMKT QANNGIVEFQ LSKLATSFPE EKIGDPFNLM ETAYLNG FI PAIYEFAVMI ESGMNSKSSV ENTAYLFKTF VDKNEAIMAP KLRTAFAALI NDRSEVAL W AYSQLAEQGY ETAQVSAAYL MYQLPYEFED PPRTTDQRKT LAISYYTRAF KQGNIDAGV VAGDIYFQMQ NYSKAMALYQ GAALKYSIQA IWNLGYMHEH GLGVNRDFHL AKRYYDQVSE HDHRFYLAS KLSVLKLHLK SWLTWITREK VNYWKPSSPL NPNEDTQHSK TSWYKQLTKI L QRMRHKED SDKAAEDSHK HRTVVQNGAN HRGDDQEEAS EILGFQMEDG GGENLYFQSG GG MDEKTTG WRGGHVVEGL AGELEQLRAR LEHHPQGQRE P |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.8 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 400 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 82.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)