+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-7466 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Segment NFGTFS, with familial mutation A315T and phosphorylated threonine, from the low complexity domain of TDP-43, residues 312-317 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報nuclear inner membrane organization / interchromatin granule / perichromatin fibrils / 3'-UTR-mediated mRNA destabilization / 3'-UTR-mediated mRNA stabilization / intracellular non-membrane-bounded organelle / negative regulation by host of viral transcription / pre-mRNA intronic binding / response to endoplasmic reticulum stress / RNA splicing ...nuclear inner membrane organization / interchromatin granule / perichromatin fibrils / 3'-UTR-mediated mRNA destabilization / 3'-UTR-mediated mRNA stabilization / intracellular non-membrane-bounded organelle / negative regulation by host of viral transcription / pre-mRNA intronic binding / response to endoplasmic reticulum stress / RNA splicing / negative regulation of protein phosphorylation / molecular condensate scaffold activity / mRNA 3'-UTR binding / regulation of protein stability / regulation of circadian rhythm / positive regulation of insulin secretion / mRNA processing / positive regulation of protein import into nucleus / cytoplasmic stress granule / rhythmic process / regulation of gene expression / double-stranded DNA binding / regulation of apoptotic process / amyloid fibril formation / regulation of cell cycle / nuclear speck / RNA polymerase II cis-regulatory region sequence-specific DNA binding / negative regulation of gene expression / lipid binding / mitochondrion / DNA binding / RNA binding / nucleoplasm / identical protein binding / nucleus 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 電子線結晶学 / クライオ電子顕微鏡法 | |||||||||
 データ登録者 データ登録者 | Guenther EL / Cao Q / Boyer DR / Sawaya MR / Eisenberg DS | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2018 ジャーナル: Nat Struct Mol Biol / 年: 2018タイトル: Atomic structures of TDP-43 LCD segments and insights into reversible or pathogenic aggregation. 著者: Elizabeth L Guenther / Qin Cao / Hamilton Trinh / Jiahui Lu / Michael R Sawaya / Duilio Cascio / David R Boyer / Jose A Rodriguez / Michael P Hughes / David S Eisenberg /  要旨: The normally soluble TAR DNA-binding protein 43 (TDP-43) is found aggregated both in reversible stress granules and in irreversible pathogenic amyloid. In TDP-43, the low-complexity domain (LCD) is ...The normally soluble TAR DNA-binding protein 43 (TDP-43) is found aggregated both in reversible stress granules and in irreversible pathogenic amyloid. In TDP-43, the low-complexity domain (LCD) is believed to be involved in both types of aggregation. To uncover the structural origins of these two modes of β-sheet-rich aggregation, we have determined ten structures of segments of the LCD of human TDP-43. Six of these segments form steric zippers characteristic of the spines of pathogenic amyloid fibrils; four others form LARKS, the labile amyloid-like interactions characteristic of protein hydrogels and proteins found in membraneless organelles, including stress granules. Supporting a hypothetical pathway from reversible to irreversible amyloid aggregation, we found that familial ALS variants of TDP-43 convert LARKS to irreversible aggregates. Our structures suggest how TDP-43 adopts both reversible and irreversible β-sheet aggregates and the role of mutation in the possible transition of reversible to irreversible pathogenic aggregation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_7466.map.gz emd_7466.map.gz | 456.1 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-7466-v30.xml emd-7466-v30.xml emd-7466.xml emd-7466.xml | 15.1 KB 15.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_7466.png emd_7466.png | 262.2 KB | ||
| Filedesc structureFactors |  emd_7466_sf.cif.gz emd_7466_sf.cif.gz | 106.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-7466 http://ftp.pdbj.org/pub/emdb/structures/EMD-7466 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7466 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7466 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_7466_validation.pdf.gz emd_7466_validation.pdf.gz | 298.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_7466_full_validation.pdf.gz emd_7466_full_validation.pdf.gz | 297.8 KB | 表示 | |
| XML形式データ |  emd_7466_validation.xml.gz emd_7466_validation.xml.gz | 4 KB | 表示 | |
| CIF形式データ |  emd_7466_validation.cif.gz emd_7466_validation.cif.gz | 4.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7466 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7466 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7466 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7466 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6cf4MC  7467C  8857C  5whnC  5whpC  5wiaC  5wiqC  5wkbC  5wkdC  6cb9C  6cewC  6cfhC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_7466.map.gz / 形式: CCP4 / 大きさ: 525.4 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_7466.map.gz / 形式: CCP4 / 大きさ: 525.4 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 これらの図は立方格子座標系で作成されたものです | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X: 0.197 Å / Y: 0.197 Å / Z: 0.188 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
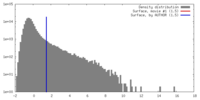
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : crystal of NFGTFS phosphorylated on threonine.
| 全体 | 名称: crystal of NFGTFS phosphorylated on threonine. |
|---|---|
| 要素 |
|
-超分子 #1: crystal of NFGTFS phosphorylated on threonine.
| 超分子 | 名称: crystal of NFGTFS phosphorylated on threonine. / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: NFGTFS
| 分子 | 名称: NFGTFS / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 751.679 Da |
| 配列 | 文字列: NFG(TPO)FS |
-分子 #2: water
| 分子 | 名称: water / タイプ: ligand / ID: 2 / コピー数: 1 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 電子線結晶学 |
| 試料の集合状態 | 3D array |
- 試料調製
試料調製
| 緩衝液 | pH: 4 |
|---|---|
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 支持フィルム - Film thickness: 30.0 nm / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
| 結晶化 | 脂質混合液: none / 装置: microcentrifuge tube / 雰囲気: air, sealed chamber / 温度: 310.0 K / 時間: 4.0 DAY 詳細: Crystals were prepared by shaking peptide in microcentrifuge tube at 37 deg Celsius for 4 days. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 温度 | 最低: 100.0 K / 最高: 100.0 K |
| 撮影 | フィルム・検出器のモデル: TVIPS TEMCAM-F416 (4k x 4k) デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 撮影したグリッド数: 1 / 回折像の数: 100 / 平均露光時間: 3.0 sec. / 平均電子線量: 0.01 e/Å2 詳細: The detector was operated in rolling shutter mode with 2X2 pixel binning. |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: DIFFRACTION / カメラ長: 819 mm |
| 試料ステージ | 試料ホルダーモデル: GATAN 626 SINGLE TILT LIQUID NITROGEN CRYO TRANSFER HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 解像度の算出法: DIFFRACTION PATTERN/LAYERLINES / ソフトウェア - 名称: SHELXD (ver. 2013/2) / ソフトウェア - 詳細: direct methods 詳細: Density map was obtained using measured diffraction intensities and phases acquired from a crystallographic direct methods program, shelxd. | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶パラメータ | 単位格子 - A: 23.650 Å / 単位格子 - B: 4.720 Å / 単位格子 - C: 30.060 Å / 単位格子 - γ: 90.00 ° / 単位格子 - α: 90.00 ° / 単位格子 - β: 90.00 ° / 空間群: P 21 21 21 | ||||||||||||||||||||||||||||
| Crystallography statistics | Number intensities measured: 15891 / Number structure factors: 4177 / Fourier space coverage: 86.6 / R sym: 17.2 / R merge: 17.2 / Overall phase error: 32.2 / Overall phase residual: 32.2 / Phase error rejection criteria: 0 / High resolution: 0.75 Å 殻:
|
-原子モデル構築 1
| 精密化 | 空間: RECIPROCAL / プロトコル: OTHER / 温度因子: 19.6 / 当てはまり具合の基準: maximum likihood |
|---|---|
| 得られたモデル |  PDB-6cf4: |
 ムービー
ムービー コントローラー
コントローラー





 Y (Sec.)
Y (Sec.) X (Row.)
X (Row.) Z (Col.)
Z (Col.)